КЛИНИЧЕСКИЙ СЛУЧАЙ УСПЕШНОГО ЛЕЧЕНИЯ ПОДРОСТКА С САРКОМОЙ ЮИНГА IV СТАДИИ | Кит
1. Александрова Г.А., Какорина Е.П., Караваева Л.В., Купеева И.А., Рыков М.Ю., Поляков В.Г. Эпидемиология злокачественных новообразований у детей: основные показатели в 2011–2016 гг. М., 2017. 208 с.
2. Ewing J. The classic: diffuse endothelioma of bone. Proceedings of the New York Pathological Society. 1921; 12: 17. Clin Orthop Relat Res. 2006; 450: 25–27. doi: 10.1097/01.blo.0000229311.36007.c7.
3. Юрченко Д.Ю., Бурцев Д.В., Кузнецов С.А., Сагакянц А.Б., Мкртчян Г.А., Старжецкая М.В., Беспалова А.И., Поповян О.П., Куштова Л.Б. Некоторые особенности молекулярно-генетического патогенеза Саркомы Юинга (обзор литературы). Современные проблемы науки и образования.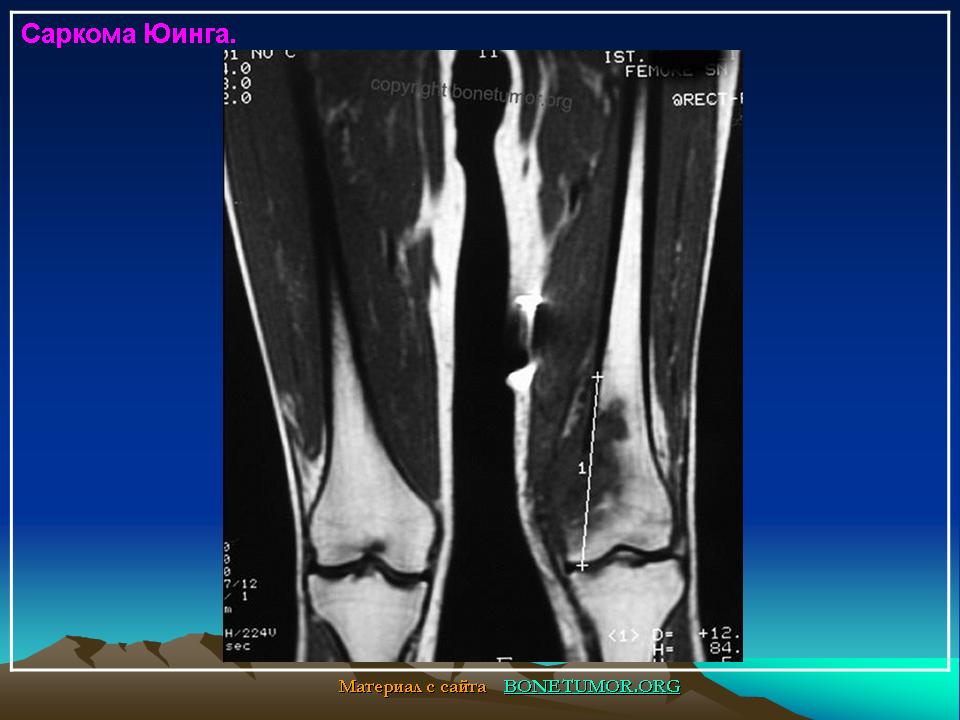
4. Рыков М.Ю. «Клинические маски» костных сарком у детей: шесть клинических случаев. Вопросы современной педиатрии. 2018; 17(1): 89–93. doi: 10.15690/vsp.v17i1.1860.
5. Кит О.И., Балязин-Парфёнов И.В., Барашев А.А.; Ростовский научно-исследовательский онкологический институт. Способ лечения опухолей позвоночника. Патент № 2551622, МПК A61B, А61К, А61Р. № 20141063936; Заявл. 20.04.14; Опубл. 27.05.15, Бюл. № 15.
7. Рыков М.Ю., Севрюков Д.Д., Вилкова А.С. Злокачественные новообразования у детей: Клинические проявления и диагностика. Вопросы современной педиатрии. 2017; 16(5): 370–382. doi: 10.15690/Vsp.V16i5.1801.
Рыков М.Ю., Севрюков Д.Д., Вилкова А.С. Злокачественные новообразования у детей: Клинические проявления и диагностика. Вопросы современной педиатрии. 2017; 16(5): 370–382. doi: 10.15690/Vsp.V16i5.1801.
Саркома мягких тканей – причины, симптомы, стадии и лечение саркомы в клинике ЕМС в Москве
Лечение сарком мягких тканей и остеосарком в EMC проводится междисциплинарной командой специалистов, включающей в себя медицинских онкологов, радиологов, хирургов-ортопедов со специализацией в онкологии, патоморфологов и реабилитологов. План лечения пациента с диагнозом саркома разрабатывается на онкологическом консилиуме. Врачи Института онкологии EMC специализируются на лечении редких видов онкологических заболеваний с использованием современных методов хирургического лечения, лучевой и химиотерапии.
Саркомы представляют собой редкую и разнородную группу злокачественных опухолей: менее 1% всех злокачественных новообразований у взрослых и около 12% случаев рака у детей.
Наиболее распространенные подтипы сарком мягких тканей у взрослых:
-
гастроинтестинальные стромальные опухоли (ГИСО, ГИСТ).
-
липосаркома
-
лейомиосаркома
-
недифференцированная плеоморфная саркома
- недифференцированная саркома мягких тканей и др.
Важно различать виды сарком, как с точки зрения прогноза, так и с точки зрения различий в лечении. Это особенно важно для педиатрических опухолей, которые развиваются у взрослых, таких как рабдомиосаркома (РМС). Как эмбриональные, так и альвеолярные РМС более восприимчивы к химиотерапии и имеют лучший прогноз, чем многие типы сарком мягких тканей у взрослых. Тем не менее, плеоморфные РМС имеют относительно неблагоприятный прогноз, по сравнению с другими подтипами РМС. Такие опухоли преобладают у взрослых, и исходы при данном виде саркомы хуже, чем у детей.
Этиология и патогенез
Почти во всех случаях саркомы возникают первично, а не развиваются из доброкачественных поражений. В большинстве случаев точная этиология неясна, но определено есть несколько сопутствующих или предрасполагающих факторов.
К ним относятся:
-
генетическая предрасположенность (например, синдром Ли Фраумени, нейрофиброматоз I типа, ретинобластома)
-
воздействие лучевой терапии или химиотерапии
-
химические канцерогены
-
лимфедема (отек мягких тканей пораженной области)
-
вирус иммунодефицита человека (ВИЧ) и вирус герпеса 8 типа (при саркоме Капоши)
Симптомы сарком мягких тканей
Наиболее частой жалобой при саркомах мягких тканей является постепенно увеличивающееся в размерах безболезненное объемное образование. Опухоли могут достигать достаточно больших размеров, особенно в области бедра и забрюшинном пространстве.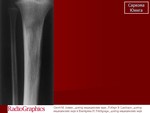
Саркомы мягких тканей могут развиваться в любой части тела, но чаще всего на конечностях.
По данным Американской коллегии хирургов локализация сарком мягких тканей распределяется следующим образом:
-
Бедро, ягодицы и паховая область – 46%
-
Верхние конечности – 13%
-
Туловище – 18%
-
Забрюшинное пространство – 13%
-
Голова и шея – 9%
Наличие отдаленных метастазов на момент первичного установления диагноза наблюдается нечасто, но более вероятно при крупных, глубоких саркомах высокой степени злокачественности.
Распространение в регионарные лимфоузлы при саркомах мягких тканей встречается редко.
Наиболее высокий риск метастазирования в лимфоузлы характерен для рабдомиосаркомы, синовиальной саркомы, эпителиоидной саркомы, светлоклеточной саркомы и сосудистых сарком (включая ангиосаркомы).
Факторы прогноза при саркоме мягких тканей
Наиболее важными прогностическими факторами являются гистологическая оценка, размер опухоли и стадия на момент постановки диагноза.
В исследовании, проведенном Memorial Sloan Kettering Cancer Center (MSKCC) с использованием классификации злокачественных новообразований TNM, 5-летние показатели безрецидивной выживаемости для I, II и III стадии заболеваний составили 86, 72 и 52% соответственно.
Диагностика сарком мягких тканей
Первоначальная оценка пациента с подозрением на саркому мягких тканей начинается со сбора анамнеза. Устанавливается скорость роста опухоли и наличие симптомов, позволяющих предположить нейроваскулярное нарушение.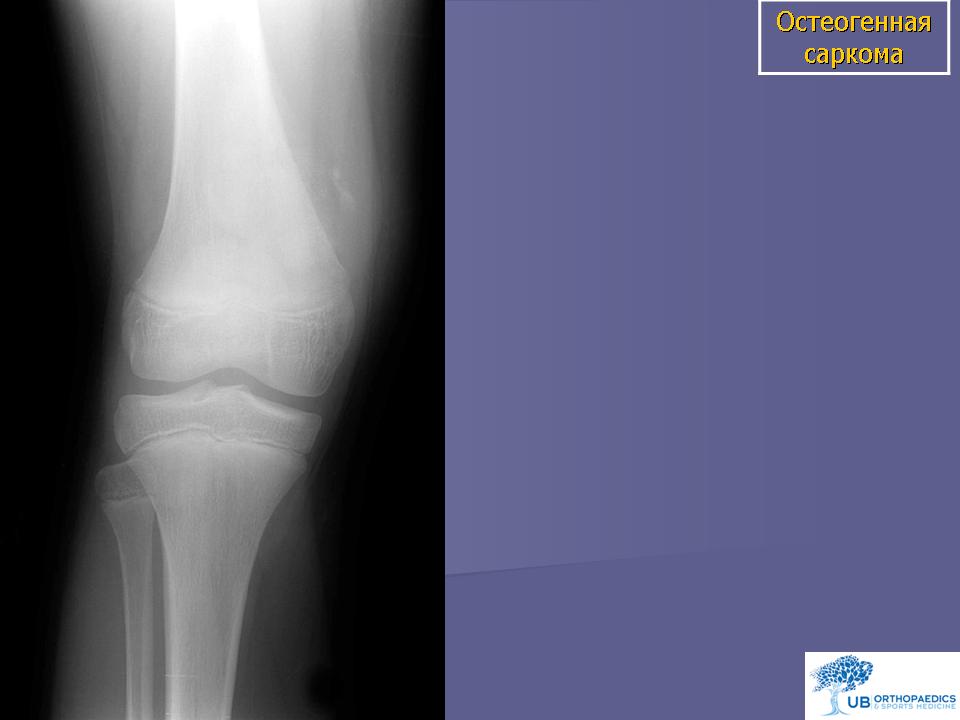 При физическом обследовании уделяется особое внимание размеру и глубине расположения опухоли, ее связи с окружающими структурами, наличию сопутствующего отека или признаков вовлечения нервов.
При физическом обследовании уделяется особое внимание размеру и глубине расположения опухоли, ее связи с окружающими структурами, наличию сопутствующего отека или признаков вовлечения нервов.
Нередко диагноз саркомы мягких тканей устанавливают поздно. Пациенты часто откладывают обращение за медицинской помощью, поскольку опухоль безболезненна.
Частичное иссечение опухоли до направления к специалисту может привести к появлению отдаленных метастазов и необходимости расширенной повторной резекции. Диагностическая биопсия, проведенная несоответствующим образом, может помешать последующему проведению хирургической резекции, косметическому восстановлению, или привести к необходимости более масштабного хирургического вмешательства. Поэтому рекомендовано как можно раньше обратиться в специализированное медицинское учреждение.
Диагностическое обследование опухолей мягких тканей включает в себя:
-
Магнитно-резонансную топографию (МРТ) при опухолях конечностей, туловища, области головы и шеи или компьютерную топографию (КТ) при опухолях брюшной полости и забрюшинного пространства
Толстоигольную биопсию с последующим морфологическим исследованием, если это технически выполнимо.
 Если требуется открытая (инцизионная) биопсия, она должна быть тщательно спланирована и выполнена хирургом, который будет проводить тотальную резекцию.
Если требуется открытая (инцизионная) биопсия, она должна быть тщательно спланирована и выполнена хирургом, который будет проводить тотальную резекцию.
Морфологическое исследование образцов, подозрительных на саркомы мягких тканей, проводится в собственной гистологической лаборатории EMC. При необходимости материалы биопсии могут быть пересмотрены в лабораториях клиник-партнеров EMC в Израиле, Германии или США.
Как только диагноз саркомы мягких тканей подтвержден, проводится исследование органов грудной клетки всем пациентам, чтобы проверить наличие метастазов в легких. У пациентов с высоким риском метастазирования в легкие (опухоли >5 см, глубоко расположенные или имеющие среднюю или высокую степень злокачественности) используется КТ. При круглоклеточных/миксоидных липомах рекомендуется также КТ брюшной полости и таза, поскольку часто встречаются внелегочные метастазы в брюшной полости и забрюшинном пространстве.
Исследование с визуализацией головного мозга предлагается пациентам с ангиосаркомой и альвеолярной саркомой мягких тканей, поскольку эти опухоли характеризуются высокой склонностью к метастазированию в центральную нервную систему.
В повседневной практике позитронно-эмиссионная топография (ПЭТ) или ПЭТ/КТ для первичной оценки стадии при впервые установленном диагнозе саркомы мягких тканей не проводится. ПЭТ или сканирование с галлием может быть значимым у пациентов с нейрофиброматозом в качестве вспомогательного метода дифференциальной диагностики.
Лечение сарком мягких тканей
В большинстве случаев лечение сарком комбинированное. На выбор метода лечения влияет размер и расположение опухоли, степень злокачественности, а также распространенность процесса.
Хирургия как единственный метод лечения может применяться только в том случае, если опухоль высокодифференцированная и возможно ее радикальное удаление.
Хирургическое лечение сарком мягких тканей
Хирургическая резекция первичной опухоли является основным компонентом лечения практически всех пациентов с саркомами мягких тканей конечностей. У большинства пациентов возможна резекция опухоли с адекватными границами резекции, и этот метод позволяет сохранить функцию конечности; небольшой подгруппе пациентов может потребоваться первичная ампутация.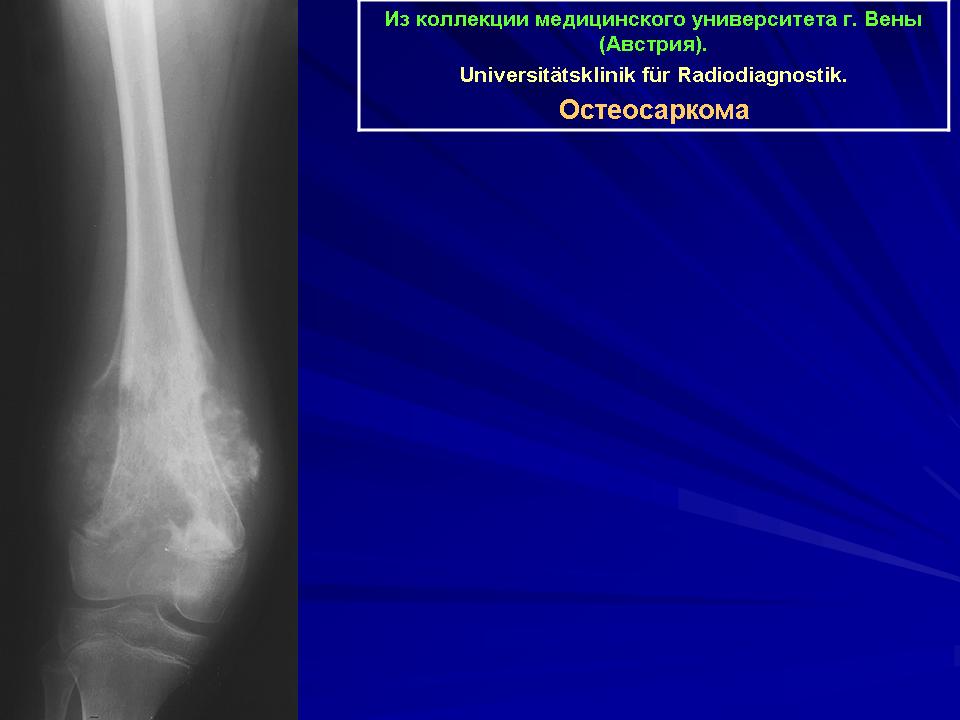
Резекция должна проводиться с захватом тканей, выходящих за пределы псевдокапсулы опухоли, если таковая есть, до достижения визуально здоровой, не вовлеченной в процесс ткани. Повреждение опухоли (т.е. рассечение опухоли или резекция, после которой остается макроскопический или микроскопический остаточный фрагмент опухоли) связано с более высокой частотой местного рецидива, даже если проводится лучевая терапия (ЛТ). Границы резекции служат наиболее важным показателем, который влияет на местный контроль опухоли.
Лучевая терапия сарком мягких тканей
Применение лучевой терапии в сочетании с резекцией снижает необходимость в ампутации и увеличивает вероятность удаления саркомы при сохранении функции конечности. В большинстве случаев сочетание операции с сохранением конечности и лучевой терапии обеспечивает лучший местный контроль.
Послеоперационная лучевая терапия значительно повлияла на частоту сохранения конечностей при саркомах мягких тканей конечностей.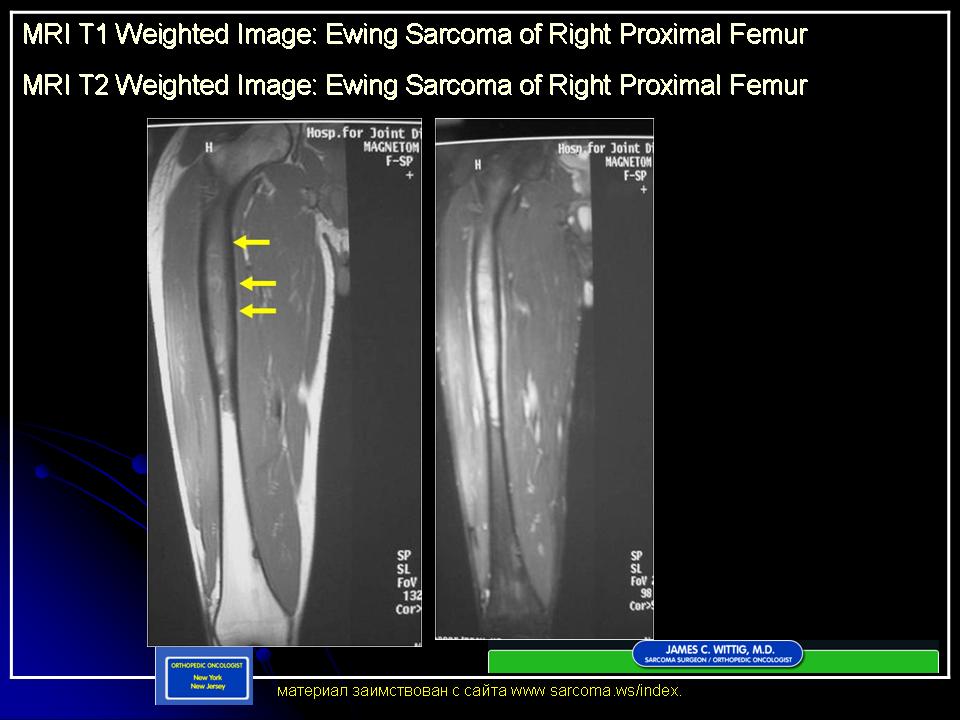 В 1970-е годы примерно половине пациентов с СМТ конечностей проводилась ампутация. С развитием лучевой терапии частота ампутаций сократилась почти до 1% без ощутимого снижения общей выживаемости.
В 1970-е годы примерно половине пациентов с СМТ конечностей проводилась ампутация. С развитием лучевой терапии частота ампутаций сократилась почти до 1% без ощутимого снижения общей выживаемости.
Метастазы саркомы. Химиотерапия.
Хирургическая резекция при метастатическом процессе обеспечивает долгосрочную безрецидивную выживаемость и, возможно, излечение у отдельных пациентов, у большинства из которых имеются изолированные метастазы в легких. Однако большинству пациентов с метастатическими саркомами мягких тканей химиотерапия назначается в качестве паллиативного лечения с целью уменьшения общего объема опухоли, уменьшения симптомов, улучшения качества жизни и увеличения выживаемости.
Естественное течение заболевания у пациентов с нерезектабельным метастатическим заболеванием может быть различным и в большей степени зависит от биологических особенностей опухоли, а не от лечения. У некоторых пациентов с бессимптомным нерезектабельным заболеванием низкой степени злокачественности может быть рациональным наблюдение за пациентом без активной химиотерапии. И, наоборот, у пациентов с опухолью высокой степени злокачественности, чувствительной к химиотерапии, такой как синовиальная саркома или липосаркома, может быть предпочтительным раннее начало комбинированной химиотерапии.
И, наоборот, у пациентов с опухолью высокой степени злокачественности, чувствительной к химиотерапии, такой как синовиальная саркома или липосаркома, может быть предпочтительным раннее начало комбинированной химиотерапии.
НМИЦ онкологии им. Н.Н. Блохина
Вот уже почти 70 лет Онкоцентр – это уникальный симбиоз науки и клинической практики, мультидисциплинарный подход к лечению онкологических больных, хирургическая школа, известная далеко за пределами России. Здесь изучаются и совершенствуются морфологические, иммунологические и генетические методы диагностики.Специалисты Блохина – авторы клинических рекомендаций по онкологии.
Ежегодно в Онкоцентре противоопухолевое лечение проходят более 35 тысяч пациентов всех возрастов. Еще почти 6 000 граждан России получают помощь дистанционно – посредством телемедицинских консультаций.
Онкоцентр – это:
- Комбинированное лечение пациентов
- Собственное производство химио- и радиофармацевтических препаратов
- Собственные методы иммунотерапии опухолей
- Передовые технологии реабилитации онкопациентов
- «Центры компетенций» по различным нозологиям, в том числе первый в России центр компетенций по лечению пациентов с опухолями без выявленного первичного очага
- Собственное отделение переливания крови, доноры которого снабжают кровью и ее компонентами исключительно пациентов Онкоцентра
- Первый и единственный онкологический центр, имеющий в своем составе специализированное отделение реабилитации для онкопациентов
- Крупнейшая педагогическая школа в области онкологии в России
На протяжении многих лет Онкоцентр является членом Международного Противоракового Союза (UICC) при Всемирной организации здравоохранения (ВОЗ) и членом Ассоциации Европейских Онкологических Институтов (OECI) в Женеве.
В 2019 году НИИ детской онкологии и гематологии НМИЦ онкологии им. Н.Н. Блохина стал полноправным членом ведущей мировой организации, которая объединяет трансплантационные центры Европы и мира — Европейской группы по трансплантации крови и костного мозга (EBMT).
НМИЦ онкологии им. Н.Н. Блохина:
- Онкологическая помощь мирового уровня, доступная каждому
- Инновации в онкологии
- Уникальный опыт для коллег
Врачи Морозовской больницы провели сложную операцию мальчику с Саркомой Юинга
В Морозовской детской клинической больнице Департамента здравоохранения Москвы провели сложную операцию по эндопротезированию большеберцовой кости 12-летнему ребенку из Севастополя с диагнозом Саркома Юинга.
Появление припухлости в области правой голени впервые появились у мальчика в мае 2018 года, но этот симптом, как и боли при ходьбе, ребенок связал с травмой, полученной на тренировке. Родители мальчика обратились в травмпункт по месту жительства, после чего ребенка госпитализировали в местную городскую больницу с подозрением на опухоль.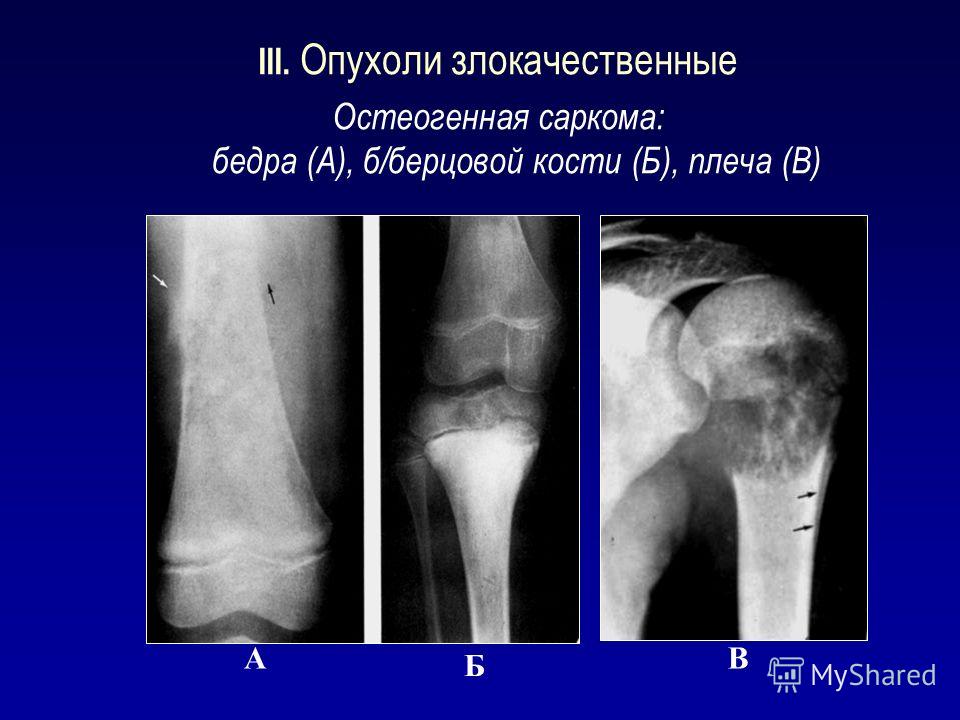 В отделении травматологии были проведены все необходимые обследования, и полученные данные подтвердили наличие новообразования в верхней трети правой голени. Для более детального обследования и дальнейшего лечения ребенок был направлен на госпитализацию в Морозовскую детскую городскую клиническую больницу.
В отделении травматологии были проведены все необходимые обследования, и полученные данные подтвердили наличие новообразования в верхней трети правой голени. Для более детального обследования и дальнейшего лечения ребенок был направлен на госпитализацию в Морозовскую детскую городскую клиническую больницу.
В онкологическом отделении Морозовской больницы ребенку провели полный комплекс диагностических исследований, включающий лабораторную диагностику, УЗИ, КТ и МРТ, а также сцинтиграфию костей скелета. Для установки диагноза врачи произвели биопсию новообразования правой большеберцовой кости, результат которой подтвердил наличие у ребенка Саркомы Юинга.
Саркома Юинга является злокачественной опухолью и чаще всего диагностируется в подростковом и молодом возрасте. Поражение проксимального отдела большеберцовой кости является типичным для данного вида опухоли. К сожалению, саркомы Юинга довольно быстро метастазируют. Установив диагноз и стадию заболевания, ребенку незамедлительно назначили необходимое лечение. Благодаря нескольким курсам химиотерапии, врачам удалось добиться уменьшения опухоли, после чего появилась возможность провести операцию.
Благодаря нескольким курсам химиотерапии, врачам удалось добиться уменьшения опухоли, после чего появилась возможность провести операцию.
— Мальчик хорошо перенес химиотерапевтическое лечение, поэтому врачи приняли решение об удалении пораженной части кости и установке раздвижного эндопротеза, чтобы спасти ногу. Для таких случаев в медицине используется раздвижной неинвазивный эндопротез, что позволяет в дальнейшем увеличивать длину конечности без операции по мере роста ребенка. Эндопротезирование длинных трубчатых костей при злокачественных опухолях у детей в Морозовской больнице проводится второй раз и является «золотым стандартом» в онкологической ортопедии, — рассказывает Максим Кубиров, заведующий отделением клинической онкологии Морозовской детской клинической больницы.
Операция по удалению кости, пораженной опухолью, и установке эндопротеза длилась 7 часов. Учитывая сложное расположение опухоли, протяженность поражения и близкое расположение магистральных сосудов, хирургическая бригада была сформирована из врачей хирургов онкологов и травматологов-ортопедов. Вмешательство проводили Максим Сергеевич Кубиров, заведующий отделением клинической онкологии, Михаил Анатольевич Петров, заведующий отделением травматологии и ортопедии, а также Иван Владимирович Панкратов, травматолог-ортопед.
Вмешательство проводили Максим Сергеевич Кубиров, заведующий отделением клинической онкологии, Михаил Анатольевич Петров, заведующий отделением травматологии и ортопедии, а также Иван Владимирович Панкратов, травматолог-ортопед.
Операция прошла успешно, сейчас мальчик чувствует себя хорошо и продолжает проходить лечение. По прогнозам врачей, после периода реабилитации, ребенок сможет жить обычной жизнью, регулярно наблюдаясь у врачей по месту жительства.
Лечение рака костей в Германии, , Цены
Общие сведения
Рак костей встречается не так часто по сравнению с другими видами онкологии. По статистике эта разновидность заболевания обнаруживается в 1 случае из 100. К примеру, в Германии данный тип ежегодно выявляют только у нескольких сотен людей. Профессионально проведенная диагностика и правильно подобранная терапия увеличивают шансы на выздоровление. Лечение рака костей в Германии – шанс получить и первое, и второе. Разберемся над тем, как производятся исследования и какие методы терапии существуют.
Также опухоль может иметь вторичный характер, то есть образовываться из раковых клеток легкого, простаты, молочной или щитовидной железы.
Симптомы зависят от ее размера и положения, а также от типа:
- Остеосаркома обычно диагностируется благодаря возникающему болезненному отеку. Кожа на этом месте становится красного или синего цвета, имеется явно выраженная венозная сетка. Очаговое образование оказывает сильное влияние на подвижность пораженной части тела. У многих пациентов остеосаркома поражает длинные трубчатые кости рук или ног, а также коленные суставы.
- Саркома Юинга характеризуется схожими симптомами – она провоцирует отек и болевые ощущения.
 Встречается в малом тазу и в длинных трубчатых костях ног. У некоторых больных наблюдается температура.
Встречается в малом тазу и в длинных трубчатых костях ног. У некоторых больных наблюдается температура. - Симптомы хондросаркомы аналогичны двум другим подвидам. Место ее локализации – спина. Больные жалуются на ее онемение и возникающую слабость.
- Первая является начальной. Образование имеет низкую степень злокачественности, местом его локализации является кость. Хорошо поддается терапии – выживаемость на этой стадии очень высокая. Именно поэтому специалисты говорят о своевременности обращения.
- На второй стадии наблюдаются изменения в клетках – они утрачивают дифференцировку, постепенно превращаясь в злокачественные. Метастазов еще не наблюдается.
- Для третьей стадии типична высокая степень злокачественности, начинают деформироваться мягкие ткани рядом с костью.
- Лечение рака костей 4 стадии под силу лишь опытным и квалифицированным онкологам. Она является последней. У новообразования могут быть любые размеры.
 Обнаруживаются метастазы во внутренних органах, тканях, лимфатических узлах. Часто проблемы наблюдаются с легкими и лимфатической системой. При использовании различных методов визуализации изменения в скелете четко просматриваются. Для данной стадии характерна низкая выживаемость пациентов.
Обнаруживаются метастазы во внутренних органах, тканях, лимфатических узлах. Часто проблемы наблюдаются с легкими и лимфатической системой. При использовании различных методов визуализации изменения в скелете четко просматриваются. Для данной стадии характерна низкая выживаемость пациентов.
Диагностика
При первом посещении доктор собирает анамнез, задает вопросы о симптомах, которые вызывают беспокойство. Далее врач производит внешний осмотр, начиная с зоны поражения и места возможного прорастания метастазов. На ранних стадиях такая диагностика не всегда помогает определить наличие злокачественных процессов. Поэтому, если есть подозрение на рак кости, врач обычно делает рентгеновские снимки (преимущественно применяется к взрослым, т.к. у детей результативность метода низкая – во время роста и развития все заболевания ОДА имеют одинаковую картину на снимках). Опухоль можно распознать на снимках следующим образом: виднеются участки с нечеткими контурами и дефектами костного вещества.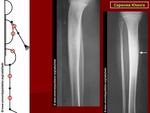 Иногда такое изображение говорит врачу о характере и типе новообразования.
Иногда такое изображение говорит врачу о характере и типе новообразования.
Также одно из первых действий доктора при обращении с подозрительными симптомами – взятие крови и мочи на анализ. При злокачественных процессах уровень гемоглобина и железа снижается, скорость оседания эритроцитов, наоборот, повышается.
В случае обнаружения ненормированных значений основных показателей проводится исследование на онкомаркеры. Обычно в случае с раком костей делают два анализа – ТГ (гормональный белок щитовидки, который помогает обнаружить в костных тканях новообразование), TRAP 5b (выявляет такие формы, как остеогенная саркома и саркома Юинга).
Более точные сведения о пораженном участке получают при помощи биопсии. Сначала иголкой забирают у пациента образец ткани, а затем исследуют под микроскопом в лаборатории. Каждый тип образования изменяет клетки особым образом. На основе этих изменений врач определяет природу новообразования.
Чтобы узнать его точное местонахождение и размер, применяются КТ и МРТ. Наличие дочерних образований в других частях скелета и органах просматривается при помощи сцинтиграфии и УЗИ.
Сцинтиграфия выполняется с введением радиофармпрепарата. Именно он помогает выявить очаговые изменения, рассчитать активность накопления вещества в метастазах – это позволяет определить динамику развития заболевания.
Лечение
Терапия зависит от типа и стадии рака костей. Как правило, специалисты используют несколько методов в комплексе. Среди них:
- химиотерапия;
- операция;
- лекарства;
- лучевая терапия.
Чтобы полностью убрать новообразование, врачам приходится прибегать к удалению значительных частей костной ткани. Утраченные части заменяются имплантатами. Существует несколько видов операций:
- Органосберегающая – ее проводят в 90% случаев при онкологии верхних и нижних конечностей. Основной целью метода является удаление пораженных тканей без затрагивания нервных окончаний, кровеносных сосудов, связок, находящихся рядом с местом поражения. Это возможно только на первых стадиях. Вырезанная кость заменяется на трансплантат, функциональность сохраняется.
- Реконструктивное вмешательство. Второй вариант термина – ротационная пластика. Хирург производит частичное удаление конечности. Убирается средняя часть, в которой наблюдается очаг поражения. При этом верхняя и нижняя соединяются между собой. Важно, что подобное вмешательство предполагает сохранение функционирования конечности, которая после операции становится значительно короче. Длина восстанавливается при помощи протезирования.
- Ампутация. Подход предполагает частичное или полное удаление конечности. Хирург убирает не только пораженные, но и часть здоровых тканей около участка поражения. Метод применяется только в том случае, если использование органосберегающего подхода не представляется возможным.
После оперативного вмешательства процедуры не заканчиваются – доктора часто назначают несколько способов лечения в сочетании друг с другом. Наряду с этим многим пациентам требуется вспомогательная реконструктивная хирургия – с ее помощью восстанавливают полноценное функционирование ранее прооперированной части ОДС.
Применение медикаментов актуально для любого из раковых больных. В процессе терапии пациенты получают обезболивающие препараты, которые купируют болевой синдром и оказывают противовоспалительное действие, бисфосфонаты, используемые для устранения осложнений и симптомов болезни. При сильных болях применяются лекарственные наркотические средства, отпускаемые по рецепту.
При остеосаркоме предпочтительным методом лечения является хирургическая операция в сочетании с химиотерапией. В некоторых случаях «химия» проводится перед оперативным вмешательством – так можно уменьшить размер опухоли. Хирургия помогает в удалении основных и вторичных новообразований. После этого пациент проходит 18-недельный курс химиотерапии, чтобы убить стремительно размножающиеся раковые клетки.
Саркома Юинга требует комбинации всех трех указанных методик. Сначала в течение 10 недель проводится химиотерапия с применением различных лекарств. На этой фазе целью является сокращение или даже удаление первичных и вторичных образований. Химиотерапия также может помочь в устранении вторичных очагов, которые не удается обнаружить методами визуализации.
Опухоль может быть удалена в ходе операции. Если локализация очага или состояние здоровья пациента не позволяют произвести хирургическое вмешательство, можно рассмотреть вопрос о внедрении лучевой терапии. Даже при условии, что врач удалил все вторичные очаги, после операции они, как правило, появляются снова. Именно поэтому далее должна проводиться химиотерапия. В целом лечение данного типа саркомы занимает около года.
Большинство хондросарком удаляется во время операции. Эта форма плохо реагирует на включение в курс химиотерапии или лучевой терапии.
Прогноз
Скорость восстановления больного, реакция на медикаменты и включение разных методов, прогнозы – все это зависит от стадии заболевания и от его типа. Главное при борьбе с раком – своевременное выявление.
Остеосаркомы обычно очень быстро распространяются на другие части тела. При их наличии в органах и системах могут образовываться вторичные очаги, наиболее часто этому процессу подвергаются легкие. Если при наличии такого типа новообразования не получили развития вторичные опухоли, то у 50 – 70 человек из 100 есть шанс прожить еще 5 лет после постановки диагноза.
Саркома Юинга. Благодаря внедрению химиотерапии с использованием эффективных медицинских препаратов продолжительность жизни пациентов с этой формой в последние годы увеличилась. При условии отсутствия вторичных опухолей на момент постановки диагноза от 50 до 75 человек из 100 проживут дольше 5 лет.
Если же опухоль значительно распространится, то из 100 страдающих заболеванием жизнь будет продлена на 3 – 5 лет только для 20 – 50 человек.
При хондросаркоме все зависит от размера и расположения опухоли. Важное значение имеет степень дифференцированности новообразования. Она показывает, насколько пораженная ткань отличается от здоровой. Чем значительнее эта разница, тем опухоль считается более злокачественной и тем меньше шансы пациента на выживание.
Для хондросарком со степенью дифференцировки 1 характерен медленный рост и отсутствие метастазов. Поэтому прогноз при раке костей данного типа положительный: порядка 83 человек из 100 с таким заболеванием живут более 5 лет после постановки диагноза. Количество пациентов, проживших 10 и более лет при данном диагнозе, – от 47 до 77.
Хондросаркомы 2-й степени часто вызывают появление метастазов – это делает их более злокачественными по сравнению с очаговыми образованиями 1 степени. То есть у таких больных менее позитивные прогнозы касаемо выживания: лечение способно продлить жизнь на 10 лет только 38 – 59 людям из 100.
Хондросаркома с 3 степенью дифференцировки быстро распространяется в организме. Из 100 страдающих заболеванием только 15 – 36 проживут еще 10 лет.
Рак костей сложно, практически невозможно предотвратить, так как механизм его развития до сих пор не до конца ясен. Но его можно оперативно обнаружить – и тогда жизнь заболевшего будет спасена, а лечение будет более щадящим и менее продолжительным. В этом могут помочь специалисты немецких клиник. Медицинские учреждения, находящиеся на территории Германии, обладают самым современным оборудованием, квалифицированным персоналом и большим опытом в диагностике и лечении рака костей. Возможность сделать все диагностические и лечебные процедуры быстро, а также современное оснащение клиник и высочайшая квалификация врачей значительно повышают шансы на благоприятный исход.
Лечение саркомы Юинга у детей
Доктор Вадим БережнойОснователь платформы MediGlobus. Медицинский эксперт, Заведующий отделением врачей-координаторов.
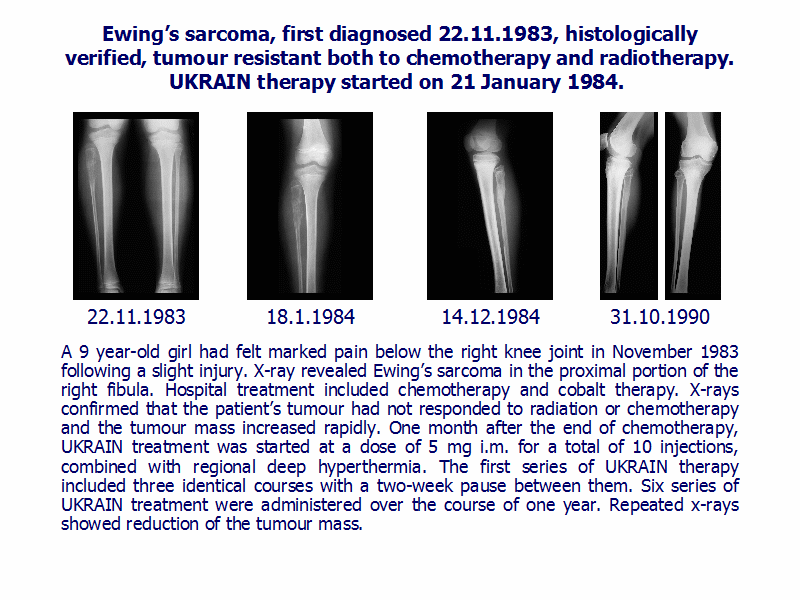
Саркома Юинга – редкий тип рака, который встречается у детей и подростков в возрасте от 10 до 19 лет. Обычно опухоль растет в кости, но также может затрагивать мягкие ткани (сухожилия, связки, хрящи или мышцы). Точная причина появления заболевания неизвестна.
До применения системной терапии у 90% онкобольных появлялись метастазы, что не оставляло шансов на благоприятный исход лечения. Развитие современной медицины позволило противостоять этому тяжелому недугу… Какие методы применяются для борьбы с саркомой Юинга у детей и где лечат данную болезнь за границей – читайте в нашей статье.
Как проявляется Саркома Юинга у детей?
Симптомы этой онкопатологии у каждого ребенка проявиться по-разному. Первые признаки саркомы Юинга легко можно перепутать с другими заболеваниями. Родителям следует насторожиться и обратиться к врачу, если у ребенка отмечается:
Рентген и другие визуальные тесты могут быть использованы для диагностики саркомы Юинга. Также необходима биопсия, которая позволяет поставить точный диагноз. Если у ребенка подтверждено заболевание – постоянный уход во время и после лечения является важным критерием, влияющим на результат терапии.
Получить бесплатную консультацию
Основные методы борьбы с болезнью
Лечение саркомы Юинга зависит от стадии заболевания, локализации опухоли, наличия у пациента сопутствующих патологий, возраста и общего состояния больного. Для повышения показателей эффективности онкотерапии применяется комплексный подход, который подразумевает использование не одного, а нескольких методов (например, хирургии, химиотерапии и радиотерапии) во время одной программы лечения.
Лечение локализованной саркомы Юинга у детей
При локализованной саркоме Юинга в первую очередь применяется неоадъювантная химиотерапия, проводимая в течение 8–12 недель.
После введения химических препаратов врачи используют визуальные тесты, такие как МРТ и КТ, для оценки состояния опухоли и составления дальнейшего плана лечения.
Если новообразование не выросло (или сократилось в размерах) его удаляют хирургическим путем. При этом доктор убирает максимальный объем опухоль вместе с краем здоровой ткани. В том случае, когда ткань, удаленная вместе с новообразованием, не содержит раковых клеток, проводится химиотерапия (адъювантная).
Если в ткани, удаленной хирургом обнаруживаются онкоклетки, вместе с химией выполняется лучевая терапия. Подобный курс лечения длится примерно 24 недели. Затем врачи проводят детальное обследование организма пациента и составляют дальнейший план лечения или профилактики рецидива болезни.
Химиотерапия
Химиотерапия проводится циклами с периодами отдыха. Наиболее распространенной комбинацией химиотерапевтических препаратов, используемых для локализованной саркомы Юинга, считается: винкристин, доксорубицин, циклофосфамид, этопозид и ифосфамид.
Хирургия
После химиотерапии (иногда и лучевой терапии) для удаления опухоли используется оперативное вмешательство. Немаловажно, что современные методы хирургии позволяют сохранить кость, удалив опухоль без ампутации пораженной конечности.
Радиационная терапия
Лучевая терапия применяется для лечения опухоли, когда операция невозможна. Кроме того, облучение показано, если после хирургического вмешательства обнаружены остаточные онкоклетки или, когда не удалось полностью иссекти новообразование.
Лечение метастатической саркомы Юинга
Метастатическая саркома Юинга лечится комбинированием методов: химиотерапии вместе с хирургией или лучевой терапией. Длительность курса лечения и выбор препаратов, а также способов удаления опухоли, определяется для каждого конкретного случая в индивидуальном порядке.
Химиотерапия
Химиотерапия является основным методом лечения метастатической саркомы Юинга. Как правило, длительность курса варьирует от 12 до 16 недель. Немаловажно, что в случае с лечение метастазирующего рака, системная комбинированная химия (одновременное применение нескольких противораковых препаратов) дает наилучшие показатели.
Высокодозная химиотерапия с сохранением стволовых клеток
Высокие дозы химических препаратов показаны для уничтожения больших очагов опухоли. Однако такое лечение пагубно действует на организм в целом, а особенно – на кроветворные клетки. Чтобы восстановить нормальные функции организма после высокодозной химиотерапии используется трансплантация стволовых клеток.
Стволовые клетки берутся из крови или костного мозга пациента или донора, а затем замораживаются и хранятся до окончания курса терапии. После того, как пациент завершает лечение, хранящиеся стволовые клетки возвращают пациенту посредством инфузии. Эти реинфузированные частицы “врастают” и восстанавливают клетки крови. Химиотерапия со спасением стволовых клеток используется для лечения локализованных и рецидивирующих Саркома Юинга.
Хирургия
Операция показана для удаления первичной опухоли и метастазов саркомы Юинга в легких и других костях. Она делается после химиотерапии или радиационной терапии. Если конечность не удается сохранить, тогда ее удаляют и заменяют на протез.
Радиационная терапия
Лучевая терапия используется до операции, после операции, а также, как самостоятельный метод лечения рака. Она показана при первичной опухоли и метастазах.
Получить бесплатную консультацию
Пересадка костного мозга при саркоме Юинга
Первый шаг в трансплантации стволовых клеток при Саркоме Юинга делается до лечения химиотерапией в высоких дозах. Собственные кроветворные стволовые клетки пациента собирают для последующего использования. Этот тип пересадки называется аутологичным . Другой тип трансплантата стволовых клеток – аллогенный. Он подразумевает использует стволовые клетки донора. Такая пересадка костного мозга не часто используется для лечения опухолей Юинга.
Материал для пересадки берут из собственной крови пациента или костного мозга. Кровь – самый распространенный источник стволовых клеток для трансплантации. Перед забором материала ребенку делают инъекции лекарства с фактором роста в течение нескольких дней. Это лекарство помогает стимулировать выработку стволовых клеток. Процесс сбора стволовых клеток похоже на сдачу крови, но это занимает больше времени. Тонкая гибкая трубка (катетер) используется для забора крови из вены. Кровь поступает в устройство для отделения стволовых клеток. Полученный материал замораживают. Чтобы собрать нужное количество клеток, процедура может проводится несколько раз.
Стволовые клетки также могут быть взяты из костного мозга. Этот процесс выполняется под общим наркозом. Медицинский работник делает несколько проколов в тазовой или тазобедренной кости. Болезненность в месте забора транспаранта может длиться несколько дней. Эти стволовые клетки фильтруются и замораживаются до тех пор, пока они не понадобятся. При Саркоме Юинга такой подход к сбору стволовых клеток используется реже.
Здоровые стволовые клетки, которые попадают в организм после трансплантации, оседают в костном мозге. Они вырабатывают новые клетки крови и разрушают раковые. Благодаря трансплантации костного мозга медицинским работникам удается использовать гораздо более высокие дозы химиотерапии для разрушения опухоли.
Согласно данным Национальный центр биотехнологической информации США, трансплантация костного мозга при рецидивирующей Саркоме Юинга повышает шансы на выживание. Около 45% пациентов преодолевают порог 3-летней выживаемости.
Лечение рецидивирующей детской саркомы Юинга
Рецидивирующую саркому Юинга можно лечить химиотерапией, хирургическим вмешательством, лучевой терапией или комбинацией этих методов. В зависимости от того, какую химиотерапию ребенок уже получил, назначается химия одним или несколькими препаратами другого типа. Также для удаления рецидивирующих опухолей показана операция и лучевая терапия. При этом радиационное облучение проводится для облегчения симптомов онкологии (так называемая паллиативная терапия).
Методы лечения саркомы Юинга, которые изучаются в клинических испытаниях
Прогноз лечения саркомы Юинга у детей
Согласно данным Американского онкологического общества, около 70 % детей с саркомой Юинга входят в стадию стойкой ремиссии и преодолевают порог 5-летней выживаемости. Подростки в возрасте от 15 до 19 лет имеют более низкие показатели, около 56%. Для детей с метастазирующим раком, выживаемость составляет менее 30%.
Благодаря применению высокодозной химиотерапии вместе с тотальным облучением тела и пересадкой костного мозга или периферических стволовых клеток, удается повысить результаты лечения и выживаемость пациентов, даже на поздних стадиях онкологии.
Где лечат саркому Юинга за границей и сколько это стоит?
Для лечения саркомы Юинга у детей иностранные пациенты выбирают ведущие клиники Израиля, Турции, Германии, Испании, а также Австрии, Южной Кореи и Чехии. К их числу относятся: госпиталь Лив Хоспитал, Университетская клиника Кирон в Барселоне, медицинский центр им. Сураски (Ихилов), Университетская клиника Мюнхена им. Людвига-Максимилиана, Венская Частная Клиника, госпиталь СунЧонХян и т.д.
Самые низкие цены на онкотерапию саркомы Юинга отмечаются в турецких и корейских больницах. При этом цена медицинских услуг здесь на 20-40% ниже, чем в некоторых европейских клиниках. К примеру, начальная стоимость операции по удалению саркомы Юинга в Турции оставляет $18,000, аутологичной пересадки костного мозга – $45,000, полный курс химиотерапии – $7,000. Больше информации о ценах на лечение саркомы Юинга за границей читайте перейдя по ссылке.
Подробную информацию о лечении саркомы Юинга у детей можно узнать у координаторов MediGlobus. Наши специалисты помогут с выбором клиники и доктора, а также организуют медицинскую поездку в кратчайшие сроки.
Получить бесплатную консультацию
Доктор Вадим Бережной
Основатель платформы MediGlobus. Медицинский эксперт, Заведующий отделением врачей-координаторов.
Editor
Более 2 лет пишет медицинские тексты. Опыт работы в сфере копирайтинга превышает 6 лет. Имеет образование по направлению “Социально-правовая защита”. Освоила программу медицинских курсов. Изучает коммуникативные техники ведения переговоров с пациентами. В свободное время посещает тренинги и семинары по медицинской психологии.
Похожие посты
Лечение миодистрофии Дюшенна за рубежом — 5 способов продлить жизнь еще на 20 лет
Читать дальшеКак работает вирусная терапия — прорыв в лечении рака кожи
Читать дальшеСаркома Юинга — причины, симптомы, диагностика и лечение
Саркома Юинга – это злокачественное новообразование, развивающееся из костной ткани. Чаще возникает в подростковом или юношеском возрасте. Поражает плоские и длинные трубчатые кости. Является одной из наиболее агрессивных опухолей, склонна к раннему метастазированию. Проявляется болью, затем – отеком, местной гиперемией и гипертермией, а также локальным расширением венозной сети. На поздних стадиях определяется опухоль, нередко возникает патологический перелом пораженной кости. Лечение комбинированное, включает в себя операцию (при возможности – радикальное удаление новообразования) в сочетании с лучевой терапией, а также пред- и послеоперационной химиотерапией.
Общие сведения
Саркома Юинга – злокачественная опухоль костей, характеризующаяся быстрым ростом и ранним появлением метастазов. Обычно развивается у детей, подростков и лиц молодого возраста. Сопровождается болями и местными изменениями мягких тканей (отек, гиперемия, гипертермия). На поздних стадиях опухоль становится заметна при осмотре и пальпации. Лечение осуществляется врачом-онкологом, включает в себя оперативное удаление новообразования, химио- и лучевую терапию.
Саркома Юинга – вторая по частоте злокачественная опухоль костной ткани, возникающая в детском возрасте, составляет от 10 до 15% от общего числа злокачественных новообразований костей. У взрослых старше 30 и детей младше 5 лет встречается редко. Наибольшее количество случаев заболевания приходится на возраст от 10 до 15 лет. Мальчики болеют чаще девочек, европеоиды – чаще представителей негроидной и монголоидной расы.
В отдельных случаях первичное новообразование при этом заболевании возникает в мягких тканях, а не в костях. Такая форма заболевания называется экстраоссальной (внекостной) саркомой Юинга. Кроме того, существуют сходные по характеру и структуре агрессивные злокачественные опухоли, относящиеся к группе так называемых опухолей семейства саркомы Юинга. В эту группу, кроме внекостной и костной саркомы относят ПНЭО (периферические примитивные нейроэктодермальные опухоли). Внекостные формы и ПНЭО в сумме составляют около 15% от всего числа случаев саркомы Юинга.
Саркома Юинга
Причины
Причины развития саркомы Юинга в настоящее время точно не установлены. Однако ряд исследователей в сфере современной онкологии считает, что определенную роль в возникновении этого заболевания играет наследственная предрасположенность. Примерно в 40% случаев выявляется связь с предшествующей травмой. Существуют данные, свидетельствующие о повышении вероятности развития болезни у пациентов с некоторыми разновидностями скелетных аномалий (аневризмальной костной кистой, энхондромой и др.), а также нарушениями внутриутробного развития мочеполовой системы (редупликацией почечной системы, гипоспадиями). Какой-либо связи с воздействием ионизирующей радиации не установлено.
Патанатомия
Чаще всего саркома Юинга выявляется в бедренной кости, костях таза, большеберцовой и малоберцовой кости, лопатке, ребрах, плечевой кости и позвонках. При возникновении в длинных трубчатых костях опухоль обычно локализуется в области диафиза, а затем по мере роста распространяется в сторону эпифизов. Более чем в 90% случаев отмечается интрамедуллярное расположение новообразования и тенденция к распространению опухолевых клеток по костномозговому каналу.
Саркома Юинга наиболее часто метастазирует в легкие. На втором месте по распространенности – метастазы в костный мозг и костную ткань. На поздних стадиях практически у всех больных определяются метастазы в центральную нервную систему. В редких случаях выявляются отдаленные метастазы в плевру, лимфатические узлы средостения, внутренние органы и забрюшинное пространство. Из-за раннего метастазирования к моменту постановки диагноза от 15 до 50% пациентов уже имеют метастазы, которые можно выявить при помощи рутинных исследований. У подавляющего количества больных есть микрометастазы.
Симптомы саркомы Юинга
Первым, самым ранним признаком заболевания становится боль в области поражения. Вначале она слабая или умеренная, самопроизвольно ослабевает или исчезает, а затем появляется снова. В отличие от болей при воспалительных процессах такая боль не ослабевает в покое, по ночам или при фиксации конечности. Напротив, для саркомы Юинга характерно усиление болей в ночное время.
По мере прогрессирования боли становятся более интенсивными, лишают сна и ограничивают повседневную активность. В близлежащем суставе развивается болевая контрактура. Пальпация области поражения болезненна. Температура кожи над ней повышена. Отмечается пастозность мягких тканей, местная гиперемия и расширение подкожных вен. Опухоль быстро увеличивается и (обычно спустя несколько месяцев после возникновения первых симптомов) становится настолько крупной, что ее можно прощупать. На поздних стадиях в области новообразования нередко возникает патологический перелом.
Местные клинические признаки сочетаются с нарастающими симптомами общей опухолевой интоксикации. Больные предъявляют жалобы на слабость и потерю аппетита. Отмечается снижение веса вплоть до истощения. Температура тела повышена до субфебрильных или даже фебрильных цифр. Определяется регионарный лимфаденит. По анализам крови выявляется анемия.
Некоторые симптомы зависят от локализации новообразования. Так, при возникновении саркомы Юинга на костях нижних конечностей появляется хромота. При поражении позвонков возможно развитие компрессионно-ишемической миелопатии с нарушением функции тазовых органов и явлениями параплегии. При новообразованиях в области костей грудной клетки может возникнуть дыхательная недостаточность, плевральный выпот и кровохарканье.
Диагностика
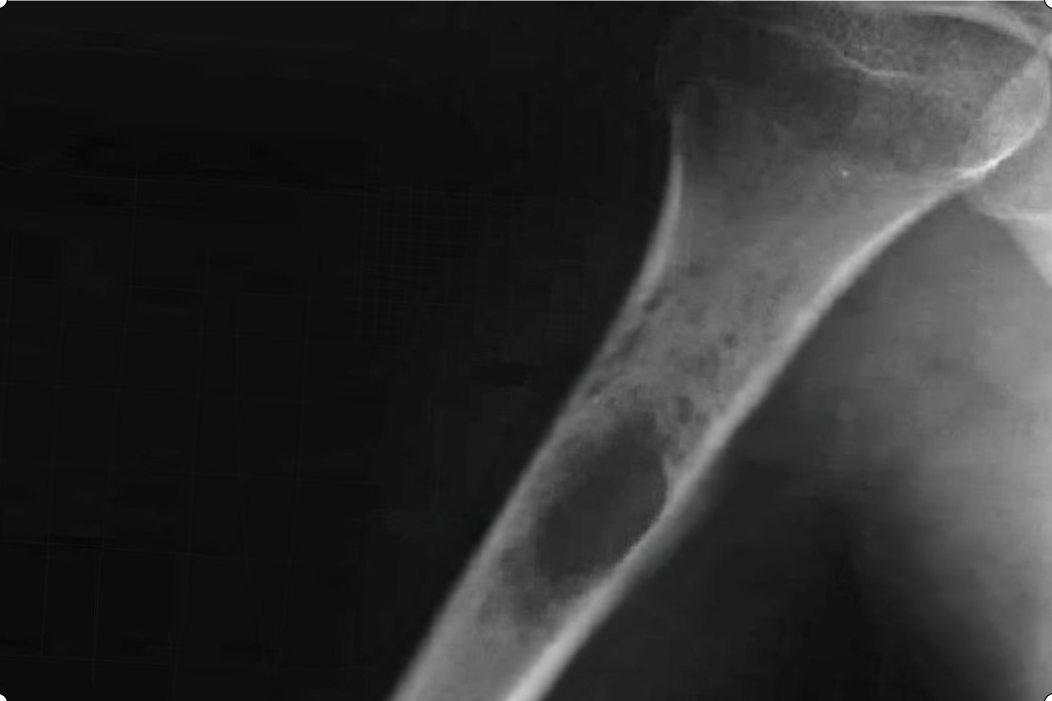
Как правило, на начальном этапе пациенты обращаются к врачам-травматологам. И первым исследованием, позволяющим заподозрить саркому Юинга, становится рентгенография пораженной кости. Для данного патологического процесса характерно сочетание реактивного и деструктивного процессов костеобразования. Контуры кортикального слоя нечеткие, определяется расслоение и разволокнение кортикальной пластинки.
При вовлечении в процесс надкостницы на рентгенограмме выявляются мелкие пластинчатые или игольчатые образования. Кроме того, на снимках видна область изменения мягких тканей, по своему размеру превышающая первичную костную опухоль. При этом мягкотканный опухолевый компонент отличается однородностью, хрящевые включение, очаги обызвествления или патологического костеобразования отсутствуют.
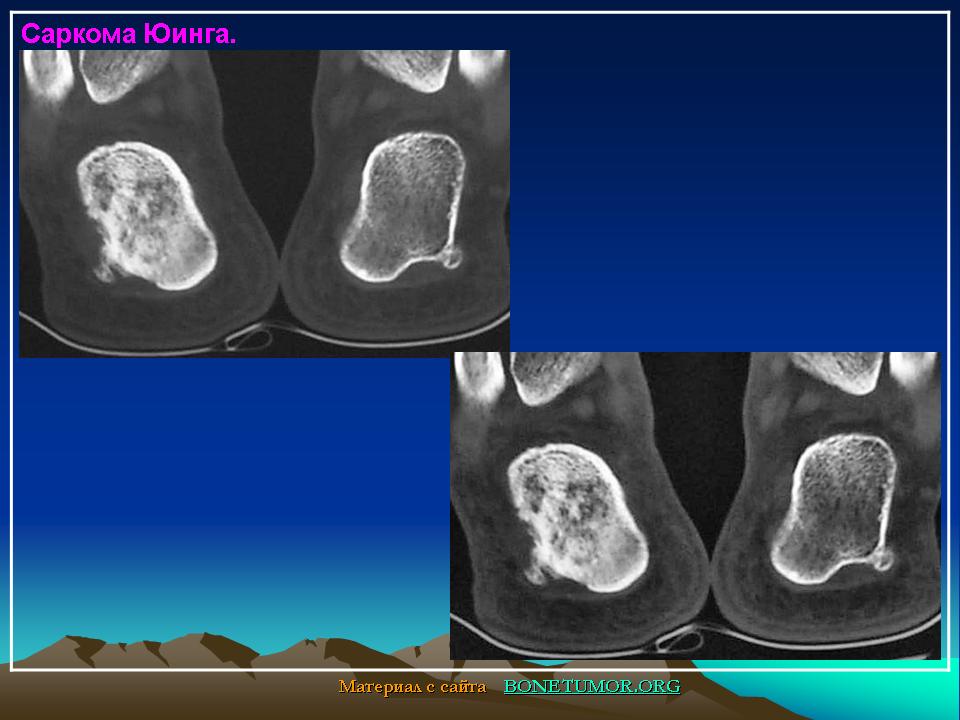
При выявлении типичных рентгенологических признаков саркомы Юинга больного направляют в отделение онкологии, где проводится расширенное обследование для оценки состояния первичного очага и выявления метастазов. В ходе такого обследования выполняется компьютерная томография или магнитно-резонансная томография костей и мягких тканей, пораженных злокачественным процессом. Данные исследования позволяют точно определить размер новообразования, степень его распространения по костно-мозговому каналу, связь с сосудисто-нервным пучком и окружающими тканями.
Для выявления метастазов в легочную ткань применяется компьютерная томография и рентгенография легких. Для обнаружения метастазов в костях, костном мозге и внутренних органах – позитронно-эмиссионная томография, УЗИ и остеосцинтиграфия. Кроме того, выполняется ряд исследований для точной оценки характера новообразования.
Производится биопсия, при этом материал берут из участка костной ткани рядом с костномозговым каналом, либо, если это невозможно – из мягкотканого компонента опухоли. Поскольку для саркомы Юинга характерно местное и отдаленное поражение костного мозга, выполняется билатеральная трепанобиопсия, в ходе которой производится забор костного мозга из крыльев подвздошной кости. Для оценки характера процесса также может проводиться иммуногистохимическое исследование и молекулярно-генетические исследования (флуоресцентная гибридизация – для подтверждения диагноза, полимеразная цепная реакция – для выявления микрометастазов).
КТ ОГК. Патоморфологически подтвержденная саркома Юинга 10-го ребра слева. Кортикальная пластинка ребра с внутренней стороны неравномерно утолщена (красная стрелка). Определяется массивное мягкотканное образование грудной стенки (зеленая стрелка).
Лечение саркомы Юинга
Поскольку данная опухоль относится к категории высокоагрессивных неоплазий, рано дающих метастазы, ее лечение должно включать в себя воздействие на весь организм, а не только на первичный очаг, даже в тех случаях, когда метастазы не были обнаружены. Дело в том, что существует очень высокая вероятность раннего появления микрометастазов, которые на момент постановки диагноза невозможно выявить при помощи существующих методов. Лечение саркомы Юинга комбинированное, включает в себя как консервативную терапию, так и хирургические вмешательства и состоит из следующих компонентов:
- Пред- и послеоперационная химиотерапия, как правило – с использованием нескольких препаратов (доксорубицин, винкристин, циклофосфан, ифосфамид, этопозид и актиномицин в различных комбинациях). После курса лечения оценивается ответ опухоли на терапию. Хорошим результатом считается наличие не более 5% живых клеток опухоли.
- Лучевая терапия с использованием высоких доз. Проводится на первичный очаг, а, при наличии метастазов в легочную ткань – и на легкие.
- Хирургическая операция. Если это возможно, опухоль удаляют радикально, вместе с мягкотканым компонентом. При этом удаленный участок кости заменяют эндопротезом. Но даже если в силу места расположения и размера новообразования удалить его полностью не представляется возможным, оперативное лечение (частичная резекция) позволяет улучшить контроль над опухолью и повысить шансы на благополучный исход.
В прошлом при саркоме Юинга обычно проводились калечащие операции – ампутации и экзартикуляции. Современные техники позволяют выполнять органосохраняющие оперативные вмешательства не только на мелких (малоберцовой, лучевой, локтевой, лопатке, ключице и ребрах), но и на крупных костях (плечевой, бедренной и даже костях таза). При метастазировании в костный мозг и кости назначается интенсивная терапия, включающая в себя тотальное облучение всего тела, химиотерапию с использованием мегадоз препаратов и трансплантацию периферических стволовых клеток или костного мозга.
Прогноз и профилактика
Своевременное комбинированное лечение обеспечивает 70% общую выживаемость пациентов с локализованной саркомой Юинга. При наличии метастазов в кости и костный мозг прогноз существенно ухудшается, однако сочетание высокодозной химиотерапии, тотальной лучевой терапии и трансплантации костного мозга дает возможность повысить выживаемость больных с метастатической формой заболевания с 10% до 30% и более.
Все пациенты после излечения должны проходить регулярное обследование для раннего выявления рецидивов и контроля над побочными эффектами. Следует учитывать, что ряд побочных эффектов может возникать не только при прохождении курса лечения, но и спустя длительное время после его окончания. К числу таких эффектов относится мужское и женское бесплодие, кардиомиопатия, нарушение роста костей и увеличение вероятности развития вторичных злокачественных новообразований. Однако многие пациенты, прошедшие лечение по поводу саркомы Юинга могут жить полноценной жизнью. Профилактика не разработана.
выживаемости при опухоли Юинга | Опухоль Юинга по стадиям
Показатели выживаемости могут дать вам представление о том, какой процент людей с таким же типом и стадией рака все еще жив в течение определенного времени (обычно 5 лет) после того, как им был поставлен диагноз. Они не могут сказать вам, сколько человек проживет, но могут помочь вам лучше понять, насколько вероятно, что лечение будет успешным.
Имейте в виду, что показатели выживаемости являются оценочными и часто основываются на предыдущих результатах большого числа людей, у которых был конкретный рак, но они не могут предсказать, что произойдет в конкретном случае человека.Эта статистика может сбивать с толку и вызывать у вас больше вопросов. Поговорите со своим врачом о том, как эти цифры могут относиться к вам (или вашему ребенку), поскольку он или она знакомы с вашей ситуацией.
Что такое 5-летняя относительная выживаемость?
Относительный коэффициент выживаемости сравнивает людей с одним и тем же типом и стадией рака с людьми в общей популяции. Например, если относительная 5-летняя выживаемость для определенной стадии опухоли Юинга составляет 80%, это означает, что люди, у которых есть этот рак, в среднем примерно на 80% выше, чем люди, у которых этого нет. рак жить не менее 5 лет после постановки диагноза.
Откуда эти числа?
Американское онкологическое общество полагается на информацию из базы данных SEER *, поддерживаемой Национальным институтом рака (NCI), чтобы предоставить статистику выживаемости для различных типов рака.
База данных SEER отслеживает 5-летнюю относительную выживаемость при опухолях Юинга в Соединенных Штатах, основываясь на том, как далеко распространился рак. Однако база данных SEER не группирует раковые заболевания по стадиям AJCC TNM (стадия 1, стадия 2, стадия 3 и т. Д.).). Вместо этого он группирует раковые заболевания на локальные, региональные и отдаленные стадии:
- Локализованный: Нет никаких признаков того, что рак распространился за пределы кости (или другой области), где он начался.
- Региональный: Рак распространился за пределы кости (или другой области) в близлежащие структуры или достиг близлежащих лимфатических узлов.
- Отдаленный: Рак распространился на отдаленные части тела, например, на легкие или кости в других частях тела.
5-летняя относительная выживаемость при опухолях Юинга
Эти цифры основаны на людях, у которых опухоль Юинга была диагностирована в период с 2009 по 2015 год.
SEER стадия | 5-летняя относительная выживаемость |
Локализованный | 82% |
Региональный | 67% |
Дальний | 39% |
Все этапы SEER вместе | 62% |
Что такое числа
- Эти цифры относятся только к стадии рака, когда он впервые диагностирован. Они не применяются позже, если рак растет, распространяется или возвращается после лечения.
- Эти цифры учитывают не все. Показатели выживаемости сгруппированы в зависимости от того, насколько далеко распространился рак. Но другие факторы, такие как перечисленные ниже, также могут повлиять на мировоззрение человека.
- Люди, у которых сейчас диагностирована опухоль Юинга, могут иметь лучшее прогнозирование, чем показывают эти цифры. Лечение со временем улучшается, и эти цифры основаны на людях, которым был поставлен диагноз и лечили не менее 5 лет назад.
Другие факторы, которые могут повлиять на прогноз (прогноз)
Факторы, отличные от стадии рака, также могут влиять на выживаемость. Факторы, которые были связаны с лучшим прогнозом, включают:
- Меньший размер опухоли
- Основная опухоль находится на руке или ноге (в отличие от грудной клетки или таза)
- Уровень ЛДГ в крови нормальный
- Хороший ответ опухоли на химиотерапию
- Возраст младше 10 лет
Даже с учетом этих других факторов выживаемость в лучшем случае является приблизительной оценкой.Ваша команда по лечению рака — ваш лучший источник информации по этой теме.
* SEER = эпиднадзор, эпидемиология и конечные результаты
Саркома Юинга — Детство и юность: Статистика
НА ЭТОЙ СТРАНИЦЕ: Вы найдете информацию о количестве детей и подростков, у которых ежегодно диагностируется саркома Юинга. Вы также прочтете общую информацию о том, как пережить болезнь. Помните, что выживаемость зависит от нескольких факторов. Используйте меню для просмотра других страниц.
Каждый год около 200 детей и подростков в США диагностируют опухоль Юинга (саркома). Опухоли Юинга составляют 1% всех онкологических заболеваний у детей и подростков в возрасте до 15 лет и 2% всех онкологических заболеваний у подростков в возрасте от 15 до 19 лет. Около половины всех диагнозов саркомы Юинга приходится на людей в возрасте от 10 до 20 лет. также влияют на детей младшего возраста и молодых людей в возрасте от 20 до 30 лет. Почти все случаи саркомы Юинга встречаются у белых людей.
Пятилетняя выживаемость показывает, какой процент детей и подростков живут не менее 5 лет после обнаружения рака.Процент означает количество из 100. 5-летняя выживаемость при этом типе рака составляет 75% для детей младше 15 лет и 58% для подростков в возрасте от 15 до 19 лет.
Выживаемость также зависит от других факторов, в том числе от того, насколько далеко распространилась опухоль. Общая 5-летняя выживаемость людей с опухолью Юинга составляет 62%. Если опухоль обнаруживается только в том месте, где она возникла (так называемая локализованная), 5-летняя выживаемость составляет 82%. Если он распространился на близлежащий регион (называемый региональным), 5-летняя выживаемость составляет 67%.Если опухоль распространилась на отдаленные области на момент постановки диагноза (так называемый метастаз), 5-летняя выживаемость составляет 39%.
Существуют и другие факторы, связанные с более высокой выживаемостью при опухолях Юинга на всех стадиях. Эти факторы включают возраст младше 10 лет, опухоль меньшего размера, опухоль, расположенную в руке или ноге, и нормальный уровень фермента лактатдегидрогеназы (ЛДГ) в крови. Выживаемость также может быть выше в зависимости от того, эффективно ли химиотерапия лечит рак.
Важно помнить, что статистические данные о выживаемости детей и подростков с саркомой Юинга являются приблизительными. Оценка основана на ежегодных данных, основанных на количестве детей и подростков с этим раком в Соединенных Штатах. Также каждые 5 лет специалисты измеряют статистику выживаемости. Таким образом, оценка может не отражать результаты более точной диагностики или лечения, доступного менее чем за 5 лет. Если у вас есть какие-либо вопросы по поводу этой информации, обратитесь к лечащему врачу вашего ребенка.Узнайте больше о , понимая статистику .
Статистика адаптирована из публикации Американского онкологического общества (ACS), Cancer Facts & Figures 2021, и веб-сайтов ACS и детской исследовательской больницы Сент-Джуда. Дополнительным источником был Seigel R, et al. .: Cancer Statistics 2021. CA: A Cancer Journal для клиницистов. 2021 Янв; 71 (1): 7–33. doi / full / 10.3322 / caac.21654 (источники по состоянию на январь 2021 г.).
Следующий раздел в этом руководстве — Медицинские иллюстрации . Он предлагает рисунки частей тела, часто пораженных саркомой Юинга. Используйте меню, чтобы выбрать другой раздел для чтения в этом руководстве.
Факторы риска метастазирования и плохой прогноз саркомы Юинга: популяционное исследование | Журнал ортопедической хирургии и исследований
Клинические данные и критерии отбора
Мы использовали данные SEER, которые содержат эпидемиологическую информацию 18 онкологических регистров в США.SEER * Stat (версия 8.3.5) производится программой надзорных исследований Отдела контроля рака и популяционных наук Национального института рака для извлечения данных из базы данных SEER. В программном обеспечении мы выбрали базу данных под названием «Заболеваемость = SEER 18 Regs Custom Data (с дополнительными полями лечения), ноябрь 2017 г. (с вариациями 1973–2015 гг.)», Которая содержала информацию о лечении пациентов с ES, включая лучевую терапию и химиотерапию.
Критерии включения: (1) пациенты с диагнозом опухоль Юинга костей и суставов в соответствии с перекодировкой сайта Site and Morphology AYA / WHO2008; (2) пациенты, которым был поставлен диагноз между 1983 и 2015 годами, поскольку клинико-патологические данные до 1983 года были в основном неполными, а некоторые переменные, такие как размер опухоли, не были ясными; (3) ЭС костей и суставов была первой и единственной первичной злокачественной опухолью; (4) полные клинические данные, включая возраст на момент постановки диагноза, пол, расу, первичную локализацию, размер опухоли, степень распространения опухоли, состояние отдаленных метастазов, хирургическое вмешательство, направленное против рака, а также проведенные или невыполненные методы лечения (лучевая и химиотерапия); (5) диагноз был получен от живого пациента — не свидетельство о вскрытии или смерти; (6) полные данные наблюдения и известное время наблюдения; и (7) известная причина смерти и время выживания после постановки диагноза.
Критериями исключения были (1) ES других внекостных участков или мягких тканей, кроме костей, таких как брюшная полость и полость таза; (2) гистологически классифицируется как pNET и саркома Аскина; (3) пациенты имели другие сопутствующие злокачественные опухоли или саркома Юинга не была первой злокачественной опухолью; и (4) неполные клинико-патологические данные и данные о выживаемости.
Факторы риска метастазирования
Мы исследовали факторы риска отдаленных метастазов при диагностике пациентов с ЭС.Состояние метастазов отражалось в переменной степени опухоли. Распространенность опухоли была разделена на три категории: локализованная (ограниченная надкостницей), региональная (простирающаяся за пределы надкостницы до окружающей ткани, но без отдаленных метастазов) и метастатическая (с отдаленными метастазами при постановке диагноза). Локализованные и регионарные были классифицированы в неметастатическую группу, а метастатические — в метастатическую группу.
Мы выбрали пять клинико-патологических переменных в качестве альтернативных факторов риска: возраст (возраст на момент постановки диагноза), пол, раса, первичный очаг и размер опухоли.Возраст был разделен на пять групп: младше 10 лет, от 11 до 20 лет, от 21 до 30 лет, от 31 до 49 лет и старше 50 лет. Пол включал мужчин и женщин, а раса включала белых, черных и других (коренные американцы / коренные жители Аляски, выходцы из Азии / островов Тихого океана). Первичные участки были разделены на пять групп: конечности (включая длинные и короткие кости верхних и нижних конечностей), черепные, позвоночные, грудные и тазовые. Размер опухоли был разделен на три группы: <5 см, 5–8 см и> 8 см.Для выбора переменных в качестве возможных факторов риска, связанных с метастазированием при постановке диагноза, использовалась одномерная логистическая регрессия, и p <0,05 считалось статистически значимым. Затем была применена многомерная логистическая регрессия для определения факторов риска, выбранных в рамках одномерной регрессии.
Кривая ROC (кривая рабочих характеристик приемника) показала мощность прогнозирования каждого фактора риска и пятифакторной комбинированной модели, а также было указано значение AUC (площадь под кривой).Чем выше AUC, тем выше предсказательная сила.
Кроме того, мы также показали дополнительную информацию о лечении, в том числе о хирургии рака, лучевой терапии и химиотерапии. Вместе с пятью альтернативными факторами риска использовался критерий хи-квадрат для сравнения различий этих клинико-патологических факторов между неметастатическими и метастатическими группами.
Прогностический анализ
Общая выживаемость (ОС) представляла интерес. ОС была определена как время с момента установления диагноза смерти от всех возможных причин.Данные о пациентах, которые были живы на момент последнего наблюдения, считались цензурированными. Мы также рассматривали выживаемость, специфичную для рака (CSS), как другую интересующую конечную точку и определили ее как время от постановки диагноза до смерти от рака. Пациенты, которые были живы или умерли по другим причинам, кроме ES, на момент последнего наблюдения считались цензурированными данными.
В прогностическом анализе кривые выживаемости для каждой переменной оценивались методом Каплана-Мейера, а значимость различий между кривыми выживаемости определялась с помощью лог-рангового критерия.Мы также использовали регрессию Кокса для анализа выживаемости. Для выбора переменных в качестве возможных факторов риска, связанных с ОС и CSS, использовалась одномерная регрессия Кокса. Затем была применена многомерная регрессия Кокса для определения факторов риска для ОС и CSS, выбранных в однофакторной регрессии Кокса.
Разработка и проверка номограммы
Мы стремились построить номограмму для прогнозирования вероятности OS и CSS у пациентов с ES. Все пациенты были случайным образом распределены по обучающей выборке и валидации в соотношении 1: 1.Номограмма построена по данным обучающей выборки. Внутренняя проверка (обучающий набор) и внешняя проверка (проверочный набор) проводились с 1000 повторных выборок начальной загрузки для предотвращения переобучения. Прогностическая сила номограммы оценивалась с помощью индекса соответствия Харрелла (C-index). Значение C-индекса должно находиться в диапазоне от 0,5 до 1,0, 0,5 указывает на случайную вероятность, а 1,0 указывает на идеально скорректированную дискриминацию. Мы также использовали калибровочные графики для сравнения результатов прогнозирования номограмм с фактическими наблюдаемыми результатами выживаемости как внутри, так и за пределами группы.
Статистический анализ
Факторы риска метастазирования
Одномерная логистическая регрессия использовалась для выбора переменных в качестве возможных факторов риска, связанных с метастазированием при постановке диагноза. Затем была применена многомерная логистическая регрессия для определения факторов риска, выбранных в рамках одномерной регрессии. Кривая ROC (кривая рабочих характеристик приемника) показала мощность прогнозирования каждого фактора риска и пятифакторной комбинированной модели, а также было указано значение AUC (площадь под кривой).Критерий хи-квадрат использовался для сравнения различий этих клинико-патологических факторов между неметастатическими и метастатическими группами. Тест хи-квадрат, а также одномерная и многомерная логистическая регрессия выполнялись с помощью SPSS версии 23.0 (IBM Corporation), и p <0,05 считалось статистически значимым.
Анализ выживаемости
Кривые выживаемости для каждой переменной оценивались методом Каплана-Мейера, а значимость различий между кривыми выживаемости определялась с помощью лог-рангового критерия.Для выбора переменных в качестве возможных факторов риска, связанных с ОС и CSS, использовалась одномерная регрессия Кокса. Затем была применена многомерная регрессия Кокса для определения факторов риска для ОС и CSS, выбранных в однофакторной регрессии Кокса. Лог-ранговый тест и регрессия Кокса также были выполнены в SPSS версии 23.0 (IBM Corporation). Все значения p были двусторонними, и мы предположили, что вероятность менее 0,05 была статистически значимой.
Разработка и проверка номограммы
Разработка и проверка номограммы были выполнены с помощью R версии 3.5.1 (http://www.r-project.org/) с пакетами rms [13] и cmprsk [14].
Факторы прогноза выживаемости при саркоме Юинга: систематический обзор
Основные моменты
- •
Систематический обзор факторов прогноза выживаемости при саркоме Юинга.
- •
Степень заболевания, размер опухоли, расположение опухоли и гистологический ответ тесно связаны с выживаемостью.
- •
Понимание влияния хирургических полей и местных методов лечения требует дальнейших исследований.
- •
Упомянутые факторы риска полезны для разработки прогностических моделей и дизайна клинических исследований.
Abstract
Разработка прогностической модели выживаемости может помочь в стратификации лечения в соответствии с индивидуальным риском пациента, что приводит к стратегиям адаптивного лечения с учетом риска и реакции, которые позволяют принимать решения на раннем этапе. Цель этого систематического обзора — предоставить обзор прогностических факторов общей выживаемости (OS) и бессобытийной выживаемости (EFS) при саркоме Юинга, которые будут использоваться при разработке моделей прогнозирования и дизайна клинических испытаний.Литературный поиск был выполнен с использованием баз данных Pubmed, Embase, Web of Science, Academic search premier и Cochrane. Исследования соответствовали критериям отбора, если: 1) размер выборки ≥100; 2) Наблюдение ≥2 лет или смерть в течение 2 лет; 3) Набор после 1975 года; 4) Измерение результата OS или EFS; 5) многомерный анализ для оценки влияния прогностических факторов на исходы выживаемости; 6) Исследование опубликовано на английском языке. В случае, если тематические исследования были взяты из одной и той же базы данных, был выбран наиболее всеобъемлющий. Отбор исследований и оценка качества проводились двумя рецензентами независимо.Для каждого фактора риска был проведен синтез доказательств. Каппа-статистика использовалась для определения согласия между наблюдателями. Всего было найдено 149 полнотекстовых статей, 21 из которых может быть добавлена. Было исследовано 24 прогностических фактора, 14 из которых имеют отношение к данному обзору. Прогностические факторы, связанные с выживаемостью, включают метастазы на момент постановки диагноза, большие опухоли (объем ≥200 мл или наибольший диаметр ≥8 см), первичные опухоли, расположенные в осевом скелете, особенно в области таза, и гистологический ответ менее 100%.Эти факторы следует включить в качестве факторов риска при разработке моделей прогнозирования ЧС.
Ключевые слова
Саркома Юинга
Факторы прогноза
Выживание
Модели прогнозов
Персонализированная медицина
Прогноз
Рекомендуемые статьиЦитирующие статьи (0)
Просмотр аннотации© 2018 Авторы. Опубликовано Elsevier Ltd.
Рекомендуемые статьи
Цитирующие статьи
Простой в использовании клинический инструмент для оценки выживаемости при саркоме Юинга при постановке диагноза и после операции
Флетчер, К. Д. М., Бридж, Дж. А., Хогендорн, П. К. У., Мертенс, Ф. Классификация опухолей мягких тканей и костей ВОЗ . 4-е издание edn, (IARC, 2013).
Ladenstein, R. et al. . Первичная диссеминированная мультифокальная саркома Юинга: результаты исследования Euro-EWING 99. J Clin Oncol 28 , 3284–3291, https://doi.org/10.1200/JCO.2009.22.9864 (2010).
CAS Статья Google Scholar
Haeusler, J. et al. . Значение местного лечения пациентов с первичной диссеминированной мультифокальной саркомой Юинга (PDMES). Рак 116 , 443–450, https://doi.org/10.1002/cncr.24740 (2010).
Артикул PubMed PubMed Central Google Scholar
Grunewald, T. G. P. et al. . Саркома Юинга. Nat Rev Dis Primers 4 , 5, https://doi.org/10.1038 / s41572-018-0003-х (2018).
Артикул Google Scholar
Паппо, А. С. и Дирксен, У. Рабдомиосаркома, саркома Юинга и другие саркомы круглых клеток. J Clin Oncol 36 , 168–179, https://doi.org/10.1200/JCO.2017.74.7402 (2018).
CAS Статья PubMed PubMed Central Google Scholar
Шталь, М. и др. .Риск рецидива и выживаемость после рецидива у пациентов с саркомой Юинга. Детский рак крови 57 , 549–553, https://doi.org/10.1002/pbc.23040 (2011).
Артикул PubMed PubMed Central Google Scholar
Баркер, Л. М., Пендерграсс, Т. У., Сандерс, Дж. Э. и Хокинс, Д. С. Выживание после рецидива опухолей семейства сарком Юинга. J Clin Oncol 23 , 4354–4362, https: // doi.org / 10.1200 / JCO.2005.05.105 (2005).
Артикул PubMed PubMed Central Google Scholar
Родригес-Галиндо, К. и др. . Анализ прогностических факторов в семействе опухолей саркомы Юинга: обзор исследований Детской исследовательской больницы Св. Иуды. Рак 110 , 375–384, https://doi.org/10.1002/cncr.22821 (2007).
Артикул PubMed PubMed Central Google Scholar
Баччи, Г. и др. . Терапия и выживаемость после рецидива опухолей Юинга: опыт Риццоли у 195 пациентов, получавших адъювантную и неоадъювантную химиотерапию с 1979 по 1997 год. Ann Oncol 14 , 1654–1659 (2003).
CAS Статья Google Scholar
Cheon, S. et al. . Точность прогнозов клиницистов о выживаемости при запущенном раке: обзор. Ann Palliat Med 5 , 22–29, https: // doi.org / 10.3978 / j.issn.2224-5820.2015.08.04 (2016).
ADS Статья Google Scholar
Бисвас Б. и др. . Разработка прогностической модели для локализованного семейства опухолей саркомы Юинга: единый институциональный опыт с 224 случаями лечения с использованием единого протокола химиотерапии. J Surg Oncol 111 , 683–689, https://doi.org/10.1002/jso.23861 (2015).
Артикул Google Scholar
Карски, Э. Э. и др. . Идентификация дискретных прогностических групп при саркоме Юинга. Детский рак крови 63 , 47–53, https://doi.org/10.1002/pbc.25709 (2016).
CAS Статья Google Scholar
Мунс, К. Г., Альтман, Д. Г., Вергуве, Ю. и Ройстон, П. Прогноз и прогностические исследования: применение и влияние прогностических моделей в клинической практике. BMJ 338 , b606, https: // doi.org / 10.1136 / bmj.b606 (2009 г.).
Артикул Google Scholar
Альтман Д. Г., Вергуве Й., Ройстон П. и Мунс К. Г. Прогноз и прогностические исследования: проверка прогностической модели. BMJ 338 , b605, https://doi.org/10.1136/bmj.b605 (2009).
Артикул Google Scholar
Ройстон, П., Мунс, К. Г., Альтман, Д. Г., Вергуве, Ю.Прогноз и прогностические исследования: разработка прогностической модели. BMJ 338 , b604, https://doi.org/10.1136/bmj.b604 (2009).
Артикул Google Scholar
Мунс, К. Г., Ройстон, П., Вергуве, Ю., Гробби, Д. Э. и Альтман, Д. Г. Прогноз и прогностические исследования: что, почему и как? BMJ 338 , b375, https://doi.org/10.1136/bmj.b375 (2009).
Артикул Google Scholar
Steyerberg, E. W. & Vergouwe, Y. На пути к лучшим моделям клинического прогнозирования: семь шагов для разработки и ABCD для проверки. Eur Heart J 35 , 1925–1931, https://doi.org/10.1093/eurheartj/ehu207 (2014).
Артикул PubMed PubMed Central Google Scholar
Босма, С. Э., Аю, О., Фиокко, М., Гелдерблом, Х. и Дейкстра, П. Д. С. Прогностические факторы выживаемости при саркоме Юинга: систематический обзор. Хирургическая онкология 27 , 603–610 (2018).
CAS Статья Google Scholar
Саймон, Р. М., Субраманиан, Дж., Ли, М. К. и Менезес, С. Использование перекрестной проверки для оценки точности прогнозирования классификаторов риска выживания на основе многомерных данных. Brief Bioinform 12 , 203–214, https://doi.org/10.1093/bib/bbr001 (2011).
Артикул PubMed PubMed Central Google Scholar
Харрелл Ф. Э. младший, Ли К. Л. и Марк Д. Б. Многовариантные прогностические модели: вопросы разработки моделей, оценки допущений и адекватности, а также измерения и уменьшения ошибок. Stat Med 15 , 361–387, DOI: 10.1002 / (SICI) 1097-0258 (19960229) 15: 4 <361 :: AID-SIM168> 3.0.CO; 2-4 (1996).
Шемпер, М. и Смит, Т. Л. Примечание о количественной оценке последующих действий при изучении времени отказа. Контрольные клинические испытания 17 , 343–346 (1996).
CAS Статья Google Scholar
Ли, Дж., Хоанг, Б. Х., Зиогас, А. и Зелл, Дж. А. Анализ прогностических факторов при саркоме Юинга с использованием популяционного ракового регистра. Рак 116 , 1964–1973, https://doi.org/10.1002/cncr.24937 (2010).
Артикул Google Scholar
Дачман, К. Р., Гао, Ю. и Миллер, Б.J. Прогностические факторы выживаемости пациентов с саркомой Юинга с использованием базы данных программы эпиднадзора, эпидемиологии и конечных результатов (SEER). Эпидемиол рака 39 , 189–195, https://doi.org/10.1016/j.canep.2014.12.012 (2015).
Артикул Google Scholar
Джавад М. У. и др. . Саркома Юинга демонстрирует расовые различия в результатах, связанных с заболеваемостью и полом: анализ 1631 случая из базы данных SEER, 1973–2005 гг. Рак 115 , 3526–3536, https://doi.org/10.1002/cncr.24388[doi] (2009).
Артикул Google Scholar
Такенака, С. и др. . Результаты лечения японских пациентов с саркомой Юинга: различия между скелетной и внескелетной саркомой Юинга. Японский журнал клинической онкологии 46 , 522–528, https://doi.org/10.1093/jjco/hyw032 (2016).
Артикул Google Scholar
Cotterill, S.J. и др. . Факторы прогноза при опухоли кости Юинга: анализ 975 пациентов из Европейской межгрупповой совместной группы по изучению саркомы Юинга. J Clin Oncol 18 , 3108–3114, https://doi.org/10.1200/JCO.2000.18.17.3108 (2000).
CAS Статья PubMed PubMed Central Google Scholar
Физази, К. и др. . Семейство опухолей Юинга у взрослых: многомерный анализ выживаемости и отдаленных результатов комбинированной терапии у 182 пациентов. J Clin Oncol 16 , 3736–3743, https://doi.org/10.1200/JCO.1998.16.12.3736 (1998).
CAS Статья PubMed PubMed Central Google Scholar
Альберго, Дж. И. и др. . Саркома Юинга: только пациенты со 100% некрозом после химиотерапии должны быть классифицированы как имеющие хороший ответ. Костный сустав J 98-B , 1138–1144, https://doi.org/10.1302/0301-620X.98B8.37346 (2016).
CAS Статья PubMed PubMed Central Google Scholar
Верма, В., Деннистон, К. А., Лин, К. Дж. И Лин, К. Сравнение педиатрических и взрослых пациентов с опухолями семейства сарком Юинга. Front Oncol 7 , 82, https://doi.org/10.3389/fonc.2017.00082 (2017).
Артикул PubMed PubMed Central Google Scholar
Миллер, Б. Дж., Гао, Ю. Б. и Дачман, К. Р. Обеспечивают ли хирургическое вмешательство или лучевая терапия наилучшую общую выживаемость при саркоме Юинга? Обзор Национальной базы данных по раку. Журнал хирургической онкологии 116 , 384–390 (2017).
Артикул Google Scholar
Протокол: Euro Ewing 99. Европейская рабочая инициатива национальных групп по опухолям Юинга, Исследования опухолей Юинга 1999 / EE99. (Евро Юинг 99, 2006 г.).
Bacci, G. et al. . Роль хирургии в местном лечении саркомы Юинга конечностей у пациентов, получающих адъювантную и неоадъювантную химиотерапию. Oncol Rep 11 , 111–120 (2004).
Google Scholar
Gaspar, N. et al. . Химиотерапия с учетом риска локализованной саркомы кости Юинга: французское исследование EW93. Eur J Cancer 48 , 1376–1385, https: // doi.org / 10.1016 / j.ejca.2012.03.017 (2012).
Артикул Google Scholar
Foulon, S. et al. . Можно ли отказаться от послеоперационной лучевой терапии при локальной саркоме Юинга стандартного риска? Наблюдательное исследование группы Euro-E.W.I.N.G. Eur J Cancer 61 , 128–136, https://doi.org/10.1016/j.ejca.2016.03.075 (2016).
Артикул Google Scholar
Дженкин, Р. Д. и др. . Локализованная саркома Юинга / PNET костно-прогностических факторов и сравнение международных данных. Med Pediatr Oncol 39 , 586–593, https://doi.org/10.1002/mpo.10212 (2002).
Артикул Google Scholar
Оберлин, О. и др. . Факторы прогноза при локализованных опухолях Юинга и периферических нейроэктодермальных опухолях: третье исследование Французского общества детской онкологии (исследование EW88). Br J Cancer 85 , 1646–1654, https://doi.org/10.1054/bjoc.2001.2150 (2001).
CAS Статья PubMed PubMed Central Google Scholar
Li, Y. J. et al. . Клинические значения шести воспалительных биомаркеров как прогностических индикаторов саркомы Юинга. Cancer Manag Res 9 , 443–451, https://doi.org/10.2147/CMAR.S146827 (2017).
CAS Статья PubMed PubMed Central Google Scholar
Саркома Юинга Рак кости | Дети с раком Великобритания
Победа Бетана над саркомой Юинга
Прочтите историю Бетан, рассказанную ее мамой Линн:
«В октябре 2011 года Бетан жаловалась на боль, но не имела никаких признаков синяков.У нее была очень высокая температура, которую я не мог контролировать, и странная сыпь по всему телу. Она поправлялась медленно, но это было необычно для Бетан, поскольку она никогда не чувствовала себя плохо.
Вскоре после этого мы обнаружили шишку на верхней части левой руки Бетан — она появилась почти в одночасье. Ничего подобного не видела, пошли к врачу.
Нам сделали рентген в больнице — он спас ей жизнь. Когда врачи поставили клинический диагноз саркомы Юинга, это стало переломным моментом. Я не мог в это поверить, я просто хотел забрать Бетан домой.Ей понадобился месяц интенсивных сканирований и тестов. После биопсии хирург поговорил с нами, он был уверен, что это саркома Юинга.
Началась химиотерапия. Бетан была на четырех капельницах сразу — ей было очень плохо, кормили через зонд и просто ужасно. Предполагалось, что она будет дома в течение двух недель между циклами, но из этого ничего не вышло — она вернется домой, у нее упадет уровень крови, и ей нужно будет вернуться в больницу для переливания крови. Она была дома максимум три-четыре дня, мы в основном жили в больнице.
В июле 2012 года Вифан потребовалась операция по спасению жизни. Консультант дал нам список вариантов лечения на выбор. Мы были обеспокоены тем, что Бетан потеряет руку, но мы выбрали вариант, чтобы дать ей наилучшие шансы на выживание. Они удалили Бетан плечо, плечевую и локтевую кости, облучили и вернули обратно. Она пролежала на операционном столе восемь часов. У нее остались очень хрупкие кости, поскольку они теперь мертвы, поэтому она не чувствует руки. Но, к счастью, саркома Юинга была удалена на 100%.
В сентябре 2012 года Бетан начала еще восемь курсов химиотерапии, и ей было немного легче переносить. Она не так часто лежала в больнице, но ей по-прежнему регулярно требовалась кровь. За это время мы смогли насладиться Бетан, пока ее кровь была хорошей и немного потухла!
Три месяца спустя Бетан прошла последний курс химиотерапии, что за день!
Бетан уже пять лет не принимает химиотерапию и находится в стадии ремиссии ».
Если вас тронуло путешествие Бетан, помогите нам инвестировать в высококачественные исследования, которые в противном случае остались бы без финансирования, помогая поддерживать детей, больных раком, чтобы они могли дольше оставаться со своими семьями.
Пожертвовать сейчас Сбор средств
Вернуться к началуСаркома Юинга — NHS
Саркома Юинга — редкий тип рака, поражающий кости или ткани вокруг костей.
В основном поражает детей и молодежь, но также встречается у взрослых. Это чаще встречается у мужчин, чем у женщин.
Информация:Консультации по коронавирусу
Получите консультацию о коронавирусе и раке:
Симптомы саркомы Юинга
Симптомы включают:
- Боль в костях — она может усиливаться со временем и может усиливаться ночью
- болезненное уплотнение или припухлость
- высокая температура, которая не проходит
- чувство усталости все время
- непреднамеренная потеря веса
Пораженные кости также могут быть слабее и с большей вероятностью сломаться.Некоторым людям ставят диагноз после перелома.
Ноги (часто вокруг колена), таз, руки, ребра и позвоночник являются основными областями, пораженными саркомой Юинга.
Тесты на саркому Юинга
Саркому Юинга сложно диагностировать, потому что она встречается довольно редко и симптомы могут быть похожи на многие другие заболевания.
Для диагностики рака и определения его местонахождения в организме может потребоваться несколько тестов.
Эти тесты могут включать:
- рентгеновский снимок
- анализы крови
- МРТ, компьютерную томографию или ПЭТ сканирование
- сканирование костей — после инъекции слаборадиоактивного вещества, которое делает кости четко показать
- биопсию кости, из которой удален небольшой образец кости, чтобы его можно было проверить на наличие признаков рака и определенных генетических изменений, связанных с саркомой Юинга
Лечение саркомы Юинга
Лечение саркомы Юинга часто включает комбинацию:
- лучевой терапии — когда радиация используется для уничтожения раковых клеток
- химиотерапии — где лекарства используются для уничтожения раковых клеток
- хирургии по удалению рака
Поскольку саркома Юинга встречается редко, а лечение сложное, вы должны лечиться у команды специалистов.Они порекомендуют план лечения в зависимости от того, где находится рак и его размер.
Поговорите со своей группой медицинского обслуживания о том, почему они предложили план лечения, и попросите их рассказать о преимуществах и любых связанных с этим рисках. Вы также можете обсудить, какое лечение вам может понадобиться впоследствии.
Лучевая терапия
Лучевая терапия часто используется для лечения саркомы Юинга до и после операции, или ее можно использовать вместо операции, если рак невозможно удалить безопасно.
Химиотерапия
Большинство людей с саркомой Юинга проходят химиотерапию, чтобы уменьшить рак, а затем операцию, чтобы удалить как можно большую часть.За этим часто следует дальнейшая химиотерапия, чтобы убить оставшиеся раковые клетки.
Хирургия
Если саркома Юинга поражает ваши кости, вам потребуется операция в специализированном центре рака костей.
Существует 3 основных типа хирургического вмешательства при саркоме Юинга. Операция может быть использована для удаления:
- пораженной кости или ткани — это называется резекцией
- кусочка кости, содержащего рак, и замены его куском металла или костью, взятой из другой части тела — это называется хирургической операцией по сохранению конечностей
- вся или часть руки или ноги — это называется ампутацией
Если у вас ампутирована рука или нога, вам может потребоваться протез конечности и поддержка, чтобы помочь вам восстановить использование пораженной конечность.
Перспективы саркомы Юинга
Саркома Юинга может довольно быстро распространяться на другие части тела. Чем раньше диагноз поставлен, тем больше шансов на успех лечения.
Иногда это можно вылечить, но это может быть невозможно, если рак распространился.
Рак также может вернуться после лечения, поэтому вам будут предложены регулярные осмотры для выявления каких-либо признаков этого. Некоторым людям требуется лечение в течение многих лет.
Около 6 из 10 человек с саркомой Юинга живут не менее 5 лет после постановки диагноза. Но это может быть разным, и некоторые люди живут намного дольше.
Поговорите со своей бригадой по уходу о шансах на успех вашего лечения.
Дополнительная информация и поддержка
Если вам или вашему ребенку сообщат о раке, это может очень расстроить и утомить.
Помимо поддержки со стороны вашей группы по уходу, вам может быть полезно получить информацию и советы от благотворительных организаций и групп поддержки.
Основными организациями, занимающимися саркомой Юинга, являются:
Другие хорошие источники информации и поддержки в отношении рака:
Возможно, вам или вашему ребенку будет проведено клиническое испытание, для получения дополнительной информации обратитесь к врачу. Вы также можете узнать о клинических испытаниях саркомы Юинга в Клинических испытаниях Европейского Консорциума Юинга и Cancer Research UK.

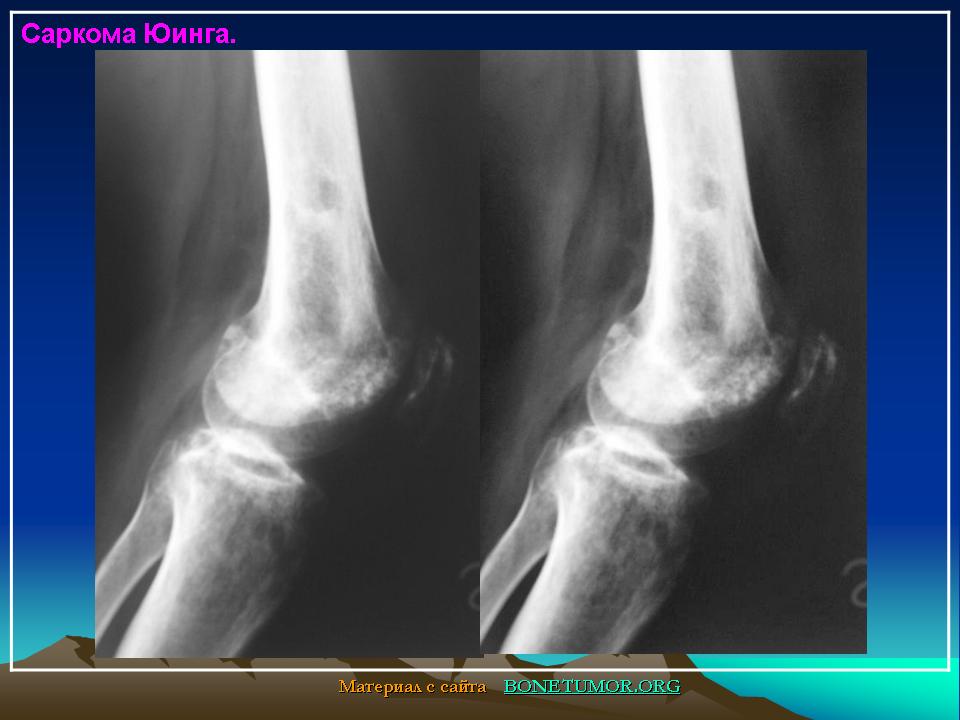 Если требуется открытая (инцизионная) биопсия, она должна быть тщательно спланирована и выполнена хирургом, который будет проводить тотальную резекцию.
Если требуется открытая (инцизионная) биопсия, она должна быть тщательно спланирована и выполнена хирургом, который будет проводить тотальную резекцию.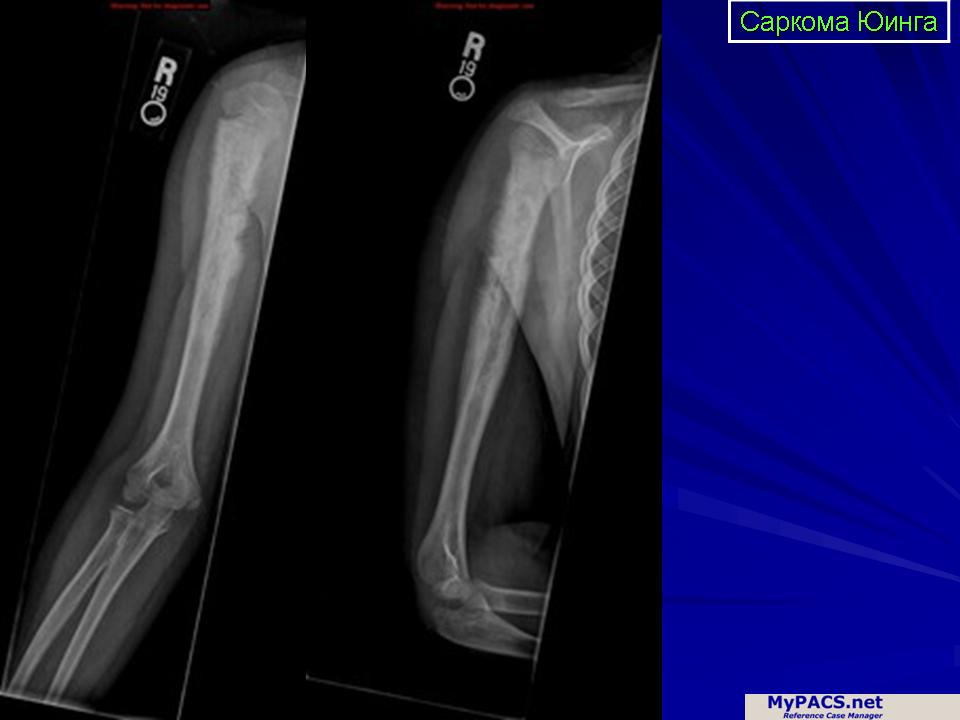 Встречается в малом тазу и в длинных трубчатых костях ног. У некоторых больных наблюдается температура.
Встречается в малом тазу и в длинных трубчатых костях ног. У некоторых больных наблюдается температура.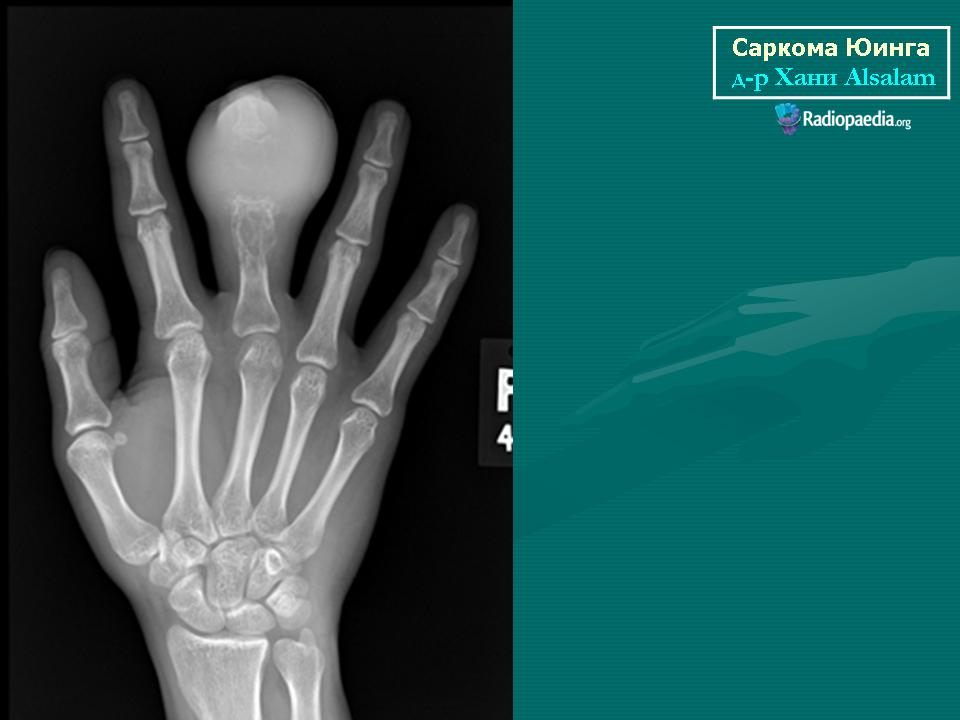 Обнаруживаются метастазы во внутренних органах, тканях, лимфатических узлах. Часто проблемы наблюдаются с легкими и лимфатической системой. При использовании различных методов визуализации изменения в скелете четко просматриваются. Для данной стадии характерна низкая выживаемость пациентов.
Обнаруживаются метастазы во внутренних органах, тканях, лимфатических узлах. Часто проблемы наблюдаются с легкими и лимфатической системой. При использовании различных методов визуализации изменения в скелете четко просматриваются. Для данной стадии характерна низкая выживаемость пациентов.