synlab: Вирусные гепатиты
Вирус гепатита В – ДНК содержащий вирус, имеющий несколько антигенов. Наиболее изученными антигенами являются:
- HBsAg – поверхностный антиген
- HbcAg – сердцевинный антиген
- HbeAg – антиген инфекционности.
Антигены вируса гепатита В, образующиеся к ним антитела и ДНК вируса являются маркерами инфекционного процесса, и различные сочетания этих маркёров характеризуют определённую стадию течения болезни.
Лабораторная диагностика вирусного гепатита В включает:
- Определение антигенов вируса гепатита В (HBsAg, HBеAg)
- Определение антител к антигенам вируса гепатита В (анти- HBsAg, анти- HBе, анти- HBс)
- Выявление ДНК вируса гепатита В (HBV-ДНК) – качественный и количественный анализ.
При остром гепатите В в типичных случаях принято выделять следующие периоды:
- Инкубационный (скрытый) – обычно от 60 до 120 дней.
- Начальный (преджелтушный) – от одного дня до 3-4 недель
- Период разгара (желтушный) — до 6-8 недель и более
- Реконвалисценция – от 2 до 12 месяцев.

При хроническом гепатите В были выявлены две биологические фазы:
- Ранняя репликативная
- Поздняя интегративная и следующие клинические варианты хронической инфекции:
- Хронический гепатит с различной степенью активности
- Носительство HBsAg
- Цирроз печени
- Гепатоцеллюлярная карцинома
Диагностическое значение маркеров вирусного гепатита В — в информационных папках для врачей Медицинской диагностической лаборатории «СИНЛАБ», отдел маркетинга — тел.: 378-58-55
Вирус гепатита С относится к семейству флавивирусов. Геном ВГС представлен одноцепочечной линейной РНК. Отличительной его способностью является генетическая неоднородность, обусловленная быстрой замещаемостью нуклеотидов. В результате изменчивости генома ВГС внутри одного генотипа образуется большое число мутантных, генетически отличающихся друг от друга вариантов вируса — “квазивидов” ВГС, которые циркулируют в организме хозяина. С наличием “квазивидов” связывают ускользание вируса от иммунного ответа, длительную персистенцию ВГС в организме человека и формирование хронического гепатита, а также устойчивость к интерферонотерапии.
Специфическими маркерами, подтверждающими наличие ОГС, являются антитела к ВГС (анти-HCV), которые обнаруживаются в ИФА современными тест-системами, начиная со 2—10-й недели болезни. Большое значение имеет определение РНК ВГС с помощью ПЦР в различных биологических субстратах (в сыворотке крови, лимфоцитах, ткани печени и др.) для определения активности репликативного процесса и оценки результатов интерферонотерапии.
Важным прогностическим маркером эффективности противовирусной терапии при инфекции вирусом гепатита С (HCV) является его генотип. Существует 6 генотипов и более 100 субтипов ВГС. Генотип HCV определяет дозу препарата и продолжительность курса лечения, что актуально, учитывая широкий спектр побочных действий и низкую переносимость интерферона в процессе терапии. Для генотипа 1 характерен крайне низкий ответ на проводимую терапию. Факторами, обусловливающими эффективность лечения, являются генотипы 2 или 3, низкая вирусная нагрузка и незначительные гистологические изменения при биопсии печени.
Диагностическое значение маркеров вирусного гепатита С — в информационных папках для врачей Медицинской диагностической лаборатории»СИНЛАБ», отдел маркетинга — тел.: (017) 378-58-55
KDL. Вирусные гепатиты. Анализы и цены
Алергология. ImmunoCAP. Индивидуальные аллергены, IgE
Аллергокомпоненты ImmunoCAP
Аллергокомпоненты деревьев
Аллергокомпоненты животных и птиц
Аллергокомпоненты плесени
Аллергокомпоненты трав
Пищевые аллергокомпоненты
Аллергология. ImmunoCAP. Комплексные исследования IgE (результат по каждому аллергену)
Аллергология. ImmunoCAP. Панели аллергенов IgE, скрининг (результат СУММАРНЫЙ)
Аллергология. ImmunoCAP. Фадиатоп
Аллергология.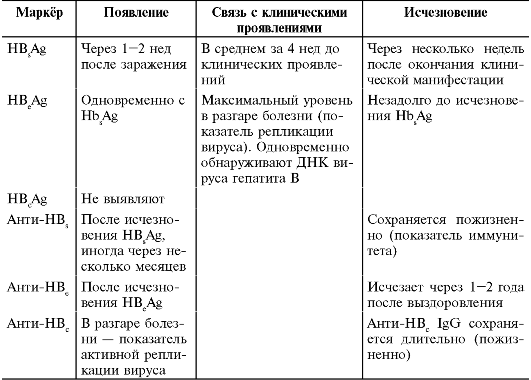 Immulite. Индивидуальные аллергены
Immulite. Индивидуальные аллергены
Аллергены гельминтов, IgE
Аллергены грибов (кандида и плесневых), IgE
Аллергены деревьев, IgE
Аллергены животных и птиц, IgE
Аллергены клещей домашней пыли, IgE
Аллергены лекарств и химических веществ, IgE
Аллергены насекомых, IgE
Аллергены пыли, IgE
Аллергены ткани, IgE
Аллергены трав, IgE
Бактериальные аллегены (стафилококк), IgE
Пищевые аллергены, IgE
Пищевые аллергены, IgG
Аллергология. Immulite. Комплексы аллергенов, IgE (результат по каждому аллргену)
Аллергология. Immulite. Панели аллергенов, скрининг (результат СУММАРНЫЙ)
Аллергены деревьев, IgE (панель)
Аллергены животных и птиц, IgE (панель)
Аллергены трав, IgE (панель)
Ингаляционные аллергены, IgE (панель)
Пищевые аллергены, IgE (панель)
Аллергология. Immulite. Панели пищевых аллергенов IgG (результат СУММАРНЫЙ)
Аллергология. ImmunoCAP. Индивидуальные аллергены, IgE
Аллергены деревьев, IgE
Аллергены животных и птиц, IgE
Аллергены пыли, IgE
Аллергены трав, IgE
Пищевые аллергены, IgE
Аллергология.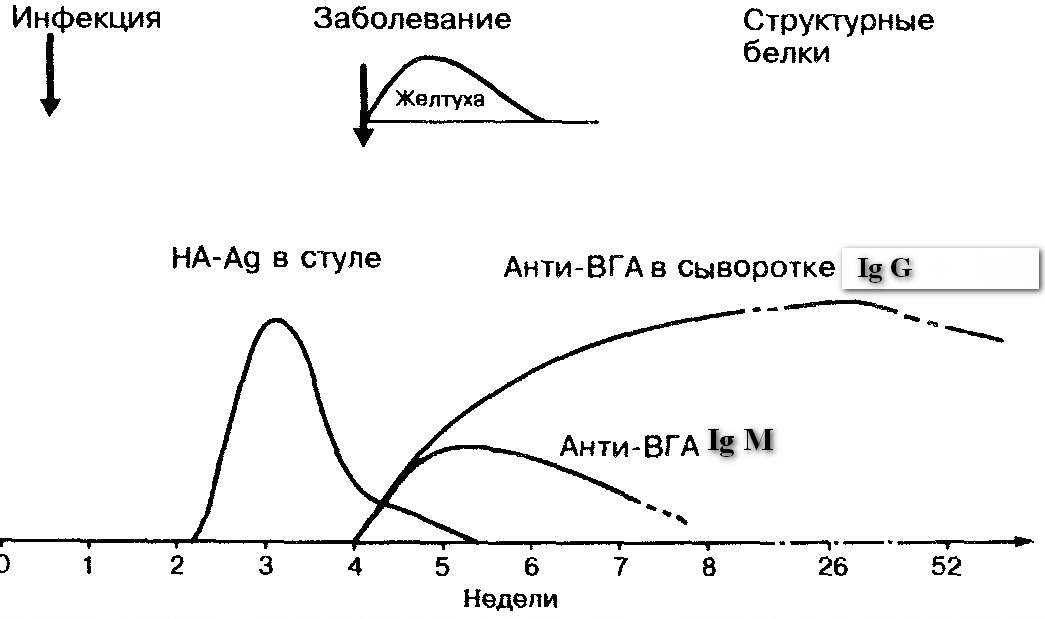
Аллергология. RIDA. Комплексы аллергенов, IgE (результат по каждому аллргену)
Аллергология. Местные анестетики, IgE
Биохимические исследования крови
Диагностика анемий
Липидный обмен
Обмен белков
Обмен пигментов
Обмен углеводов
Специфические белки
Ферменты
Электролиты и микроэлементы
Биохимические исследования мочи
Разовая порция мочи
Суточная порция мочи
Витамины, аминокислоты, жирные кислоты
Гематология
Гемостаз (коагулограмма)
Генетические исследования
HLA-типирование
Исследование генетических полиморфизмов методом пиросеквенирования
Исследование генетических полиморфизмов методом ПЦР
Молекулярно-генетический анализ мужского бесплодия
Гистологические исследования
Гистологические исследования лаборатории UNIM
Гормоны биологических жидкостей
Гормоны гипофиза и гипофизарно-адреналовой системы
Гормоны крови
Гормоны гипофиза и гипофизарно-адреналовой системы
Маркеры остеопороза
Пренатальная диагностика
Ренин-альдостероновая система
Тесты репродукции
Функция органов пищеварения
Функция щитовидной железы
Гормоны мочи
Диагностика методом ПЦР
COVID-19
Андрофлор, иследование биоценоза (муж)
Вирус герпеса VI типа
Вирус Варицелла-Зостер (ветряной оспы)
Вирус герпеса VI типа
Вирус простого герпеса I, II типа
Вирус Эпштейна-Барр
Вирусы группы герпеса
Возбудитель туберкулеза
ВПЧ (вирус папилломы человека)
Грибы рода кандида
Листерии
Парвовирус
Респираторные инфекции
Стрептококки (вкл. S.agalactie)
S.agalactie)
Токсоплазма
Урогенитальные инфекции, ИППП
Урогенитальные инфекции, комплексные исследования
Урогенитальные инфекции, условные патогены
Фемофлор, исследование биоценоза (жен)
Флороценоз, иследование биоценоза (жен)
Цитомегаловирус
Диагностика методом ПЦР, кал
Кишечные инфекции
Диагностика методом ПЦР, клещ
Клещевые инфекции
Диагностика методом ПЦР, кровь.
Вирус Варицелла-Зостер (ветряной оспы)
Вирус герпеса VI типа
Вирус краснухи
Вирус простого герпеса I, II типа
Вирус Эпштейна-Барр
ВИЧ
Возбудитель туберкулеза
Гепатит D
Гепатит G
Гепатит А
Гепатит В
Гепатит С
Листерии
Парвовирус
Токсоплазма
Цитомегаловирус
Жидкостная цитология
Изосерология
Иммуногистохимические исследования
Иммунологические исследования
Иммунограмма (клеточный иммунитет)
Интерфероновый статус, базовое исследование
Интерфероновый статус, чувствительность к препаратам
Оценка гуморального иммунитета
Специальные иммунологические исследования
Исследование абортуса
Исследование мочевого камня
Исследование парапротеинов. Скрининг и иммунофиксация
Скрининг и иммунофиксация
Исследования слюны
Исследования слюны
Комплексные исследования
Лекарственный мониторинг
Маркеры аутоиммунных заболеваний
Антифосфолипидный синдром (АФС)
Аутоиммунные заболевания легких и сердца
Аутоиммунные неврологические заболевания
Аутоиммунные поражения ЖКТ и целиакия
Аутоиммунные поражения печени
Аутоиммунные поражения почек и васкулиты
Аутоиммунные эндокринопатии и бесплодие
Диагностика артритов
Пузырные дерматозы
Системные ревматические заболевания
Эли-тесты
Микробиологические исследования (посевы)
Посев крови на стерильность
Посев на гемофильную палочку
Посев на грибы (Candida)
Посев на грибы (возбудители микозов кожи и ногтей)
Посев на дифтерию
Посев на микоплазмы и уреаплазмы
Посев на пиогенный стрептококк
Посев на стафилококк
Посевы кала
Посевы мочи
Посевы на микрофлору (конъюнктива)
Посевы на микрофлору (отделяемое)
Посевы на микрофлору (урогенитальный тракт женщины)
Посевы на микрофлору (урогенитальный тракт мужчины)
Посевы на микрофлору ЛОР-органы)
Ускоренные посевы с расширенной антибиотикограммой
Неинвазивная диагностика болезней печени
Программы неинвазивной диагностики болезней печени
Неинвазивный пренатальный ДНК-тест (НИПТ)
Неинвазивный пренатальный тест (пол/резус плода)
Общеклинические исследования
Исследование назального секрета
Исследование секрета простаты
Исследования кала
Исследования мочи
Исследования эякулята
Микроскопическое исследование биологических жидкостей
Микроскопия на наличие патогенных грибов и паразитов
Микроскопия отделяемого урогенитального тракта
Онкогематология
Иммунофенотипирование при лимфопролиферативных заболеваниях
Миелограмма
Молекулярная диагностика миелопролиферативных заболеваний
Цитохимические исследования клеток крови и костного мозга
Онкогенетика
Онкомаркеры
Пищевая непереносимость, IgG4
Полногеномные исследования и панели наследственных заболеваний
Пренатальный скрининг
Серологические маркеры инфекций
Аденовирус
Бруцеллез
Вирус HTLV
Вирус Варицелла-Зостер (ветряной оспы)
Вирус герпеса VI типа
Вирус Коксаки
Вирус кори
Вирус краснухи
Вирус эпидемического паротита
Вирус Эпштейна-Барр
Вирусы простого герпеса I и II типа
ВИЧ
Гепатит D
Гепатит А
Гепатит В
Гепатит Е
Гепатит С
Грибковые инфекции
Дифтерия
Кишечные инфекции
Клещевые инфекции
Коклюш и паракоклюш
Коронавирус
Менингококк
Паразитарные инвазии
Парвовирус
Респираторные инфекции
Сифилис
Столбняк
Токсоплазма
Туберкулез
Урогенитальные инфекции
Хеликобактер
Цитомегаловирус
Специализированные лабораторные исследования.
Дыхательный тест
Микробиоценоз по Осипову
Тяжелые металлы и микроэлементы
Тяжелые металлы и микроэлементы в волосах
Тяжелые металлы и микроэлементы в крови
Тяжелые металлы и микроэлементы в моче
Услуги
Выезд на дом
ЭКГ
Установление родства
Химико-токсикологические исследования
Хромосомный микроматричный анализ
Цитогенетические исследования
Цитологические исследования
Чекап
Анализы в KDL. Диагностика гепатитов, скрининг
Комплекс лабораторных тестов «Диагностика гепатитов, скрининг» представлен маркерами вирусных гепатитов, которые можно выявить по анализу крови. Оценивается реакция иммунитета на попадание вирусов в организм, что позволяет врачу подтвердить или исключить инфекционную природу заболеваний печени. Используется в рамках дифференциальной диагностики гепатитов.
Что определяется в данном исследовании?
Маркеры вирусного гепатита А (ВГА, Болезнь Боткина).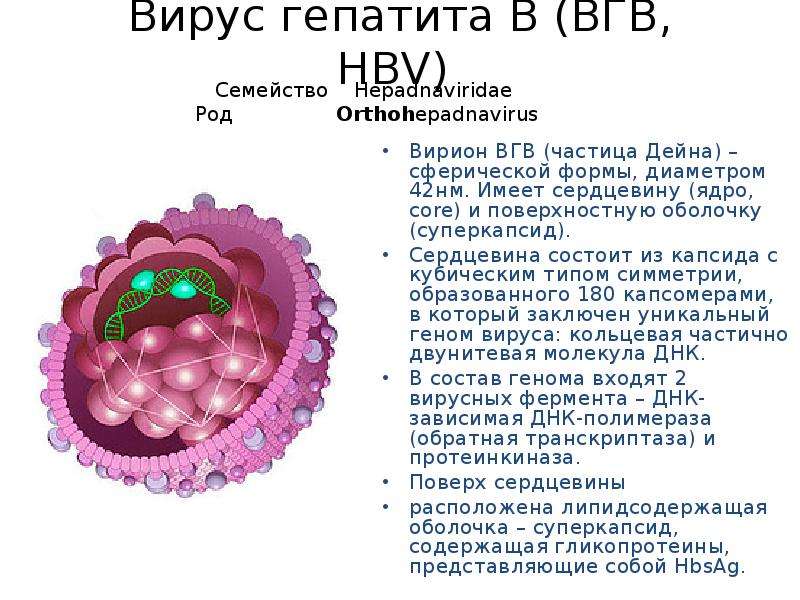 Для ВГА характерен фекально-оральный механизм передачи, заражение происходит через грязные руки, предметы обихода, пищевые продукты, воду. В большинстве случаев протекает без осложнений, выздоровление полное.
Для ВГА характерен фекально-оральный механизм передачи, заражение происходит через грязные руки, предметы обихода, пищевые продукты, воду. В большинстве случаев протекает без осложнений, выздоровление полное.
Маркеры вирусного гепатита В. Гепатит В передается через кровь, зараженные медицинские инструменты, половым путём, от матери к ребёнку. Клинические проявления разнообразные: от бессимптомного носительства до прогрессирующего поражения печени с последующим формированием цирроза или рака печени, может протекать в острой и хронической форме. Наиболее целесообразно определение антител через 6 недель от момента возможного заражения.
Маркеры вирусного гепатита С. ВГС известен как «ласковый убийца», чаще других гепатитов приводит к развитию цирроза и гепатоцеллюлярного рака.
В каких случаях назначают комплекс «Диагностика гепатитов, скрининг»
- Обследование пациентов с патологией печени для исключения вирусной природы гепатита
- Обследование контактных лиц с больными вирусным гепатитом
- Контакт беременной женщины с больными детьми
Что означают результаты теста?
В результате будет указано «обнаружено/не обнаружено» или цифровое значение с нормативными показателями.
При получении ответа «обнаружено» или превышении нормальных значений результат расценивается как положительный.
Обнаружение антител IgG к вирусному гепатиту А и антител к поверхностному антигену вируса гепатита В (Anti-HBs) при отсутствии других антител расценивается как перенесенное в прошлом заболевание или поствакцинальный иммунитет.
Во всех остальных случаях требуется дополнительная диагностика, назначаемая лечащим врачом.
Напоминаем, что интерпретацию результата проводит врач, сопоставляя данные анамнеза, осмотра, лабораторных и инструментальных методов.
Сроки выполнения теста.
Результат будет получен в течение 1-2 дней
Как подготовиться к анализу?
Кровь сдаётся утром натощак при соблюдении питьевого режима или через 3 часа после необильного приёма пищи. Специальная подготовка не нужна.
HBsAg, качественный тест (HBs-антиген, поверхностный антиген вируса гепатита B, «австралийский» антиген)
Исследуемый материал Сыворотка крови
Метод определения
Иммуноферментный анализ (ИФА).
Основной маркёр инфицирования вирусом гепатита В
Внимание. При положительных и сомнительных реакциях, срок выдачи результата может быть увеличен до 2-х рабочих дней.
HBsAg — поверхностный антиген вируса гепатита В, основной маркёр острого и хронического гепатита В — представляет собой белковую молекулу (липопротеин), ответственную за адсорбцию вируса на поверхности гепатоцитов (клеток печени). После встраивания вируса в геном печёночных клеток они начинают продуцировать вирусную ДНК и белки, и новые молекулы HBsAg поступают в кровь.
В большинстве случаев HBsAg обнаруживается уже в инкубационном периоде и при остром течении гепатита выявляется в крови в течение 5 — 6 месяцев. Обнаружение поверхностного антигена вируса гепатита В в крови дольше 6 месяцев после начала болезни свидетельствует о возможной хронизации процесса. Возможно пожизненное носительство HBsAg.
HBsAg способен активизировать клеточные протоонкогены. Через достаточно длительный срок (более 20 лет) возможно развитие гепатокарциномы.
Через достаточно длительный срок (более 20 лет) возможно развитие гепатокарциномы.
Особенности инфекции. Гепатит B (ВГВ, HВV) острое системное вирусное заболевание. Характеризуется поражением печени и различными внепечёночными проявлениями. Протекает остро или хронически, в желтушной (35%) или безжелтушной (65%) формах. Вирус гепатита В является ретровирусом семейства гепаднавирусов — Hepadnaviridae, содержит ДНК, чрезвычайно устойчив во внешней среде (к УФ-лучам, температуре, детергентам). Гепатит В передаётся с кровью и биологическими жидкостями парентеральным, трансплацентарным, половым и бытовым путями. Группу повышенного риска составляют лица, практикующие внутривенную наркоманию, беспорядочные половые связи, а также медицинские работники, пациенты, нуждающиеся в гемодиализе или переливаниях крови, заключённые, члены семей HBs-положительных лиц, новорождённые от HBs-положительных матерей.
Проникая в организм, вирус гепатита попадает в макрофаги крови и разносится по организму. Репликация вируса происходит в лимфатических узлах, костном мозге, фолликулах селезёнки, макрофагах, гепатоцитах. Повреждение печени обусловлено, в основном, за счёт иммунного лизиса; также вирус оказывает прямое цитопатическое действие. Сходство антигенов вируса с антигенами системы гистосовместимости человека обусловливает возникновение аутоиммунных («системных») реакций.
Репликация вируса происходит в лимфатических узлах, костном мозге, фолликулах селезёнки, макрофагах, гепатоцитах. Повреждение печени обусловлено, в основном, за счёт иммунного лизиса; также вирус оказывает прямое цитопатическое действие. Сходство антигенов вируса с антигенами системы гистосовместимости человека обусловливает возникновение аутоиммунных («системных») реакций.
Поверхностные (HBsAg) и сердцевинные (HBcAg) белки вируса являются антигенами, обусловливая выработку anti-HBs и anti-HBscore соответственно. Сердцевинный антиген, попадая в кровь, расщепляется на более устойчивые составные части, одна из которых HBe-Ag также несёт антигенные свойства. На неё и вырабатываются anti-HBe антитела. Генетическая изменчивость HВV способствует «ускользанию» вируса из-под иммунного ответа. С этим связаны трудности в лабораторной диагностике (серонегативный гепатит В), а также хронизация заболевания. Появление атипичных участков ДНК в геноме вируса приводит к фульминантному течению гепатита В.
Инкубационный период в среднем составляет 50 дней, но может растягиваться до 6 месяцев. В конце инкубационного периода повышаются уровни печёночных трансаминаз, увеличиваются печень и селезёнка. Возможно повышение концентрации билирубина до 2 — 2,5 нормальных значений, хотя это не приводит к потемнению мочи. Встречаются гриппоподобный, артралгический, диспептический или смешанный варианты клинического течения продромы. Наиболее неблагоприятным является течение продромы по типу сывороточной болезни (зуд, мигрирующие околосуставные высыпания).
Острый период (2 — 12 дней) протекает с интоксикационным синдромом: снижением аппетита, диспепсией, инверсией сна. В трети случаев возникает желтуха: резко повышается уровень билирубина, слизистые оболочки и кожа окрашиваются в различные оттенки жёлтого цвета, появляется зуд. Наиболее тревожным симптомом является снижение протромбинового индекса и альбумина крови, свидетельствующие о печёночно-клеточной недостаточности. Осложнение заболевания печёночной энцефалопатией свидетельствует об острой гепатодистрофии. Бурный гуморальный иммунный ответ зачастую приводит к появлению иммунных комплексов, оседающих на эндотелии сосудов почек, щитовидной железы, половых органов и др. Возникают васкулиты. В программе системных проявлений HBV-инфекции могут возникать аутоиммунный тиреоидит, хронический гастрит, синдром Шегрена, идеопатическая тромбоцитопеническая пурпура, узелковый периартериит, гломерулонефрит, синдром Гийена Барре, ревматоидный артрит и др.
Фаза выздоровления характеризуется исчезновением признаков холестаза, нормализацией процессов обмена веществ, восстановлением функции печени, на первый план выходят системные проявления заболевания. По сравнению с другими вирусными гепатитами, гепатит В имеет более системный характер, менее благоприятно протекает у детей. Хроническое течение возникает в 5% случаев. «Здоровые носители» HBsAg, также как и больные хроническим гепатитом В, подвержены высокому риску развития цирроза печени и гепатоцеллюлярной карциномы. Системные проявления не всегда исчезают вместе с излечением гепатита В.
Разработанные на сегодняшний день вакцины не вызывают вакцино-обусловленного гепатита В, т. к. представляют собой генно-инженерный HBs-антиген. Однако вакцинопрофилактика обеспечивает защиту от гепатита В только на 5 — 7 лет. До вакцинации, по итогам вакцинации и по прошествии 5 лет после вакцинации необходимо исследовать уровень anti-HBs-антител.
| Уровень anti-HBs (Ед/л) | Рекомендуемые сроки
ревакцинации |
| менее 10 | Немедленно |
| 11 — 100 | Через 3 — 6 месяцев |
| 101 — 1000 | Через 1 год |
| 1001 — 10000 | Через 3,5 года |
| более 10000 | Через 7 лет |
Оформление заявок для проведения исследований в ООО «ИНВИТРО» осуществляется по паспорту или документу, его заменяющему (миграционная карта, временная регистрация по месту жительства, удостоверение военнослужащего, справка из паспортного стола при утере паспорта, регистрационная карта учёта из гостиницы). Предъявленный документ в обязательном порядке должен содержать информацию о временной или постоянной регистрации на территории РФ и фотографию. При отсутствии паспорта (документа его заменяющего) пациент вправе оформить анонимную заявку для сдачи биоматериала. При анонимном обследовании, заявке и полученному от клиента образцу биоматериала присваивается номер, известный только пациенту, и медперсоналу, оформлявшему заказ.
! Результаты исследований, выполненных анонимно, не могут быть представлены для госпитализации, профессиональных осмотров и не подлежат регистрации в ОРУИБ.
Аланинаминотрансфераза и специфические маркеры вирусных гепатитов в крови доноров | Буркитбаев
1. Zhiburt E.B., Belgesov N.V., Vaschenko T.N. et al. Alanine aminotransferase is a surrogate marker of viral hepatitis. Vopr virusol 1995; 1(40):25-7.
2. Zhiburt E.B. Study design «The Importance of Screening of Alanine Aminotransferase in donors blood for the Prevention of Post-Transfusion Hepatitis». Transfusiology 2004; 1(5):90-7.
3. Zhiburt E.B. About ALT and not only. Transfusiology 2004; 1(5):102-6.
4. Zhiburt E.B., Abzhueva O.V., Atakishiev M.M. et al. Significance of activity of alanine aminotransferase as a surrogate marker of transfusion-transmitted infections — the results of a national study. Vestnik Sluzby Krovi Rossii 2005; 2:22-7.
5. Zhiburt E.B. Alanine aminotransferase is a surrogate marker of viral hepatitis. Vopr virusol 2005; 6(50):18-20.
6. Zhiburt E.B., Kodenev A.T. Preliminary screening of alanine aminotransferase activity increases the economic efficiency of blood production. Klin labor diagnost 2009; 11:14-6.
7. Golosova S.A., Cherkasov E.G., Popova V.I. et al. Donors blood with increased ALT activity, but with a negative EIA result for viral hepatitis, does not contain these viruses. Top issues hematol transfusiol 2004; 118-9.
8. Filina N.G., Kolotvina T.B., Titova S.A., Zhiburt E.B. Diagnostic significance of alaninaminotransferase detection in donors blood. Transfusiology 2011; 1(12):9-12.
9. Filina N.G., Kolotvina T.B., Titova S.A., Zhiburt E.B. Preliminary screening of blood donor alaninaminotransferase activity has been lost its economical efficacy. Transfusiology 2011; 3(12):61-4.
10. Petrik J., Lozano M., Seed C.R. et al. Hepatitis E. Vox Sang 2016; 1(110):93-103.
11. Tereshchenko Y.A., Tereshchenko S.Y. Asymptomatic increase in serum aminotransferase activity: stages of diagnostic search. Ross z gastroenterol gepatol koloproktol 2014; 1(24):29-38.
12. Приказ и.о. Министра здравоохранения Республики Казахстан от 10 ноября 2009 года № 684 «Об утверждении Правил контроля качества и безопасности донорской крови и ее компонентов».
13. Abdrakhmanova S. The pattern of donor blood rejection after implementation of pre-donation liver transferase screening. Vox Sang 2016; 111(Suppl. 1):149-50.
14. Rommel K., Koch C.D., Spilker D. Influence of specimen withdrawal on the results of chemical analyses of blood, plasma and serum in patients with stable or centralized circulation. J Clin Chem Clin Biochem 1978; 16(7):37380.
15. Haymond R.E., Knight J.A. Venous serum, capillary serum, and capillary plasma compared for use in determination of lactate dehydrogenase and aspartate aminotransferase activities. Clin Chem 1975; 21(7):896-7.
16. Solanki A., Singh A., Chaudhary R. Impact of grey zone sample testing by enzyme-linked immunosorbent assay in enhancing blood safety: Experience at a tertiary care hospital in North India. AJTS 2016; 10(1):71-4.
17. Alter M.J., Kuhnert W.L., Finelli L. Guidelines for laboratory testing and result reporting of antibody to hepatitis C virus. MMWR Recomm Rep 2003; 52(RR-3):1-13, 15; quiz CE1-4.
18. Ivashkin V.T., Herman E.N., Maevskaya M.V. Hidden infection with hepatitis B virus. Ross z gastroenterol gepatol koloproktol 2008; 2(18):4-11.
Диагностика вирусных гепатитов
Гепатит — серьезное заболевание, поражающее, главным образом, печень. В частности гепатит В и С способствуют развитию хронических заболеваний и, в последствии, приводят к циррозу и раку печени. Анализ на гепатит — эффективная мера по предупреждению серьезных последствий этой вирусной инфекции.
Гепатит А
Гепатит А передается контактным путем через зараженные предметы обихода, продукты питания и воду. Для предотвращения этого вируса достаточно соблюдать правила личной гигиены. Анализ на гепатит А заключается в выявлении повышенного уровня печеночных ферментов и билирубина.
Гепатит В
Гепатит В передается через кровь естественным или искусственным путем. Эта разновидность вируса определяется по наличию в крови специфических антител, образующихся в результате выработки вирусом антигенов.
Гепатита С
Передача вируса гепатита С осуществляется парентерально и может приводить к хроническим формам заболевания. Лабораторная диагностика вирусных гепатитов этого вида предполагает проведение нескольких тестов (ПЦР, биохимия крови). К сожалению, в настоящее время вакцина против гепатита С не изобретена.
Где сдать анализы на гепатит?
Сдать анализ на гепатит можно в Минске, Гомеле, Бресте, Гродно, Витебске, Могилеве, Бобруйске, Барановичах, Солигорске, Слуцке, Полоцке, Новополоцке, Орше, Жлобине, Светлогорске, Молодечно, Пинске, Борисове, Речице, Мозыре, Сморгони.
Помимо указанных, существуют и другие типы вирусных гепатитов. Но А, В и С являются самыми распространенными. В медицинской лаборатории «Синэво» Вы можете сдать анализы на гепатит А, В и С и максимум через три дня получить результаты исследований. Лечение гепатита — не то дело, которое стоит откладывать на завтра.
Научно-популярные статьи – полезная информация на сайте ЛИТЕХ
Вирус гепатита В (hepatitis B virus, HBV) относится к семейству Hepadnoviridae. Геном вируса представлен частично сдвоенной кольцевой молекулой ДНК размером 3200 п.н. При электронной микроскопии HBV выглядит сферической частицей диаметром 42 нм (частица Дейна), состоящей из ядра — нуклеотида, имеющего форму икосаэдра диаметром 28 нм, внутри которого находится двуцепочечная ДНК, концевой белок и фермент ДНК-полимераза. В состав нуклеоидного белка входят HBcAg и HBeAg. Внешняя оболочка (толщиной 7 нм) образована поверхностным антигеном HBV — HBsAg. Вирус гепатита В является псевдоретровирусом, т. е. его ДНК может частично встраиваться в геном гепатоцитов.
При ОВГ и обострении ХГ вирусные частицы можно обнаружить в гепатоцитах и сыворотке крови больного. При интегративной форме ХГ В и в стадии ремиссии HBV в сыворотке крови не выявляется.
Основой лабораторной диагностики инфекции HBV является определение серологических маркеров инфицирования вирусом: HBsAg, HВeAg, анти-НВс класса IgM и IgG, анти-НВе и анти-HBs, HBV ДНК и активности вирусной ДНК — полимеразы. В зависимости от течения вирусного гепатита В спектр изменения серологических маркеров выглядит по-разному.
HBsAg — основной маркер инфицирования HBV. При остром вирусном В в большинстве случаев (90-80 %) HBsAg удается выявить в инкубационном периоде, начиная с 3-5-й недели заражения. Средняя продолжительность циркуляции антигена — 70-80 дней. Быстрое исчезновение HBsAg (в первые дни желтухи) с появлением антиНВs — плохой прогностический признак. При хроническом гепатите В HBsAg может циркулировать в крови больного на протяжении многих лет. Следует отметить, что применяющиеся в настоящее время методы определения HBsAg, в том числе ИФА, имеют порог чувствительности. Поэтому при наличии клинических признаков гепатита и отсутствиии HBsAg в сыворотке крови необходимо исследовать другие маркеры инфекции HBV. Наличие HBsAg в крови свидетельствует о присутствии вируса в печени и с большой долей вероятности в крови. Не всякая сыворотка, содержащая HВsAg, содержит вирус гепатита В. В ряде случаев ДНК вируса встраивается в ДНК гепатоцита не полностью, а частично, только тем участком, который кодирует синтез HBsAg. В этих случаях синтезируется HBsAg без других компонентов вириона (то есть без других антигенов). Считают, что такая ситуация возникает при “здоровом” носительстве HBsAg.
HBeAg вируса гепатита В характеризует высокую инфекционность крови, являясь показателем активной репликации HBV. HBeAg циркулирует в крови больного только в присутствии HBsAg. В первую неделю желтушного периода он выявляется у 85-95 % больных. Выявление HBeAg в течение двух и более месяцев служит прогностическим признаком развития хронического гепатита. У большинства больных хроническим гепатитом с высокой активностью процесса HBeAg сохраняется на длительный срок (до нескольких лет).
Антитела к ядерному антигену вируса гепатита В класса M (анти-НВc IgM) — маркер активной репликации НВV и острой инфекции. Выявляются через 1-2 недели после обнаружения HBsAg и сохраняются на протяжении 2-18 месяцев. У 4-20 % больных острым гепатитом В анти-HBc IgM являются единственным маркером инфекции. При ХГ В анти-НВс IgM могут быть выявлены у некоторых больных в меньших титрах, чем при острой инфекции, причем титр антител отражает тяжесть гепатита.
Антитела к HBcAg класса G (анти-НВс IgG) появляются практически одновременно с анти-НВс IgM. Как првило, они остаются у всех лиц, переболевших гепатитом В, пожизненно. У 95 % носителей HBsAg наряду с HBsAg циркулируют и анти-НВс IgG.
Антитела к HBsAg (анти-НВs) свидетельствуют о ранее перенесенной инфекции или о наличии поствакцинального иммунитета (защитный уровень — 10 МЕ/мл). Они появляются в период выздоровления, через 4 недели после исчезновения HBsAg, достигая максимальной концентрации через 1-2 года, с последующим постепенным снижением уровня, недоступного выявлению современными методами диагностики. В некоторых случаях анти-HВs могут циркулировать пожизненно. Появление анти-HBs на фоне клинического улучшения у больного гепатитом В является хорошим прогностическим признаком. Важно отметить, что в динамике острой инфекции HBV имеется “окно”, когда HBsAg уже не определяется, а ан-ти-HBs еще не появились. При этом выявляются анти-HBc IgM и IgG. Из этого следует вывод о необходимости обследования больных ОВГ на анти-HBc IgM даже при отрицательных результатах исследования HBsAg и анти-НВs.
Антитела к HBeAg (анти-НВе) появляются в крови после элиминации HBeAg и завершения репликации вируса. К концу 9-й недели острого периода гепатита В более 90 % больных имеют анти-НВе. В период выздоровления анти-НВе могут исчезать. Однако, наличие анти-НВе не является показателем отсутствия инфекционности конкретной сыворотки крови. Показано, что у ряда больных в ходе развития гепатита В (около 10%) под влиянием “иммунного давления” на вирус возникают мутантные формы, которые “избегают” иммунного надзора и не элиминируются. У носителей анти-HBe был выделен мутант, неспособный продуцировать HBeAg из-за дефектов в области precore и получивший обозначение HBeAg-отрицательного. Появление HBeAg-отрицательного мутанта приводит к прогрессированию поражения печени при продолжающейся репликации вируса (наличие ДНК HBV в сыворотке крови). При первичном инфицировании HBeAg-отрицательным мутантом существенно возрастает риск развития фульминантного гепатита.
Описанные маркеры гепатита В исследуются методом ИФА. Спектр антител (анти-НВе, анти-НВs, анти-НВc IgM, анти-НВc IgG) и антигенов (HBsAg, HBeAg) позволяет установить диагноз гепатита В и определить стадию заболевания (таблица 5). Недостатком данного метода является невозможность его использования при заражении мутантными формами вируса, при иммуносупрессии (больные онкологическими заболеваниями, наркоманы и т.д.) и для количественной оценки присутствующего в организме возбудителя. Решение этих задач стало возможным в результате внедрения молекулярно-биологических методов в практику клинико-диагностических лабораторий.
Таблица 5. Различные сочетания серологических маркеров инфицирования вирусом гепатита В и их интерпретация
|
HBsAg |
HBeAg |
антиНВ c IgM |
антиНВ c сумм |
антиНВе |
антиНВs |
HBV ДНК |
Трактовка результата |
|
+ |
+ |
+ |
+ |
— |
— |
+ |
Острый гепатит В. Дикий штамм |
|
+ |
— |
+ |
+ |
— |
— |
+ |
Острый гепатит В. Мутантный штамм |
|
+ |
— |
+/- |
+ |
+ |
— |
-/+ |
Разрешившийся острый гепатит В. Сероконверсия. |
|
+ |
+ |
+/- |
+ |
-/+ |
— |
+ |
Хронический активный гепатит В |
|
+/- |
-/+ |
-/+ |
+ |
+/- |
— |
+/- |
Хронический интегративный гепатит В |
|
+ |
— |
— |
+ |
— |
-/+ |
— |
«Здоровое» носительство |
|
— |
— |
— |
+ |
-/+ |
+ |
— |
Перенесенный вирусный гепатит В |
|
— |
— |
— |
— |
— |
+ |
— |
Состояние после иммунизации |
Методы генодиагностики, к которым относится ПЦР, существенно расширяют возможности лабораторной диагностики вирусного В, позволяя непосредственно выявить возбудитель, установить тканевую и внутриклеточную локализацию HBV, выявить и охарактеризовать мутантные формы вируса, оценить уровень виремии в течение заболевания, в том числе — на фоне противовирусной терапии.
В настоящее время существует широкий спектр диагностических тест-систем для выявления ДНК HBV в лабораторных условиях, основанных на методах ПЦР — фирмы “Roche”, НПФ “Литех”, “ДНК технология”, LCR (лигазная цепная реакция) — фирма “Abbott”, bDNA (метод “развлетвленных” ДНК зондов) — фирма “Chiron”. Эти тест-системы позволяют проводить качественное определение наличия возбудителя в биологическом материале: сыворотке или плазме крови, ткани печени, мононуклеарах. Одним из вариантов качественного определения ДНК HBV является технология ПЦР in situ (в гистологических срезах), позволяющая установить внутриклеточную локализацию вируса в гепатоцитах.
Единственная коммерческая тест-система дифференциальной диагностики НВеAg-отрицательного гепатита В создана фирмой “Abbot” с использованием LCR. Существенным недостатком этой системы является выявление только одной из многих мутаций, приводящих к отсутствию синтеза НВеAg вирусом. Выявление всей совокупности генетических изменений, характерных для НВеAg-отрицательных вирусов гепатита В, возможно пока только прямым секвенированием ПЦР-амплифицированных фрагментов вирусного генома.
Количественная характеристика содержания ДНК HBV в клинических образцах важна для оценки эффективности противовирусной терапии и имеет прогностическое значение для определения хронизации HBV. При исходно низком уровне виремии (ДНК HBV менее 500 фг/мкл) процент хронизации острого гепатита В близок к нулю, при концентрации HBV ДНК от 500 до 2000 фг/мкл хронизация процесса наблюдается у 25-30% больных, а при высоком уровне виремии у пациента (более 2000 фг/мкл) острый гепатит В чаще всего переходит в хронический.
Известные коммерческие тест-системы оценки концентрации ДНК HBV реализуют принцип конкурентного ПЦР-анализа с последующей гибридизационной схемой определения продуктов амплификации (фирма “Roche”, НПФ “Литех”). Этот подход основан на внесении в клинический образец внутреннего стандарта известной концентрации, качественно отличающегося от определяемой матрицы. После ПЦР концентрация ДНК HBV в исследуемом материале рассчитывается на основании известной концентрации внутреннего стандарта и соотношения накопления продуктов амплификации внутреннего стандарта и определяемой матрицы.
В настоящий момент развитие методов лабораторной диагностики гепатита В идет по направлению создания коммерческих тест-систем для идентификации клинически значимых мутантных штаммов HBV, а также использованию новых оптических приборов (биосенсоров) для комплексной диагностики инфекции HBV (вирусных белков, антител к ним и ДНК HBV).
неожиданно высокий уровень сочетанной инфекции тихим гепатитом B
Наркомания. Авторская рукопись; доступно в PMC 2013 28 октября.
Опубликован в окончательной редакции как:
PMCID: PMC3810150
NIHMSID: NIHMS512815
Гэвин Барт
1 Лаборатория биологии аддиктивных заболеваний Нью-Йорк, США
Паола Пикколо
2 Департамент медицины, больница Фатебенефрателли Изола Тиберина, Рим, Италия
Линци Чжан
3 Центр исследования СПИДа Аарона Даймонда, Университет Рокфеллера, Нью-Йорк, США
4 Центр исследований СПИДа, Институт биологии патогенов Китайской академии медицинских наук и Пекинский медицинский колледж, Пекин, Китай
Ира Якобсон
5 Гастроэнтерология и гепатология, Медицинский колледж Вейл Корнелл, Нью-Йорк, США
Роберт А.Schaefer
5 Гастроэнтерология и гепатология, Медицинский колледж Вейл Корнелл, Нью-Йорк, США
Мэри Джин Крик
1 Лаборатория биологии аддиктивных заболеваний, Университет Рокфеллера, Нью-Йорк, США
1 The Лаборатория биологии аддиктивных заболеваний, Университет Рокфеллера, Нью-Йорк, США
2 Департамент медицины, Больница Фатебенефрателли Изола Тиберина, Рим, Италия
3 Центр исследования СПИДа Аарона Даймонда, Университет Рокфеллера, Нью-Йорк, США
4 Центр исследований СПИДа, Институт биологии патогенов Китайской академии медицинских наук и Пекинский медицинский колледж Союза, Пекин, Китай
5 Гастроэнтерология и гепатология, Медицинский колледж Вейл Корнелл, Нью-Йорк, США
Для корреспонденции: Мэри Жанна Крик, Лаборатория биологии аддиктивных заболеваний, Университет Рокфеллера, 1230 York Avenue, NY 10021 , США.ude.rellefekcor@keerk Окончательная отредактированная версия этой статьи издателем доступна на Addiction. См. другие статьи в PMC, в которых цитируется опубликованная статья.Abstract
Цели
Определить распространенность вирусов гепатита A, B и C у пациентов, посещающих клинику поддерживающей метадоновой терапии в Нью-Йорке.
Окружение
Клиника обслуживания взрослых медицинского колледжа Вейл Корнелл, метадоновая программа, связанная с городской больницей.
Участники
Взрослые, бывшие героиновой зависимостью ( n = 103), проходят поддерживающую терапию метадоном.
Измерения
Маркеры вируса гепатита A [иммуноглобулин M (IgM) HAV и имуноглобулин G (IgG)], гепатита B [поверхностный антиген гепатита B (HBsAg), поверхностные антитела гепатита B (HBsAb) и ядерные антитела гепатита B (HBcAb). )] и вируса гепатита С (HCVAb). Также были получены сывороточная аланинаминотрансфераза (ALT) и количественная РНК HCV. Качественное определение ДНК HBV и генотипа HCV было получено в подгруппе субъектов.
Результаты
Более 40% испытуемых имели маркеры для всех трех вирусов.HCVAb был наиболее распространенным (83,5%), за ним следовали HBcAb (65,0%), HAV IgG (46,1%) и HBsAb (41,1%). РНК гепатита С была обнаружена у 70,6% HCVAb-положительных субъектов. Хотя ни у одного субъекта не было HBsAg, ДНК HBV была обнаружена у 26,4% субъектов, прошедших эту меру; все ( n = 20) имели HBcAb в качестве единственного маркера HBV. Наличие ДНК HBV не влияло на АЛТ. У субъектов с РНК ВГС были более высокие уровни АЛТ, чем у лиц без РНК ВГС.
Выводы
У большинства субъектов, получающих метадон, был по крайней мере один маркер вирусного гепатита, из них 41.8% имеют маркеры HAV, HBV и HCV. У четверти субъектов была скрытая инфекция HBV, определяемая как наличие ДНК HBV в отсутствие HBsAg. Эти предметы следует считать заразными и представлять опасность для здоровья населения.
Ключевые слова: Гепатит В, гепатит С, поддерживающая метадоновая терапия, скрытая инфекция, вирусный гепатит
ВВЕДЕНИЕ
Передача инфекционного гепатита при употреблении инъекционных наркотиков (ПИН) признана более 50 лет назад [1].Ранние исследования нашей и других групп показали, что 85–95% нелеченных героиновых наркоманов и героиновых наркоманов, получающих поддерживающую терапию метадоном (MMT), имели по крайней мере один серологический маркер вируса гепатита B (HBV) [2–4]. С открытием вируса гепатита С (ВГС) и последующим развитием серологических тестов было обнаружено, что 60–98% наркоманов и пациентов, получающих ММТ, имеют маркеры инфекции ВГС [5–8]. Ранее мы сообщали, что 60% пациентов с MMT имеют серологические маркеры обоих вирусов [9].В то время как инфекция вируса гепатита А (ВГА) реже передается через ПИН, сообщалось о вспышках среди ПИН, а инфицирование на фоне ВГС увеличивает вероятность молниеносной печеночной недостаточности [10,11]. Недавние отчеты из сельской Германии и округа Лос-Анджелес, Калифорния, показали, что примерно у 30% ПИН есть маркеры всех трех вирусов [12,13].
Стандартный скрининг на вирусный гепатит включает определение сывороточных антител. Поскольку инфекция HAV, как правило, является ограниченным по времени заболеванием, наличие антител к HAV [иммуноглобулин G (IgG) к HAV] указывает на разрешенную инфекцию с продолжающейся иммунозащитой от повторного инфицирования.Поскольку вакцинация против HAV стимулирует продукцию IgG к HAV, стандартный скрининг на HAV не может отличить прошлую инфекцию от предшествующей иммунизации.
Стандартный скрининг на ВГС выявляет антитела (HCVAb), которые указывают на инфекцию, но не позволяют различить разрешенную и продолжающуюся инфекцию. Присутствие РНК HCV определяет текущую инфекцию и выявляется примерно у 75% тех, кто является HCVAb-положительным. В настоящее время вакцинация от ВГС отсутствует.
Как и ВГА, ВГВ обычно носит ограниченный по времени характер.Менее 5% взрослых, инфицированных ВГВ, заболевают хронической инфекцией, причем треть из них страдает серьезными заболеваниями, связанными с ВГВ [14]. Скрининг на HBV включает тесты на активную инфекцию [поверхностный антиген HBV (HBsAg) и ядро антитела HBV, иммуноглобулин M (HBcAb IgM)] и иммунитет [поверхностное антитело HBV, HBsAb и ядро антитела HBV IgG (HBcAb IgG)]. Вакцинация против HBV индуцирует HBsAb, тогда как инфекция HBV может индуцировать продукцию как HBsAb, так и HBcAb. Следовательно, присутствие поверхностного антитела в отсутствие ядра антитела обычно указывает на предшествующую вакцинацию.ДНК HBV присутствует во время активной инфекции (то есть во время положительного теста на HBsAg), но она не измеряется рутинно, за исключением тех, кому требуется мониторинг хронического HBV, и тех, кто находится в режиме лечения. За исключением необычных обстоятельств (см. Обсуждение скрытого HBV ниже), пациенты с предыдущей инфекцией HBV, у которых развился иммунитет (т. Е. Отрицательный HBsAg и положительный HbsAb, с HBcAb или без него), больше не имеют определяемой ДНК HBV.
Серологически тихая (также называемая скрытой или латентной) инфекция HBV определяется наличием вирусной ДНК в отсутствие HBsAg [15].Вирусная ДНК необходима для репликации вируса и, следовательно, для передачи информации. Однако большинство пациентов с «тихой» инфекцией HBV имеют HBcAb IgG-положительные [16]. Хотя существует множество тестов для скрининга на ВГВ, стандартный скрининг ограничивается в основном тестом на инфекцию (HBsAg) и тестом на иммунитет (HBsAb) [14], поэтому общие клинические условия не включают HBcAb в свою панель скрининга. . Таким образом, возможно, что стандартный скрининг на HBV упустит важный ключ (например, HBcAb) к скрытой инфекции HBV.Это имеет клиническое значение, потому что сыворотки от пациентов с скрытой инфекцией HBV заразны, и эти люди должны рассматриваться как имеющие продолжающуюся инфекцию HBV [17,18]. Хотя о крупных эпидемиологических исследованиях скрытой инфекции HBV не сообщалось, в нескольких небольших исследованиях была обнаружена связь между скрытой инфекцией HBV и плохой иммунокомпетентностью, употреблением инъекционных наркотиков и инфекцией HCV [19–21].
В настоящем исследовании представлены данные о HAV, HBV, HCV и скрытой HBV-инфекции в когорте бывших опиатных наркоманов, получавших MMT, посещающих Клинику обслуживания взрослых медицинского центра Weill Cornell в Нью-Йорке.
МЕТОДЫ
С ноября 2000 г. по сентябрь 2004 г. мы проводили тесты на серологические маркеры вирусного гепатита у бывших опиатных наркоманов, посещавших Клинику обслуживания взрослых медицинского центра Weill Cornell в Нью-Йорке, городскую программу MMT. Набор проводился лицом к лицу с пациентами врачом-исследователем и медсестрой. Пациентам и медицинскому персоналу также предлагалось несколько групповых занятий по вирусному гепатиту и исследованию. Клинический персонал мог направлять пациентов в ежедневные рабочие часы для получения дополнительной информации / участия в исследовании.Единственным исключением из участия в исследовании была невозможность дать информированное согласие. Исследования начинались только после одобрения соответствующих комитетов по обзору Рокфеллеровского университета и Медицинского колледжа Вейля Корнелла и проводились в соответствии с Хельсинкской декларацией 1975 года, пересмотренной в 1983 году.
После получения письменного информированного согласия мы протестировали 103 субъекта на предмет пригодности. Антитело HAV (HAVAb IgM и IgG), поверхностный антиген HBV (HBsAg), ядро антитела HBV (HBcAb IgM и IgG), поверхностное антитело HBV (HBsAb) и РНК HCV (РНК 3 HCV.0 bDNA IVD, нижний предел обнаружения 2500 копий / мл; Bayer Diagnostics, Беркли, Калифорния, США). Тридцать три субъекта также предоставили отдельное согласие на тестирование на антитела к ВИЧ. Также определяли уровень АЛТ в сыворотке (верхний предел нормы 37 МЕ / мл).
Из-за бюджетных ограничений мы смогли протестировать только первых 79 последовательных субъектов, включенных в исследование на ДНК HBV с помощью полимеразной цепной реакции (ПЦР) в реальном времени (диапазон обнаружения 1,0 × 10 2 — 1,0 × 10 9 копий / мл).Этот анализ на основе молекулярных маяков был разработан и утвержден одним из авторов (LZ), хорошо коррелирует с COBAS AMPLICOR HBV Monitor [22] и предлагает более широкий диапазон обнаружения, чем любой отдельный доступный коммерческий анализ (комбинированный диапазон для нескольких продуктов: 2,0 × 10 2 — 5,0 × 10 9 ) [23]. Тихий HBV был определен как присутствие ДНК HBV в отсутствие HBsAg [15]. За исключением случаев, указанных выше, все лабораторные исследования были выполнены в клинических лабораториях Мемориального онкологического центра Слоуна-Кеттеринга (Нью-Йорк, Нью-Йорк, США).
Данные о вирусных маркерах отсутствовали у разных людей либо из-за недостаточного размера образца для выполнения теста, либо из-за того, что тест не был проведен. Из 103 участников у одного субъекта не было данных о HAV, у девяти не было данных о HBsAb, а у одного не было данных о РНК HCV. У двух из 79 субъектов, протестированных на ДНК HBV, отсутствовали данные. Ни один субъект не тестировался на HBeAg, HBeAb или HDV.
РЕЗУЛЬТАТЫ
Средняя клиническая перепись за период исследования составила 210 человек.Всего в исследовании приняли участие 103 человека. Шестьдесят семь процентов субъектов были мужчинами, а средний возраст составлял 46 лет [диапазон 22–71; стандартное отклонение (8,7). 57% составляли европеоид, 11% афроамериканец, 29% латиноамериканец и 3% принадлежали к другой или нераскрытой этнической принадлежности. Демографические данные субъектов исследования не отличались от демографических данных пациентов клиники, которые не участвовали. в исследовании
Ни один из субъектов в этом исследовании не был положительным на HBsAg.Показано преобладание маркеров антител для HAV, HBV и HCV.46% (48 из 102) пациентов были положительными по HAV IgG (ни у одного из субъектов не было HAV IgM). Хотя в клинике не проводилась вакцинация против ВГА, у нас нет документации о количестве субъектов, которые могли пройти вакцинацию где-либо еще. Семьдесят процентов ( n = 72) всех субъектов имели по крайней мере один серологический маркер вируса гепатита B (данные о количестве субъектов, получивших вакцинацию против HBV, отсутствуют, хотя только семь субъектов имели HBsAb в качестве единственного маркера HBV).У девяноста одного субъекта были полные наборы данных по всем вирусным маркерам; из них 41,8% ( n = 38) имели маркеры для всех трех вирусов (). Антитела к ВИЧ были обнаружены у трех из 33 испытуемых.
Таблица 1
Распространенность маркеров вирусных гепатитов.
| HAV IgM | HAV IgG | HBsAg | HBsAb | HBcAb | HCVAb |
|---|---|---|---|---|---|
| n7103 n7 n = 95 | n = 103 | n = 103 | |||
| 0/102 = 0% | 47/102 = 46.1% | 0/103 = 0% | 39/95 = 41,1% | 67/103 = 65,0% | 86/103 = 83,5% |
Таблица 2
Распространенность маркеров вирусного гепатита в подмножество субъектов, для которых были доступны полные данные по всем трем вирусам.
| Вирусные маркеры | Субъекты (n = 91) | |
|---|---|---|
| Нет | 11/91 = 12,1% | |
| Только HAV | 0/9116 = 0% | 1/91 = 1.1% |
| только HCV | 10/91 = 11,0% | |
| только HAV + HBV | 3/91 = 3,3% | |
| только HAV + HCV | 4/91 = 4,4% | |
| только HBV + HCV | 24/91 = 26,4% | |
| HAV + HBV + HCV | 38/91 = 41,8% |
РНК вируса гепатита C была обнаружена у 70,6% пациентов с HCVAb ( n = 86). Связи между вирусной нагрузкой ВГС и количеством серологических маркеров вирусного гепатита не было (данные не показаны).РНК HCV (4470 копий / мл) была обнаружена у субъекта, отрицательного по HCVAb, который ранее прошел абляционную химиотерапию лимфомы. Этот субъект также был отрицательным по всем другим маркерам антител вирусного гепатита, несмотря на то, что он описал отдаленный анамнез «сывороточного гепатита». Из-за бюджетных ограничений только первые 43 субъекта с положительной реакцией на РНК ВГС прошли генотипирование. Тридцать два субъекта имели генотип 1, пять субъектов имели генотип 2a, пять субъектов имели генотип 2b и один субъект имел генотип 3.
Данные о ДНК HBV доступны для первых 77 субъектов, включенных в исследование ().Двадцать шесть процентов ( n = 20) были положительными по HBV-ДНК. Все 20 субъектов имели анти-HBcAb в качестве единственного маркера HBV. У пяти (8,7%) из 57 субъектов, отрицательных по ДНК HBV, HBcAb был единственным маркером HBV. Шестьдесят пять процентов и 59% субъектов с положительной ДНК HBV и отрицательной ДНК HBV, соответственно, также были положительными по РНК HCV.
Таблица 3
Статус маркера вируса гепатита B (HBV) и ДНК HBV.
| HBsAb — HBcAb — | HBsAb + HBcAb — | HBsAb + HBc156 + HBcAb +6 HBcAb | ||||
|---|---|---|---|---|---|---|
| ДНК HBV + ( n = 20) | 0 | 0 | 0 | 20 | ||
| HBV-ДНК — ( n = 57) | 17 | 17 | 24 * | 5 * |
Тестирование на ВИЧ было проведено у 23 из 77 субъектов, которые также были протестированы на ДНК HBV.Антитела против ВИЧ были обнаружены у трех из этих субъектов. Из 17 испытуемых, прошедших тестирование на ВИЧ и имевших отрицательный результат на ДНК ВГВ, только один был ВИЧ-положительным. Из шести испытуемых, прошедших тестирование на ВИЧ и имевших положительный результат на ДНК ВГВ, двое были ВИЧ-положительными.
В 77 субъектах с данными, доступными как для РНК ВГС, так и для ДНК ВГВ, мы использовали дисперсионный анализ факторного дизайна 2 × 2, чтобы выяснить, влияет ли вирусный статус на уровни сывороточной АЛТ (). Уровни АЛТ в сыворотке крови у субъектов с РНК ВГС были значительно выше, чем у лиц без РНК ВГС ( F 1,73 = 11.4, P < 0,01). Присутствие ДНК HBV не влияло на уровни ALT, а также не было эффекта взаимодействия между РНК HCV и ДНК HBV на уровни ALT.
Таблица 4
Уровни аланинаминотрансферазы в сыворотке по ДНК вируса гепатита B (HBV) и статусу РНК HCV. Средние значения (стандартное отклонение) приведены в МЕ / мл.
| РНК ВГС + * | РНК ВГС — | ||||
|---|---|---|---|---|---|
| ДНК ВГВ + | n = 13 68.3 (55,0) | n = 7 32,3 (19,7) | |||
| ДНК HBV — | n = 34 71,2 (55,8) | n = 23 25,9 (12,2) |
| Гепатит | А | В | С | D | E |
| Вирус | HAV | HBV | ВПЦ | HDV | HEV |
| Семья | Пикорнавирус | Гепаднавирус | Флавивирус | Спутник | Калицивирус |
| Геном | оцРНК | дцДНК | оцРНК | оцРНК | оцРНК |
| Распространение | Фекально-оральный | парентерально, половое, перинатальное | парентерально,? Половое | парентерально,? Половое | Фекально-оральный |
| Антигены | HAV-Ag | HbsAg, HBcAg, HBeAg | HCV-Ag | HDV-Ag | HEV-Ag |
| Антитела | Anti_HAV | Anti-HBs, Anti-HBc, Anti-HBe | Анти-HCV | Анти-HDV | Анти-HEV |
| Вирусные маркеры | РНК ВГА | ДНК HBV, ДНК-полимераза | HCV RNa | HDV RNa | вирусоподобных частиц |
Семин.Печень Ds. 11: 74,1991, Thieme Medical Publishers, Inc.
Серология гепатита А
- anti-HAV (антитела к гепатиту А
вирус)
, он выявляет общие антитела как IgG, так и IgM под классами HAV. Его наличие указывает на острую или разрешенную инфекцию. - IgM anti-HAV (подкласс антител IgM анти-HAV,
вирус гепатита A)
указывает на недавнюю инфекцию HAV (<6 месяцев). Это использовано для диагностики острого гепатита А
Серология гепатита В
- HBsAg (поверхностный антиген гепатита B)
указывает на острую или хроническую инфекцию вируса гепатита B (HBV). - anti-HBs (HBsAb = антитело к поверхностному гепатиту B
антиген)
это маркер иммунитета к гепатиту В. - anti-HBc (HBcAb = антитело к ядру гепатита B
антиген)
это неспецифический маркер острой, хронической или разрешенной инфекции HBV. Это не маркер иммунитета, индуцированного факцином. - IgM anti-HBc (подкласс антител IgM
anti-HBc)
указывает на недавнюю инфекцию HBV (<6 месяцев).Его присутствие указывает на острую инфекцию. - HBeAg (антиген гепатита B «е»)
это маркер высокой степени инфекционности HBV и коррелирует с высокий уровень репликации HBV. Он в основном используется для определения клиническое ведение пациентов с хронической инфекцией HBV. - anti-HBe (антитело к гепатиту B «е»
антиген)
он может быть преснетом у инфицированного или иммунного человека. У лиц с хроническая инфекция HBV, ее наличие предполагает низкий титр вируса и низкий степень заразности. - ДНК HBV (дезоксирибонуклеиновая кислота HBV)
является маркером репликации вируса. Это хорошо коррелирует с инфекционностью. Он используется для оценки и мониторинга лечения пациентов с хроническим ВГВ-инфекция.
Серология гепатита С
- anti-HCV (антитела к HCV — вирусу гепатита С)
методом ELISA или RIBA-2
для выявления острой и хронической инфекции гепатита С - Качественный и количественный анализ РНК HCV в сыворотке
методом ПЦР
для установления виремии и используется при лечении хронической инфекции ВГС - Генотипирование РНК HCV (генотип 1-меньше
Rx-чувствительность или генотип 2 или 3 с лучшей Rx-реактивностью)
Исследования 1998 года комбинированной терапии интерфероном и рибавирином показали важные различия в исходе на основе генотипа ; что составляет примерно 30% пациентов с генотипом 1 и примерно 65% с генотипом 2 или 3 имели устойчивые вирусологические ответы .Кроме того, пациенты с генотипом 1 имели более высокий уровень стойкого вирусологического ответа с 48 неделями комбинированной терапии, чем с 24 неделями терапии, тогда как пациенты с другими генотипами не достигли дополнительного улучшения после 24 недель терапии. Эти исследования привели к практике применения терапию в течение 12 месяцев для пациентов с генотипом 1, но только в течение 6 месяцев до люди с генотипом 2 или 3. Известно, что помимо генотипа прогнозировать вероятность успешной терапии рибавирином и интерфероном.
В начало | Домашняя страница
10262004
Гепатит B | Кливлендская клиника
ЭпидемиологияЭпидемиология
Уильям Кэри, Мэриленд
Заболевания печени, связанные с гепатитом B, остаются важной проблемой общественного здравоохранения и основной причиной заболеваемости и смертности.Это также является распространенной сложной проблемой для практикующих врачей.
Гепатит B встречается во всем мире, но его распространенность сильно различается; он особенно высок в Азии, Африке к югу от Сахары и южной части Тихого океана, а также среди определенных групп населения в Южной Америке, на Ближнем Востоке и в Арктике. Распространенность в Соединенных Штатах варьируется в зависимости от состава населения, включая количество иммигрантов из эндемичных районов, а также от факторов риска и поведения, таких как распространенность внутривенного употребления наркотиков и гомосексуальных практик.По оценкам агентств общественного здравоохранения, в Соединенных Штатах инфицировано около 1,25 миллиона человек, но во всем мире инфицировано 2 миллиарда человек, причем примерно 5% населения мира (или 350 миллионов человек) являются носителями хронического гепатита B. В типичный год, 70 000 американцев заражаются хроническим вирусом гепатита B (HBV), и примерно 5000 пациентов с хроническим гепатитом B умирают от осложнений, вызванных этим заболеванием. Во всем мире хронический гепатит B занимает десятое место среди причин смерти.
Гепатит B был впервые обнаружен в 1963 году доктором Барухом Блумбергом и его коллегами, которые идентифицировали белок («австралийский антиген», который реагировал на антитела пациентов с гемофилией и лейкемией. Связь этого белка с инфекционным гепатитом была обнаружена 3 года спустя. несколькими исследователями, а вирус был обнаружен с помощью электронной микроскопии в 1970 году.
HBV — это двухцепочечный гепатотропный ДНК-вирус, принадлежащий к семейству Hepadnaviridae. Вирус поражает только людей и некоторых других приматов.Репликация вирусов происходит преимущественно в гепатоцитах и, в меньшей степени, в почках, поджелудочной железе, костном мозге и селезенке. Вирусный геном имеет длину 3,2 т.п.н. и имеет четыре частично перекрывающиеся открытые рамки считывания, которые кодируют различные антигены. Неповрежденный вирион представляет собой сферическую частицу с двойной оболочкой с оболочкой из поверхностного антигена гепатита B (HBsAg), внутренним нуклеокапсидом корового антигена (HBcAg) и активным ферментом полимеразой, связанным с одной молекулой двухцепочечной ДНК HBV.Существует значительная вариабельность нуклеотидной последовательности, и вирус можно разделить на восемь различных генотипов в зависимости от степени вариабельности. Однако их клиническое значение все еще не определено.
ИммунизацияИммунизация
Эффективные вакцины для профилактики ВГВ доступны в Соединенных Штатах с 1982 года.Вакцина против гепатита В была описана как первая эффективная противоопухолевая вакцина, и Всемирная организация здравоохранения продвигает ее использование в качестве рутинной помощи во всем мире с 1997 года. Предконтактная профилактика является весьма успешной. Он достигает двойной цели — индивидуальной защиты и коллективного иммунитета. Ранние стратегии, нацеленные на группы высокого риска (например, подростков и молодых людей), не увенчались успехом из-за отсутствия мотивации у представителей этой возрастной группы обращаться за профилактической помощью.Соответственно, универсальная вакцинация против ВГВ рекомендована для младенцев Американской академией педиатрии с 1991 года и привела к снижению числа новых случаев гепатита В в США на 90%.
Для невакцинированных лиц с задокументированным контактом с гепатитом B, постконтактная профилактика состоит из однократной дозы иммуноглобулина гепатита B (HBIG), вводимой внутримышечно, с последующей немедленной вакцинацией против HBV.
Три рекомбинантные вакцины против гепатита B доступны в США: Engerix-B, Recombivax HB и Heplisav B.
Engerix B: Для первичной вакцинации лиц в возрасте 19 лет и младше Engerix-B вводится в дозе 10 мкг. Первоначальная доза повторяется через один и шесть месяцев, всего три приема. Для людей старше 20 лет доза составляет 20 мкг и вводится по тому же графику.
Реокомбивакс В: доза Рекомбивакса-HB для младенцев в возрасте до 10 лет составляет 5 мкг. Дозировка повторяется через один и шесть месяцев, всего три приема. Подростки (в возрасте 11-15 лет) могут получать тот же режим ИЛИ получать 10 мкл (доза для взрослых), повторенные через четыре-шесть месяцев, всего две дозы.Для тех, кто старше 20 лет, доза составляет 20 мкг и повторяется через один и шесть месяцев, всего три приема.
Heplisav B: новейшая вакцина — Heplisav B. Она имеет два преимущества перед другими: для нее требуется всего две иммунизации (20 мкг) с интервалом в один месяц. Оказывается, он более иммуногенен, что дает 95% -ный уровень защиты. Признавая наличие существенных доказательств несоблюдения режима множественных доз, мы рекомендуем, когда это возможно, этот подход с двумя дозами вакцины.
Предварительный скрининг на анти-HBs не рекомендуется, за исключением взрослых пациентов, которые, вероятно, ранее подвергались воздействию, в том числе из групп высокого риска (например, потребителей инъекционных наркотиков, мужчин-гомосексуалистов). Поствакцинальное тестирование на анти-HBs для подтверждения сероконверсии обычно не рекомендуется, за исключением людей, которые находятся в группе риска из-за отсутствия ответа или продолжающегося воздействия. Бустерные дозы могут быть подходящими для пациентов из группы высокого риска, если титры анти-HBs ниже того, что считается защитным (10 МЕ / мл).Вакцину следует регулярно вводить всем лицам моложе 18 лет и взрослым, подверженным риску заражения. Его следует назначать новорожденным от HBV-инфицированных матерей вместе с гипериммунным B-глобулином (HBIg).
ПатофизиологияПатофизиология
Вирус гепатита В не является цитопатическим. Считается, что повреждение печени при хроническом гепатите B является иммунологически опосредованным.Тяжесть и течение заболевания не коррелируют с уровнем вируса в сыворотке крови. Считается, что антиген-специфические цитотоксические Т-клетки играют роль в повреждении клеток при гепатите В, но в конечном итоге они отвечают за клиренс вируса. Специфические цитокины, продуцируемые цитотоксическими и другими Т-клетками, также обладают противовирусным действием, способствуя выведению вируса без гибели клеток. Отсутствие сильного и специфического ответа цитотоксических Т-лимфоцитов CD8 + и вспомогательных Т-лимфоцитов CD4 + может привести к развитию хронической инфекции.Затем привлечение неспецифических Т-клеток приводит к хроническому воспалению низкого уровня и повреждению печени. Точно так же спонтанная сероконверсия от HBeAg к анти-HBeAb во время хронического гепатита B также является иммунологически опосредованной, что предполагает временное обострение заболевания, которое часто непосредственно предшествует клиренсу HBeAg.
Естественная историяЕстествознание
Гепатит B передается парентерально, при интимном личном контакте и перинатально.В группу риска входят потребители инъекционных наркотиков, дети матерей с ВГВ, мужчины, практикующие секс с мужчинами, пациенты, находящиеся на гемодиализе, и те, кто контактирует с кровью или продуктами крови.
Инкубационный период от 45 до 160 дней. Острое заболевание обычно протекает в легкой форме, особенно у детей. Симптомы неспецифичны. У некоторых из взрослых возникает желтуха; и гепатит может быть молниеносным от 0,1% до 0,5%. Симптомы могут длиться несколько дней, за исключением более серьезных случаев, когда симптомы, включая сильную усталость, могут длиться несколько недель.
Признаки физического осмотра неспецифичны, но могут включать легкое увеличение и легкую болезненность печени, легкую спленомегалию и заднюю шейную лимфаденопатию у 15–20% пациентов. Фульминантное заболевание (острая печеночная недостаточность) проявляется изменением психического статуса (энцефалопатия) и коагулопатией.
Риск развития хронической инфекции, определяемый как сохранение HBsAg в крови более 6 месяцев, зависит от возраста и иммунной функции пациента на момент первоначальной инфекции.Девяносто процентов инфицированных новорожденных, 30% детей младше 5 лет и 10% взрослых прогрессируют до хронической инфекции. Из этих 15–40% в течение жизни развиваются последствия, связанные с гепатитом B. Люди с хронической инфекцией спонтанно удаляют поверхностный антиген со скоростью 0,5% в год. У пациентов с хроническим гепатитом В могут развиться внепеченочные проявления, включая артралгии, кожно-слизистый васкулит, гломерулонефрит и узелковый полиартериит. Гломерулонефрит гепатита B чаще встречается у детей и обычно характеризуется нефротическим синдромом с незначительным снижением функции почек.Узелковый полиартериит возникает в основном у взрослых и характеризуется внезапным и тяжелым началом гипертонии, почечной недостаточности и системного васкулита с артериитом сосудов почек, желчного пузыря, кишечника или головного мозга. Редкими внепеченочными проявлениями являются смешанная эссенциальная криоглобулинемия, перикардит и панкреатит.
ДиагностикаДиагностика
Существует 6 лабораторных тестов, важных для диагностики гепатита B:
- Поверхностный антиген гепатита B (HBsAg)
- Антитело к поверхностному антигену гепатита B (anti-HBs)
- Антитело к коровому антигену гепатита В (anti HBc)
- е антиген гепатита В (HBeAg)
- Антитело к HBeAg: (анти HBe)
- Вирус гепатита B (ДНК HBV)
Острая инфекция
Во всем мире наиболее распространенным способом заражения гепатитом В является инфицированная мать.Это называется вертикальной передачей. В противном случае инфекции чаще всего возникают в подростковом и взрослом возрасте, что называется горизонтальной передачей. Острый гепатит B диагностируется путем выявления как HBsAg, так и антител к HBc (IgM). Если тестирование откладывается, HBsAg мог исчезнуть. В этом случае для постановки диагноза достаточно наличия только анти-HBc (IgM). Основные антитела IgM теряются в течение 6–12 месяцев после начала болезни. Биохимически уровни сывороточной аланинаминотрансферазы (АЛТ) и аспартатаминотрансферазы (АСТ) могут повышаться до 500–5000 Ед / л и падать после острой фазы инфекции.Уровень билирубина в сыворотке редко превышает 10 мг / дл, уровень щелочной фосфатазы обычно в норме или повышен лишь незначительно. За исключением молниеносных случаев протромбиновое время обычно нормальное или слегка повышенное (например, от 1 до 3 секунд). Уровень сывороточного альбумина нормальный или минимально пониженный. Анализ периферической крови может показать умеренную лейкопению с относительным лимфоцитозом или без него. Потеря HBsAg и развитие HBsAb означают выздоровление от острой инфекции и развитие иммунитета (рис.1).
На рисунке 1 показана серологическая динамика типичного острого гепатита B.
Рисунок 1: Серологическое течение острого гепатита B.
Хроническая инфекцияХроническая инфекция
Серологическим признаком хронического гепатита B является наличие HBsAg и анти-HBc, но отсутствие анти-HBs.У людей с хроническим заболеванием будут разные уровни циркулирующей ДНК HBV и воспаление печени. Серология таких хронических инфекций представлена на Рисунке 2.
Рисунок 2 . Серологическое течение хронического гепатита В.
Удобный способ интерпретации результатов лабораторных исследований показан во вставке 1.
Вставка 1: Серологические образцы гепатита B
Иммунитет
Естественное воздействие
- HBsAg отрицательный
- HBcAb положительный (или отрицательный, если отстает во времени)
- HBsAb положительный
Вакцинация
- HBcAb отрицательный
- HBsAb положительный
- HBsAg отрицательный
Острая инфекция
- IgM HBcAb положительный
- HBsAb отрицательный
- HBeAg может быть положительным или отрицательным, в зависимости от времени
- HBsAg положительный
- ДНК-положительный HBV (обычно)
Хроническая инфекция
- lgG HBcAb положительный
- HBsAb отрицательный
- HBsAg положительный
- Положительный результат на ДНК ВГВ (обычно)
HBcAb, ядерное антитело против гепатита В; HBsAb, поверхностные антитела к гепатиту В; HBeAg, е антиген гепатита В; HBsAg, поверхностный антиген гепатита В; ВГВ, вирус гепатита В; lg, иммуноглобулин.
© 2005 Фонд клиники Кливленда.
Хронический гепатит В
Хронический гепатит B определяется как сохранение HBsAg в сыворотке крови не менее 6 месяцев. Клиническое течение гепатита B значительно варьируется между людьми и у одного и того же человека с течением времени. Ниже описаны признанные стадии хронического гепатита B:
Терминология различных состояний хронического гепатита B сбивает с толку, непонятна и несовершенна.Некоторых людей сложно классифицировать. В конце концов, мы чаще всего заинтересованы в выявлении людей с хроническим гепатитом B, у которых или может развиться прогрессирующее повреждение печени, и, следовательно, кому будет полезно противовирусное лечение. Количество вируса в сыворотке не является точным предиктором того, кто может иметь активную болезнь печени. Например, ребенок с вертикально приобретенным гепатитом B часто имеет чрезвычайно высокую вирусную нагрузку (иммунная толерантность; фаза 1), но нормальные тесты печени и нормальная гистология печени.Следующая классификация, разработанная Европейской ассоциацией изучения печени, представляет собой полезную схему.
Важно отметить, что Фаза 5 («разрешенная инфекция HBV») не должна интерпретироваться как отсутствие фрагментов вируса гепатита B. После заражения большинство людей навсегда скрывают HBVDNA в ядре клетки гепатоцита, либо интегрированную в ДНК хозяина, либо в виде cccDNA, отдельно стоящей «мини-хромосомы». При обстоятельствах, описанных ниже, реактивация гепатита B (возврат к фазе 2 или 4) может иметь серьезные последствия.
Пациенты с иммунореактивным HBeAg-положительным хроническим гепатитом B (фаза 2) и HBeAg-отрицательным хроническим гепатитом B (фаза 4), скорее всего, будут иметь активное повреждение печени и, следовательно, будут кандидатами на противовирусное лечение.
Спонтанная потеря HBeAg происходит со скоростью от 8% до 12% в год и связана с уменьшением ДНК HBV. Потеря HBsAg происходит реже (<1% / год). Хронически инфицированные люди без активного заболевания печени или вирусной репликации (неактивные носители) обычно имеют доброкачественное течение с меньшей вероятностью прогрессирования до цирроза.У тех, у кого сохраняется активная репликация вируса с высоким уровнем ДНК HBV и HBeAg в сыворотке, часто наблюдается прогрессирующее повреждение печени, и могут развиться цирроз и терминальная стадия заболевания печени. Преходящее обострение болезни часто предшествует ремиссии.
Потеря HBeAg не всегда сопровождается необратимым излечением заболевания, и могут возникать обострения болезни, особенно если пациент лечится стероидами или другими иммунодепрессантами. Пациенты, которые возвращаются к хроническому HBeAg-положительному статусу, имеют тенденцию к развитию цирроза значительно чаще, чем у тех, кто остается HBeAg-отрицательным.HBe Ag-отрицательные люди с признаками продолжающегося воспаления печени, как правило, имеют более высокий риск прогрессирования заболевания, чем пациенты, которые являются HBeAg-положительными.
Гепатоцеллюлярная карцинома: Хроническая инфекция HBV связана с десятикратным увеличением риска развития гепатоцеллюлярной карциномы (ГЦК). Этот риск еще больше увеличивается в условиях продолжающегося воспаления: у пациентов с HBsAg и HBeAg риск увеличивается до 60 раз по сравнению с населением в целом.Наибольшему риску подвержены пожилые мужчины с циррозом печени и люди с коинфекцией гепатита С. В регионах, где HBV является эндемическим заболеванием, HCC является ведущей причиной смерти от рака.
УЗИ (с альфа-фетопротеином или без него) дважды в год рекомендуется для следующих лиц с хроническим гепатитом B:
- Цирроз
- Чернокожие мужчины азиатского или африканского происхождения старше 40 лет
- Азиатские женщины старше 50 лет
- Родственник первой степени родства с ГЦК
- Коинфекция ВИЧ или гепатитом D
При отсутствии доступа к ультразвуку можно использовать только альфа-фетопротеин.HCC.
УходЛечение
При типичном остром гепатите B лечение является поддерживающим. Нет четких доказательств того, что ранняя терапия противовирусными препаратами при остром гепатите B снижает риск хронического заболевания или ускоряет выздоровление. Большинство пациентов с острым желтушным гепатитом B выздоравливают без остаточных повреждений или хронического гепатита. Эти люди должны пройти повторное тестирование на уровни HBsAg и ALT, чтобы определить, произошла ли сероконверсия и клиренс поверхностного антигена.Исключение составляет человек с молниеносным гепатитом B, которому предполагается трансплантация печени. В таких случаях обычно начинается противовирусная терапия.
Следующие ситуации требуют начала противовирусной терапии гепатита В:
- Фульминантный гепатит В, у которого предполагается трансплантация печени
- Иммунореактивный HBeAg-положительный хронический гепатит B (фаза 2)
- HBeAg-отрицательный хронический гепатит (4 фаза)
- Беременные, вирусная нагрузка которых превышает 200000 МЕ
- Те, кто подвержен риску реактивации гепатита В.
Доступные в настоящее время противовирусные препараты не излечивают гепатит В и даже не ускоряют потерю HBsAg. Терапия способна подавить репликацию вирусов и воспаление печени, а также предотвратить или обратить вспять фиброз печени. Терапия также может вызвать сероконверсию из фазы 2 (HBeAg-положительный иммунореактивный хронический гепатит) в более спокойную фазу 3 (HBe Ag-отрицательный неактивный носитель).
Чаще всего решение о лечении хронического гепатита принимается без биопсии печени, хотя биопсия дает наиболее точную информацию о некровоспалительной активности и фиброзе.
Пациентам с циррозом рекомендуется противовирусное лечение, если имеется поддающаяся измерению ДНК HBV независимо от ферментов печени и статуса HBeAg. Этот подход подтверждается несколькими исследованиями, которые показали снижение скорости развития прогрессирующего заболевания печени или осложнений у пролеченных пациентов.
Беременные женщины проходят скрининг на гепатит B, поэтому новорожденным от HBsAg-положительных матерей можно сделать активную иммунизацию и HBIG, что снизит вероятность вертикальной передачи.Недавно было показано, что дополнительная защита обеспечивается новорожденным, если матери с очень высокой вирусной нагрузкой (> 200 000 МЕ) получают лечение и NA в течение третьего триместра для снижения вирусной нагрузки.
Реактивация Гепатит B неожиданно часто встречается у восприимчивых людей, проходящих курс лечения рака или ревматологических заболеваний. Все пациенты, которым назначают цитотоксическую, иммуносупрессивную или иммуномодулирующую терапию, должны быть проверены на HBsAg и анти-HBc.Следует предусмотреть превентивное лечение нуклеозидами.
Руководство AASLD позволяет проводить тщательный мониторинг (частые АЛТ, ДНК HBV, HBsAg) тех, у кого есть только анти-HBc, но не получающих анти-CD-20 терапию или трансплантацию стволовых клеток. Поскольку реактивация гепатита B может быть связана с тяжелым заболеванием, печеночной декомпенсацией и высокой вероятностью смерти, мы рекомендуем вести HBsAg- / anti-HBc-положительные методы так же, как и HBsAg-положительные.
Фармакологическое лечение
Шесть противовирусных препаратов были одобрены U.S. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) для лечения гепатита B. В США обычно используются только 3, все нуклеозидные или нуклеотидные аналоги (NA)
- Тенофовир алафенамид 25 мг в сутки (взрослые)
- Тенофовир дизосопроксил 300 мг в сутки (взрослые)
- Энтекавир от 0,5 до 1 мг в день (взрослые)
Каждый из них выводится почками, поэтому тем, у кого нарушена скорость клубочковой фильтрации, требуется снижение дозы. Каждый из них приводит к значительному снижению вирусной нагрузки, а устойчивость к вирусам встречается редко.Оптимальная продолжительность лечения продолжает оставаться предметом дискуссий для пациентов с гепатитом B фазы 2, у которых произошла сероконверсия с HBeAg-положительной на анти-HBe-положительные. Некоторые могут оставаться неактивными носителями, если лечение NA прекращается через 6-12 месяцев после сероконверсии HBe. Поскольку многие обостряются, лечащие врачи часто не хотят останавливать НА. Существует больше единодушного мнения о необходимости постоянной терапии NA для пациентов с гепатитом B фазы 4. Исключение из пожизненного лечения сделано для тех немногих счастливчиков, которые становятся HBsAg-отрицательными и остаются таковыми в течение шести месяцев.
Другие НА страдают появлением вирусной устойчивости и используются редко.
Терапия интерфероном альфа для лечения гепатита B одобрена FDA с 2005 года. Потому что она требует подкожных инъекций и связана с множеством побочных эффектов. Основные побочные эффекты интерферона включают усталость, мышечные боли, лихорадку, депрессию и раздражительность. Необычные серьезные побочные эффекты включают обострение депрессии, психоза, почечной и сердечной недостаточности, бактериальных инфекций и индукции аутоиммунитета.У пациентов с положительным ответом на терапию интерфероном часто развиваются обострения болезни с повышением уровня АЛТ в сыворотке до уровней в два-три раза по сравнению с исходным уровнем до наступления нормализации. Из-за возможности того, что обострение заболевания печени может привести к декомпенсации, использование интерферона у пациентов с циррозом не рекомендуется. Длительные курсы лечения интерфероном не имеют себе равных в достижении потери HBsAg. Тем не менее, сегодня это лечение редко используется в США.
Хотя введение аналогов нуклеотидов или нуклеозидов представляет собой значительный прогресс в лечении хронического гепатита B, остается много вопросов относительно оптимальной дозировки, продолжительности и возможных комбинаций для предотвращения резистентности и увеличения долгосрочного подавления.Эти новые методы лечения, включая новые и более эффективные противовирусные препараты, в сочетании с агрессивной всемирной политикой вакцинации вселяют надежду на то, что однажды гепатит B будет под контролем. Действительно, в 2015 году Всемирная организация здравоохранения разработала реалистичный план ликвидации гепатита В во всем мире к 2030 году.
Другие рекомендации по лечению
Накоплено немало доказательств того, что пациенты с хроническим гепатитом В, получающие липофильные статины (аторвастатин, симвастатин, ловастатин, флувастатин, церивастатин и питавастатин), имеют значительно более низкий риск развития гепатоцеллюлярной карциномы.Такие средства следует рассматривать даже при отсутствии повышенных липидов.
РезюмеСводка
- Гепатит В встречается во всем мире. Заболеваемость особенно высока в Азии, Африке к югу от Сахары, южной части Тихого океана, Южной Америке, на Ближнем Востоке и в Арктике.
- Самый распространенный путь передачи гепатита В во всем мире — от матери к младенцу.Гепатит В передается преимущественно парентерально, при интимном личном контакте и перинатально.
- В группу риска входят потребители инъекционных наркотиков, дети матерей с ВГВ, мужчины, практикующие секс с мужчинами, пациенты, находящиеся на гемодиализе, и лица, подвергшиеся воздействию зараженной крови или продуктов крови.
- Большинство острых инфекций протекает бессимптомно. При наличии симптомы широко варьируются по степени тяжести — от бессимптомной субклинической инфекции до молниеносного смертельного исхода.
- Риск развития хронической инфекции (или состояния носительства) зависит от возраста и иммунной функции пациента на момент первоначальной инфекции.
- Вирусные и иммунные маркеры обнаруживаются в крови, и характерные паттерны антиген-антитело со временем развиваются. Первым обнаруживаемым вирусным маркером является HBsAg, за которым следуют HBeAg и ДНК HBV.
- Эффективные вакцины против ВГВ, определяемые как обеспечивающие защиту от ВГВ выше 90%, доступны в Соединенных Штатах с 1982 года. Вакцина против гепатита В была описана как первая эффективная противораковая вакцина, и Всемирное здравоохранение способствовало ее использованию. Организация повседневной медицинской помощи по всему миру с 1997 года.
- При остром гепатите В лечение является поддерживающим. Хотя было опубликовано несколько серий случаев, нет четких доказательств того, что ранняя терапия противовирусными препаратами при остром гепатите B снижает риск хронического заболевания или ускоряет выздоровление. При хроническом гепатите В назначается терапия для подавления репликации вируса и предотвращения прогрессирования заболевания печени. Многие программы лечения доказали свою эффективность и были одобрены FDA и другими государственными учреждениями здравоохранения по всему миру
Благодарность: Эта глава основана на предыдущей версии, написанной Робертом О’Ши, MD
Рекомендуемое чтениеРекомендуемая литература
- Terrault N, Lok A, McMahon J и др.Обновленная информация о профилактике, диагностике и лечении хронического гепатита B: руководство AASLD 2018 по гепатиту B. ГЕПАТОЛОГИЯ, ТОМ. 67, НЕТ. 4, 2018; 1560 (https://www.aasld.org/sites/default/files/2019-06/HBVGuidance_Terrault_et_al-2018-Hepatology.pdf)
- Cox, A.L., Эль-Сайед, M.H., Kao, JH. et al. Прогресс в достижении целей ликвидации вирусного гепатита. Nat Rev Gastroenterol Hepatol 17, 533–542 (2020). https://doi.org/10.1038/s41575-020-0332-6
- Вопросы и ответы по гепатиту B для медицинских работников (https: // www.cdc.gov/hepatitis/hbv/hbvfaq.htm)
Растворимые иммунные маркеры в различных фазах хронической вирусной инфекции гепатита В
Популяция пациентов
В это кросс-секционное исследование были включены триста тридцать три европейских пациента с персистирующей инфекцией HBV, не получающих противовирусную терапию (Таблица 1).
Таблица 1 Исходные характеристики и факторы, однозначно дифференцирующие пациентов на разных этапах хронической инфекции HBV на основе дисперсионного анализа (непрерывные значения) и анализа хи-квадрат (дискретные значения).Набор пациентов проводился в амбулаторной клинике Ганноверской медицинской школы, Германия. Сто тридцать четыре пациента были HBeAg-положительными, а 199 — HBeAg-отрицательными. В их число вошли 190 мужчин и 143 женщины со средним возрастом 32 года (мин. 1, макс. 69 лет). Ни один из включенных лиц не был коинфицирован вирусом гепатита δ (HDV), вирусом гепатита C (HCV) или вирусом иммунодефицита человека (ВИЧ). Другими критериями исключения были терминальная стадия печеночной недостаточности, алкоголизм, аутоиммунные расстройства, иммуносупрессивное лечение и злокачественные новообразования.Пациенты были разделены в зависимости от фазы хронической инфекции HBV или гепатита, определенной в соответствии с EASL 2 :
HBeAg-положительная хроническая инфекция (EPI, n = 45)
HBeAg-положительный хронический гепатит (EPH, n = 89),
HBeAg-отрицательная хроническая инфекция (ENI, n = 88)
HBeAg-отрицательный хронический гепатит (ENH, n = 63)
HBeAg-отрицательная хроническая инфекция, высокая репликация (ДНК HBV> 20 000, АЛТ в норме) (ENI-HR, n = 48).
Высокий репликативный статус при HBeAg-отрицательной хронической инфекции (ENI-HR) оценивался, когда уровни ДНК составляли от 2000 до 20000 МЕ / мл как минимум в двух последовательных временных точках с уровнями АЛТ меньше или равными верхнему пределу нормы ( ULN).
Для анализа 2 и субпопуляция пациентов с хронической инфекцией HBV (n = 39 из 333) и пациентов с острой инфекцией HBV (n = 10) или пациентов с подавленной ДНК HBV под аналогами нуклеоз (т) идов. (NA) терапия была включена.
Количественное определение HBsAg в сыворотке
Анализ Abbott ARCHITECT (Abbott Diagnostics, Abbott Park, IL) использовали для количественного определения уровней HBsAg в сыворотке.
Динамический диапазон теста 0,05–250 МЕ / мл. Образцы разбавляли 1: 100 в сыворотке лошади, и если уровни HBsAg были> 250 МЕ / мл, образцы повторно тестировали при разведении 1: 500 и 1: 1000, соответственно. Образцы с уровнем HBsAg <0,05 МЕ / мл были повторно протестированы без предварительного разбавления. Результаты представлены в МЕ / мл.
Измерение ДНК HBV
ДНК HBV в сыворотке количественно определяли с использованием COBAS AmpliPrep / COBAS TaqMan (Roche Diagnostics, Mannheim, Germany) и TaqMan Universal Master Mix (Applied Biosystems, Foster City, CA) с пределами обнаружения 12 МЕ. / мл и 50 МЕ / мл соответственно.Результаты определения ДНК HBV выражаются в МЕ / мл.
Генотипирование HBV
Генотипирование HBV было оценено у 254 пациентов. ДНК экстрагировали из 200 мкл сыворотки с использованием высокочистой вирусной нуклеиновой кислоты K15it (Roche Diagnostics, Mannheim, Germany) в соответствии с протоколом производителя. Генотип HBV определяли с помощью модифицированного ПЦР-анализа RFLP с амплифицированной ДНК HBV с использованием вложенной ПЦР, как описано ранее 15 . Отобранные последовательности сравнивали с Национальным центром биотехнологической информации GenBank и сравнивали с описанными прототипами HBV (номер доступадля: HBV-A Z72478; HBV-B D00329; HBV-C X01587; HBV-D V01460; HBV-E X75658; HBV-G AF160501). Последовательность S HBV и соответствующие ссылочные последовательности были выровнены с помощью CLC Main Workbench 6 (CLCBio, Орхус, Дания). Генетическое расстояние было оценено также с использованием CLC Main Workbench 6. Передискретизация и реконструкция начальной загрузки были выполнены 1000 раз.
Количественное определение растворимых иммунных медиаторов (цитокинов и хемокинов)
Концентрации следующих SIM были измерены в сыворотке / плазме с использованием мультиплексной технологии на основе Luminex.У всех пациентов CXCL10 (IP-10), IL-2, IL-4, IL-7, IL-10, IL-12p70 (IL-12), IL-16, IL-17, интерферон-γ, CCL4 (MIP -1β), TNF-α, TGF-β1, -2, -3 были измерены, и в субпопуляции были оценены дополнительные концентрации для: IL-1β, IL-1R, IL-5, IL-6, IL-8, IL -9, IL-13, IL-15, эотаксин, FGF-β2, G-CSF, GM-CSF, MCP-1, CCL3, PDGF-BB, RANTES, VEGF, IL-1α, IL-2Rα, IL-3 , IL-12p40, IL-18, CTACK, GRO-α, HGF, IFN-α2, LIF, MCP-3, M-CSF, MIF, MIG, β-NGF, SCF, SCGF-β, SDF-1α, IL -2, TNF-β, TRAIL, sCDL40.
Анализы Bio-Plex (Bio-Rad, Hercules, США) содержат стандартные концентрации каждого аналита, а расчет соответствующих стандартных кривых позволяет точно определить концентрации интересующего белка.Анализ проводили в соответствии с протоколом производителя. Вкратце, стандартный лиофилизированный цитокин ресуспендировали в стандартном разбавителе. Серии серийных разведений были выполнены для создания стандартных кривых для каждого интересующего цитокина, хемокина и фактора роста. Смесь гранул, специфичную для цитокинов, хемокинов, инкубировали в течение 30 мин при комнатной температуре с 50 мкл стандартных образцов или образцов сыворотки, разбавленных в разбавителе образцов (разведение 1: 2). Несколько этапов промывки выполняли с использованием 100 мкл промывочного буфера на лунку с использованием автоматической промывки магнитных шариков (Bio-Rad).Для количественного определения TGF-β1-3, в соответствии с протоколом производителя, была введена стадия подкисления путем добавления 5 мкл HCl к образцам сыворотки на 15 мин, чтобы высвободить TGF-β из связывающих белков. После стадии нормализации с NaOH до pH 7 все образцы добавляли к смеси шариков и обрабатывали по тому же протоколу, что и все другие аналиты. После добавления смеси вторичных биотинилированных антител в течение 30 минут при комнатной температуре и еще трех стадий промывки SAPE добавляли в течение 10 минут при комнатной температуре (разведение 1: 100).
После трех заключительных этапов промывки гранулы ресуспендировали в 125 мкл буфера для анализа, собирали и анализировали с помощью программного обеспечения BioPlex Manager 6.0.
In-vitro Пептидная стимуляция и внутриклеточное окрашивание (ICS)Для изучения влияния IL-12 на Т-клетки размороженные PBMC от двух пациентов с EPI стимулировали в течение 10 дней 2,5 мкг / мл перекрывающихся ядер HBV пептидов (OLP) (Генотип D, Proimmune, Великобритания) в присутствии 10 нг / мл rhIL-12 (Miltenyi Biotech).41 базовый OLP HBV был разделен на 2 пула; Коровые пептиды №1 HBV, включая 20 пептидов, и коровые пептиды №2 HBV, включая 21 пептид. К культурам добавляли 5 ед / мл rhIL-2 (Invitrogen Life Technologies) на 4 и 8 дни. Клетки повторно стимулировали на 10 день теми же самыми OLP HBV и rhIL-12 в течение 6 часов. 2 мкг / мл брефельдина А (Sigma-Aldrich) добавляли через 1 час рестимуляции. Для окрашивания клеточной поверхности PBMC окрашивали CD3 (Biolegend), CD14 (BD Bioscience), CD19 (BD Bioscience), CD4 (BD Bioscience) и CD8 (Biolegend).Мертвые клетки исключали с помощью набора для окрашивания клеток Aqua (Life technologies). После фиксации и пермеабилизации PBMC с помощью набора буферов для окрашивания Foxp3 / транскрипционного фактора (Ebioscience / Thermofisher) их окрашивали на IFN-γ (BD Bioscience) и TNF (Biolegend) в течение 30 мин. Образцы были получены с использованием BD LSR Fortessa (BD Biosciences), а данные были проанализированы в FlowJo версии 9.9.4 (Treestar).
Статистический анализ
Статистический анализ выполнялся с использованием программного обеспечения SPSS версии 21 (SPSS Inc., Чикаго, Иллинойс). Значения P <0,05 считались статистически значимыми. Если не указано иное, все упомянутые значения представляют собой медианное значение и доверительный интервал 10–90%. Корреляция была проверена с помощью теста корреляции Спирмена.
Был рассчитан критерий хи-квадрат для сравнения дискретных переменных. Для одномерного анализа мы применили U-критерий Манна-Уитни для непрерывных данных. Многовариантный анализ выполняли с помощью ANOVA Краскела-Уоллиса. Анализ многомерной логистической регрессии проводился с использованием теста отношения правдоподобия для обратного отбора.
Для предотвращения систематической ошибки, связанной с разными типами образцов (сыворотка / плазма), сначала были рассчитаны медианные значения. Отношение медианы результатов в плазме к медиане результатов в сыворотке умножали на каждый результат в сыворотке для каждого цитокина. Концентрации SIM были логарифмированы (log10) для использования параметрической математики.
Для анализа цитокиновых паттернов был проведен анализ выбросов. Для оценки мы использовали 50-кратный медианный порог и 1/50 медианный порог в каждой группе.Все параметры, не попавшие в этот диапазон, были удалены для последующего анализа.
Этическое одобрение
Это ретроспективное исследование было проведено в соответствии с руководящими принципами Хельсинкской декларации, принципами надлежащей клинической практики и стандартами местного комитета по этике. Все пациенты дали информированное согласие на анализ параметров, оцениваемых в хранимых образцах крови, взятых во время рутинной диагностики. Данные были проанализированы анонимно.Местный этический комитет Ганноверской медицинской школы одобрил ретроспективное анонимное повторное тестирование образцов пациентов и анонимный анализ данных пациентов.
Диагностика, мониторинг и скрининг вирусных гепатитов
- 5 выявленных форм вирусного гепатита поражают около 400 миллионов человек во всем мире.
- Пандемия вирусного гепатита является причиной примерно 1,4 миллиона смертей в год. 47% связаны с вирусом гепатита В и 48% — с вирусом гепатита С.
- Вирусные гепатиты A и E — это инфекции, передаваемые через пищу и воду, которые могут вызывать острые вспышки в общинах с небезопасной водой и плохой санитарией.
- Более 95% людей, живущих с хроническим гепатитом, не знают, что у них он есть.
- В 2015 году лечение получали менее 1% людей с хроническим гепатитом.
Источники:
Определение
Гепатит — это воспаление печени. Острая инфекция некоторых типов гепатита может привести к хронической инфекции, потенциально вызывая заболевания печени, включая цирроз и рак.Он может развиться в результате алкоголизма или приема лекарств, но чаще всего вызывается вирусной инфекцией . Было идентифицировано пять различных вирусов гепатита: A, B, C, D и E. Вместе они поражают около 400 миллионов человек во всем мире . Гепатиты A, B и C — самые распространенные типы.
Гепатиты B и C, которые могут привести к хроническому гепатиту, особенно распространены . Они являются ведущими причинами рака печени, цирроза печени и смертности 1,2,3 .Цирроз вследствие гепатита — одна из основных причин трансплантации печени 2 .
Пути передачи зависят от типа вирусного гепатита (см. Таблицу). Существуют вакцины против HAV и HBV; в противном случае гигиена и просвещение способствуют профилактике. Во время острой фазы гепатит может вызывать «гриппоподобные» симптомы (например, тошноту, рвоту), желтуху, белый стул и темную мочу. Тем не менее, вирусный гепатит в основном протекает бессимптомно, поэтому большинство людей не знают, что они заражены .Вот почему вирусный гепатит получил название «тихая эпидемия , ».
Средства потенциальной передачи вирусного гепатита
означает | HAV | HBV | ВПЦ | HDV | HEV |
| Загрязнение пищевых продуктов и воды | наиболее распространенный | № | № | Инфекция HDV связана с инфекцией HBV. | наиболее распространенный |
| Кровь напр. через переливание; загрязненные инструменты в медицинских учреждениях; совместное использование игл среди потребителей наркотиков | № | да | да | редкий | |
| Секс с инфицированным | редкий | да | да | редкий | |
| Передача от матери к ребенку | редкий | да | да | редкий |
Диагностика
Гепатит может быть трудно диагностировать , потому что он может протекать бессимптомно или симптомы могут быть неспецифическими.
- неспецифические или отсутствующие симптомы (90% случаев):
- боль в правом подреберье — лихорадка
- тошнота и рвота — артралгия
- крапивница
- Специфический симптом (≤ 10% случаев) 4 :
- Тяжелая форма: молниеносный гепатит
- Клинические признаки: печеночная энцефалопатия
- биологических признаков: уровень протромбина (<50%); уровень трансаминаз не коррелирует с тяжестью фульминантного гепатита
Когда у пациента есть подозрение на гепатит , знание его биографии часто помогает клиницистам сориентировать свой диагноз . 1,2 К группе повышенного риска относятся:
- ВИЧ-инфицированные люди подвергаются более высокому риску заражения как гепатитом В, так и С. По оценкам, ¼ ВИЧ-инфицированных в США также инфицированы ВГС 2
- Мужчины, практикующие секс с мужчинами 2
- Потребители инъекционных наркотиков 2
- Люди в ЛПУ и исправительных учреждениях 2
- Медицинские работники 2
- Большинство людей из стран с низким уровнем ресурсов заразятся гепатитом А в детстве 1,2
- Жители Азии и островов Тихого океана подвержены более высокому риску заражения гепатитом В 2
Поскольку разные типы гепатита вызывают сходные симптомы во время острой фазы, серологические тесты важны для определения типа вируса и времени его заражения.После получения результатов серологического исследования (и, возможно, проведения биопсии печени для оценки степени тяжести) можно применять соответствующие меры лечения и лечения.
Вирусный гепатит: Краткое руководство по серологическим маркерам
Ситуация | Гепатит | Серологические маркеры |
| Острый гепатит | С Д E | Anti-HAV IgM |
| Хронический гепатит | В С | HBsAg / Anti-HBc, затем HBe Ag / Anti-HBe |
| Пренатальный скрининг на ВГВ | B | HBsAg: если HBsAg +: • Мать: отслеживается на HBe Ag / Anti-HBe и • Новорожденный: количественные анти-HBs после вакцинации |
| Группы риска | В С | Anti-HBc |
| Вакцинация против ВГВ | B | Предварительная вакцинация: количественное определение Anti-HBs Всего • если — → вакцинировать • if + → количественный HBsAg / Anti-HBc Всего после вакцинации: количественный anti-HBs Всего |
| Вакцинация против ВГА | А | Пациент> 30 лет: Всего анти-HAV • если — → вакцинировать |
Профилактика / Лечение
Профилактика
Заболеваемость вирусным гепатитом в мире неравномерна.Это в основном связано с отсутствием доступа к профилактическим мерам в группах населения с ограниченными ресурсами и странах . По этой причине глобальная политика ВОЗ по профилактике вирусного гепатита и борьбе с ним направлена на адаптацию ответных мер к конкретным национальным или региональным условиям 3 . В целом это согласуется с основными глобальными стратегиями здравоохранения. В отношении гепатита наиболее важными стратегиями профилактики являются всеобщий доступ к детской вакцинации против гепатита В ; улучшенная гигиена и практика в медицинских учреждениях и за их пределами; и скрининг .
Вакцинация: Имеются эффективные вакцины против гепатита А и В 2,3 . Вакцина против HBV также защищает от HDV, поскольку HDV поражает только те группы населения, которые уже инфицированы HBV.
- Универсальная вакцинация в детстве показывает очень хорошие результаты в сдерживании числа инфекций HBV.
- Вакцинация помогает снизить передачу от матери ребенку (основная передача HBV)
- Информационно-пропагандистские программы и программы вакцинации также являются частью сокращения распространения вируса среди взрослых, особенно среди групп риска.Вакцинация является обязательной для некоторых групп риска в некоторых странах
Гигиена: Правильная гигиена — важный метод профилактики всех типов вирусных гепатитов. Сюда входят:
- Чистая питьевая вода и гигиеническое обращение с пищевыми продуктами
- Правильная ручная стирка
- Безопасный секс
- Потребители инъекционных наркотиков: отказ от совместного использования игл и программы обмена игл
- Медицинские учреждения: основные меры инфекционного контроля; асептические методы; запрещение повторного использования игл и шприцев; методы безопасных инъекций
Скрининг : Скрининг людей из групп риска и продуктов крови помогает снизить распространение гепатита 2,3 .
Лечение
Лечение различных типов гепатита сильно различается, как и лечение острых и хронических заболеваний.
Гепатит А
Обычно проходит самостоятельно. Лечение симптомов включает отдых и устранение алкоголя.
Гепатит B
Острая инфекция HBV обычно не лечится у иммунокомпетентных взрослых, поскольку она проходит естественным путем.
Современные методы лечения хронического HBV 5 :
- Пегилированный интерферон альфа (Peg-IFN)
- Аналоги нуклеотидов (НА):
- Первая линия: Энтекавир (ETV), Тенофовир (TDF)
- Вторая линия: Адефовир, Телбивудин, Ламивудин
- Пересадка печени может рассматриваться при декомпенсированном циррозе
- Терапевтический мониторинг, рекомендуемый во время, в конце лечения и в период после окончания лечения
Гепатит C
Нет специального лечения острого гепатита C.
Референсное лечение хронического ВГС 6 :
- Генотип 1 (60% пациентов) Пегилированный интерферон-α + рибавирин + противовирусное средство прямого действия (боцепревир или телапревир)
- Другие генотипы: Peg IFN + рибавирин
- Продолжительность лечения: 48 недель для генотипа 1, 24 недели для других генотипов
- Промежуточный критерий для определения терапевтической эффективности: устойчивый вирусный ответ
- Продолжительность и эффективность терапии зависит от генотипа
- Необходимо проводить мониторинг лечения:
- В T0 перед началом терапии,
- Регулярно после нескольких недель терапии, обычно на 4, 12, 24, 36, 48 неделях и т. Д.
- В зависимости от генотипа, препаратов, вирусной реакции
- Новые процедуры тройной терапии станут , доступными в 2014 году 7 :
- PegIFN + RBV + Софосбувир или Симепревир
- Схемы без PegIFN также будут доступны в 2014 году 7 :
Гепатит D
Нет специального лечения острого HDV. См. Профилактику и лечение его вируса-помощника, HBV.
Гепатит E
Как правило, специального лечения острого гепатита E нет, хотя лечение рибавирином может быть эффективным. Пациентам с ослабленным иммунитетом может быть снижена иммуносупрессивная терапия. В противном случае лечение обычно направлено на облегчение признаков и симптомов.
Руководящие принципы
ССЫЛКИ
1) Информационные бюллетени ВОЗ: Гепатит A (№ 328), B (№ 204) и C (№ 164), июль 2013 г.
2) Веб-сайт CDC: http: // www.cdc.gov/hepatitis/
3) ВОЗ: Отчет о глобальной политике в области профилактики вирусного гепатита и борьбы с ним в государствах-членах ВОЗ. Июль 2013г.
4) Lefrère JJ, Lunel F, Marcellin P, Pawlotsky JM, Zarski JP. Руководство pratique des hépatites virales. MMI Ed, Paris, 1998.
5) Европейская ассоциация изучения печени. Руководство EASL по клинической практике: ведение хронической инфекции вируса гепатита В. 2012.
6) Европейская ассоциация изучения печени.Руководство EASL по клинической практике: лечение вирусной инфекции гепатита С. Редакция 2013 г.
7) Американская ассоциация по изучению заболеваний печени / Общество инфекционных болезней Америки. Рекомендации по тестированию, ведению и лечению гепатита. 14.02.2014
Этот сайт не является источником медицинских консультаций
Медицинское содержание этого сайта представлено в краткой форме, носит общий характер и предоставляется только в информационных целях.Он не предназначен и не рекомендуется использовать в качестве замены профессиональной медицинской консультации. Вы не должны использовать Медицинский контент этого Сайта для диагностики проблем или заболеваний, связанных со здоровьем или физической подготовкой. Всегда обращайтесь за советом к своему врачу или другому квалифицированному поставщику медицинских услуг относительно любого заболевания или лечения. Ничто, содержащееся на этом Сайте, не предназначено для медицинской диагностики или лечения. Он не должен использоваться врачами как единственный источник информации для принятия решений о назначении.Никогда не пренебрегайте медицинскими советами и не откладывайте их поиск из-за того, что вы прочитали на этом Сайте.
Вирусные маркеры гепатита
Нет примечаний к слайду
— вирус семейства Hepadnaviridae, HBV — самый маленький ДНК-вирус человека, несущий геном длиной всего 3200 нуклеотидов [4]. Частично двухцепочечная кольцевая ДНК содержит четыре перекрывающиеся открытые рамки считывания, кодирующие гены S (поверхность), C (ядро), P (полимераза) и X
Геном HBV состоит из кольцевой ДНК, но это необычно, потому что ДНК не является полностью двухцепочечной. Один конец полноразмерной цепи связан с вирусной ДНК-полимеразой. Длина генома составляет 3020–3320 нуклеотидов (для полной цепи) и 1700–2800 нуклеотидов (для короткой цепи).
Геном HBV состоит из кольцевой ДНК, но это необычно, потому что ДНК не является полностью двухцепочечной. Один конец полноразмерной цепи связан с вирусной ДНК-полимеразой. Длина генома составляет 3020–3320 нуклеотидов (для полной цепи) и 1700–2800 нуклеотидов (для короткой цепи).
Геном HBV состоит из кольцевой ДНК, но это необычно, потому что ДНК не является полностью двухцепочечной. Один конец полноразмерной цепи связан с вирусной ДНК-полимеразой. Длина генома составляет 3020–3320 нуклеотидов (для полной цепи) и 1700–2800 нуклеотидов (для короткой цепи).
C Seeger и W.S Mason, 2000 Биология вируса гепатита B Microbiol Mol Biol Rev.6415168
Существует общий групповой реактивный антиген (а).
Кроме того, он может содержать один из нескольких специфических антигенов подтипа (d, y, w и r). Изоляты
HB относятся как минимум к 8 генотипам (A-H).
, например генотип A (подтип adw) и генотип D (ayd).
Географическое расположение, например генотип A и D преобладает в США и Европе, а генотип B и C преобладает в Азии.
Клинический курс напр. генотип B связан с менее агрессивным поражением печени и меньшим HCC по сравнению с генотипом C.
, например генотип A (подтип adw) и генотип D (ayd).
Географическое расположение, например генотип A и D преобладает в США и Европе, а генотип B и C преобладает в Азии.
Клинический курс напр. генотип B связан с менее агрессивным поражением печени и меньшим HCC по сравнению с генотипом C.
, например генотип A (подтип adw) и генотип D (ayd).
Географическое расположение, например генотип A и D преобладает в США и Европе, а генотип B и C преобладает в Азии.
Клинический курс напр. генотип B связан с менее агрессивным поражением печени и меньшим HCC по сравнению с генотипом C.
, например генотип A (подтип adw) и генотип D (ayd).
Географическое расположение, например генотип A и D преобладает в США и Европе, а генотип B и C преобладает в Азии.
Клинический курс напр. генотип B связан с менее агрессивным поражением печени и меньшим HCC по сравнению с генотипом C.
Он предшествует повышению активности аминотрансфераз и появлению клинических симптомов на 2-6 недель.
Он остается повышенным на протяжении всей желтушной или симптоматической фазы заболевания.
Обычно она исчезает через 1-2 месяца после начала желтухи и редко сохраняется после 6 месяцев.
После первичного курса из 3 прививок через интервал в 1–4 месяца можно сдать анализ крови, чтобы установить, есть ли адекватный ответ. , который определяется как уровень антител к поверхностному антигену гепатита B (анти-Hbs) выше 100 мМЕ / мл.Такой полный ответ наблюдается примерно у 85–90% людей. [10]
Уровень антител от 10 до 100 мМЕ / мл считается плохой реакцией, и эти люди должны получить однократную ревакцинацию в это время, но не нуждаются в дальнейшем повторном тестировании. [10]
Людям, не отвечающим на лечение (уровень антител к Hbs ниже 10 мМЕ / мл), следует пройти тестирование, чтобы исключить текущую или прошлую инфекцию гепатита B, и им должен быть проведен повторный курс из 3 прививок с последующим повторным тестированием через 1–4 месяца после второй вакцинации. курс.Те, кто все еще не отвечает на второй курс вакцинации, могут отреагировать на внутрикожное введение [11] или на высокую дозу вакцины [12], или на двойную дозу комбинированной вакцины против гепатита А и В. [13]. Тем, кто все еще не отвечает, потребуется иммуноглобулин против гепатита В (HBIG), если они в дальнейшем будут подвергаться воздействию вируса гепатита В. [10]
Плохие ответы в основном связаны с возрастом старше 40 лет, ожирением и курением [14], а также с алкоголиками, особенно с запущенным заболеванием печени.[15] Пациенты с ослабленным иммунитетом или на почечном диализе могут реагировать хуже и требовать больших или более частых доз вакцины. [10] По крайней мере, одно исследование предполагает, что вакцинация против гепатита В менее эффективна у пациентов с ВИЧ. [16]
В настоящее время считается, что вакцина против гепатита В обеспечивает бессрочную защиту. Однако ранее считалось и предполагалось, что вакцинация обеспечит эффективное покрытие только на период от пяти до семи лет [17] [18], но впоследствии было признано, что долгосрочный иммунитет происходит из иммунологической памяти, которая сохраняется дольше потери антител. У успешно вакцинированных иммунокомпетентных людей не требуется последующее тестирование и введение бустерных доз.[19] [20] Следовательно, с течением времени и более продолжительным опытом защита была продемонстрирована в течение как минимум 25 лет у тех, кто продемонстрировал адекватную первоначальную реакцию на первичный курс вакцинации, [21] и в руководствах Великобритании теперь предлагается, что для Первым респондентам, которым требуется постоянная защита, например медицинским работникам, рекомендуется однократная ревакцинация через 5 лет [10].
Корневой антиген гепатита В (HBcAg) — это антиген, экспрессируемый на поверхности ядра нуклеокапсида, продуцируемый, когда трансляция начинается с коровой области.
Не секретируется, остается в гепатоцитах и экспортируется только после оболочки HBsAg
Уровни> 10 мМЕ / мл являются защитными.
Положительный результат у лиц с недавней острой инфекцией HBV указывает на выздоровление.
В некоторых случаях хронической инфекции HBV могут присутствовать как HBsAg, так и Anti HBs.Эти антитела гетеротипны и, вероятно, не защищают.
Уровни> 10 мМЕ / мл являются защитными.
Положительный результат у лиц с недавней острой инфекцией HBV указывает на выздоровление.
В некоторых случаях хронической инфекции HBV могут присутствовать как HBsAg, так и Anti HBs. Эти антитела гетеротипны и, вероятно, не защищают.
Уровни> 10 мМЕ / мл являются защитными.
Положительный результат у лиц с недавней острой инфекцией HBV указывает на выздоровление.
В некоторых случаях хронической инфекции HBV могут присутствовать как HBsAg, так и Anti HBs. Эти антитела гетеротипны и, вероятно, не защищают.
C. Chang, et al. 1987 Экспрессия предкорной области вируса гепатита В птиц не требуется для репликации вируса.Дж. Вирол 611033225
Мария Куттикан Джаялакшми, Нараянан Кальянараман и Рамасами Питчаппан (2013). Генетическое разнообразие вируса гепатита B: патогенез заболевания, вирусная репликация, доктор Герман Росас-Акоста (ред.), ISBN: 978-953-51-1055-2, InTech, DOI: 10.5772 / 53818. Доступно по адресу: http://www.intechopen.com/books/viral-replication/hepatitis-b-virus-genetic-diversity-disease-pathogenesis
e-антиген гепатита B (HBeAg), вырабатываемый, когда трансляция начинается в предкорной области и секретируется в кровообращение.
HBeAg — дополнительный белок HBV, не необходимый для репликации in vivo, но важный для естественной инфекции.
Хорошо коррелирует с уровнем инфекционности, количеством присутствующего вируса и присутствием вирусной ДНК-полимеразы в сыворотке.
Этот антиген использовался клинически как показатель репликации вируса, инфекционности, тяжести заболевания и ответа на лечение
Milich et al. Также продемонстрировали иммуномодулирующую роль HBeAg в презентации антигена и распознавании клетками CD4 +.
D. R Milich, 1999 По-разному ли Т-клетки «видят» ядро гепатита В и е-антигены? Гастроэнтерология. 11637658
D. R. Milich, et al., 1998 Секретируемый антиген-предкоры гепатита В может модулировать иммунный ответ на нуклеокапсид: механизм персистенции. J Immunol.1604201321
D. R Milich, et al. 1993 Роль толерантности к Т-клеткам в сохранении инфекции вируса гепатита В.J Immunol Emphasis Tumor Immunol. 14322633D.
R Milich, et al. 1990 Является ли функция секретируемого е антигена гепатита В функцией индукции иммунологической толерантности в утробе матери? Proc Natl Acad Sci U S A. 87176599603
Сероконверсия к Anti HBe указывает на исчезновение инфекции.
В большинстве случаев эта сероконверсия связана с острым гепатитом, таким как повышение уровня аминотрансферазы.Это может отражать опосредованное клетками иммунное очищение гепатоцитов, инфицированных вирусом.
Напротив, не-A генотипы HBV (B, C, D и E) содержат тимидин в такая же позиция (T-1858), которая сочетается с A в 1896 году (16).Таким образом, прекоровые мутанты преобладают в Средиземноморье, где преобладают не-А генотипы, особенно D (17; 18).
Lindh M, AnderssonAS, Gusdal A: Генотипы, варианты nt 1858 и географическое происхождение вируса гепатита B — крупномасштабный анализ с использованием нового метода генотипирования. J. Infect. Дис. 175: 1285-1293, 1997 [pubmed] Ларас А., Коскинас Дж., Авгидис К. и др.: Частота и клиническое значение мутаций инициации трансляции прекоровых генов вируса гепатита В у пациентов с отрицательным антигеном е. J. Viral Hepat 5: 241-248, 1998 [опубликовано] Bozdayi AM, Bozkaya H, Turkyilmaz A, et al: Полиморфизм прекоровой области ДНК вируса гепатита B среди пациентов с хронической инфекцией HBV в Турции.Infection 27: 357-360, 1999 [pubmed] Amini-Bavil-Olyaee S, Sarrami-Forooshani R, Mahboudi F, et al: Характеристика генотипа и филогенетический анализ изолятов вируса гепатита B от иранских пациентов. J. Med. Virol. 75: 227-234, 2005 [pubmed
— вирус семейства Hepadnaviridae, HBV — самый маленький ДНК-вирус человека, несущий геном длиной всего 3200 нуклеотидов [4].Частично двухцепочечная кольцевая ДНК содержит четыре перекрывающиеся открытые рамки считывания, кодирующие гены S (поверхность), C (ядро), P (полимераза) и X
Напротив, не-A генотипы HBV (B, C, D и E) содержат тимидин в такая же позиция (T-1858), которая сочетается с A в 1896 году (16).Таким образом, прекоровые мутанты преобладают в Средиземноморье, где преобладают не-А генотипы, особенно D (17; 18).
Lindh M, AnderssonAS, Gusdal A: Генотипы, варианты nt 1858 и географическое происхождение вируса гепатита B — крупномасштабный анализ с использованием нового метода генотипирования. J. Infect. Дис. 175: 1285-1293, 1997 [pubmed] Ларас А., Коскинас Дж., Авгидис К. и др.: Частота и клиническое значение мутаций инициации трансляции прекоровых генов вируса гепатита В у пациентов с отрицательным антигеном е. J. Viral Hepat 5: 241-248, 1998 [опубликовано] Bozdayi AM, Bozkaya H, Turkyilmaz A, et al: Полиморфизм прекоровой области ДНК вируса гепатита B среди пациентов с хронической инфекцией HBV в Турции.Infection 27: 357-360, 1999 [pubmed] Amini-Bavil-Olyaee S, Sarrami-Forooshani R, Mahboudi F, et al: Характеристика генотипа и филогенетический анализ изолятов вируса гепатита B от иранских пациентов. J. Med. Virol. 75: 227-234, 2005 [pubmed
Кластеры молниеносного HBV в Израиле и Японии были отнесены к общему источнику инфекции с мутантами-предшественниками.
Это обычное явление в Средиземноморье и Европе.
Гепатит B: скрининг, профилактика, диагностика и лечение
2. Терро Н.А., Бзовей NH, Чанг КМ, Хван JP, Йонас М.М., Murad MH; Американская ассоциация по изучению заболеваний печени. Руководство AASLD по лечению хронического гепатита B. Гепатология . 2016; 63 (1): 261–283.
3. Шилли С., Мерфи ТВ, Сойер М, и другие.; Центры по контролю и профилактике заболеваний. Руководство CDC по оценке медицинского персонала на предмет защиты от вируса гепатита B и для управления постконтактным лечением. MMWR Recomm Rep . 2013; 62 (RR-10): 1–19.
4. Лин ЦЛ, Kao JH. Естественная история острого и хронического гепатита B: роль генотипов и мутантов HBV. Лучший Практик Рес Клин Гастроэнтерол . 2017; 31 (3): 249–255.
5. Ли М, Сон Дж. А., Сигер К.Распространение ядерной ДНК вируса гепатита В. Дж. Вирол . 2017; 92 (1): e01391–17.
6. Скрининг на вирус гепатита B во время беременности: заявление о подтверждении рекомендаций Целевой группы профилактических служб США. Энн Интерн Мед. . 2009. 150 (12): 869–873.
7. LeFevre ML. Скрининг на вирусную инфекцию гепатита В у небеременных подростков и взрослых: рекомендация Рабочей группы США по профилактическим услугам. Энн Интерн Мед. .2014. 161 (1): 58–66.
8. Американская академия семейных врачей. Рекомендации клинико-профилактической службы. Гепатит. https://www.aafp.org/patient-care/clinical-recommendations/all/hepatitis.html. По состоянию на 8 октября 2018 г.
9. Weinbaum CM, Уильямс I, Мачта EE, и другие.; Центры по контролю и профилактике заболеваний. Рекомендации по выявлению и ведению общественного здравоохранения лиц с хронической инфекцией вируса гепатита В. MMWR Recomm Rep . 2008; 57 (RR-8): 1–20.
10. Абара З.Е., Казим А, Шилли С, МакМахон Б.Дж., Харрис А.М. Вакцинация против гепатита B, скрининг и связь с лечением: рекомендации по передовой практике Американского колледжа врачей и Центров по контролю и профилактике заболеваний. Энн Интерн Мед. . 2017; 167 (11): 794–804.
11. Шилли С., Веллоцци C, Рейнгольд А, и другие. Профилактика заражения вирусом гепатита В в США: рекомендации Консультативного комитета по практике иммунизации. MMWR Recomm Rep . 2018; 67 (1): 1–31.
12. Центры по контролю и профилактике заболеваний. Вопросы и ответы по гепатиту B для медицинских работников. https://www.cdc.gov/hepatitis/hbv/hbvfaq.htm#D4. По состоянию на 3 ноября 2018 г.
13. Вакцина Heplisav-B® (HepB-CpG). Рекомендации Консультативного комитета по практике иммунизации (ACIP). https://www.cdc.gov/vaccines/schedules/vacc-updates/heplisav-b.html. По состоянию на 3 ноября 2018 г.
14. Kao JH. Вакцинация против гепатита В и профилактика гепатоцеллюлярной карциномы. Лучший Практик Рес Клин Гастроэнтерол . 2015; 29 (6): 907–917.
15. Шилли С., Харрис А, Link-Gelles R, Ромеро Дж, Палата J, Нельсон Н. Рекомендации Консультативного комитета по практике иммунизации по использованию вакцины против гепатита В с новым адъювантом. MMWR Morb Mortal Wkly Rep . 2018; 67 (15): 455–458.
16. Дэвид М.К., Ха Ш, Пэйнтер С, Лау К. Систематический обзор и метаанализ вариантов ведения взрослых, плохо реагирующих на вакцинацию против гепатита В. Вакцина . 2015; 33 (48): 6564–6569.
17. Манцукис К., Родригес-Перальварес М, Buzzetti E, и другие. Фармакологические вмешательства при острой инфекции гепатита B: попытка сетевого метаанализа. Кокрановская база данных Syst Rev . 2017; (3): CD011645.
18. Trépo C, Чан Х.Л., Лок А. Инфекция вирусом гепатита В. Ланцет . 2014. 384 (9959): 2053–2063.
19.Европейская ассоциация изучения печени. Руководство EASL 2017 по клинической практике лечения инфекции, вызванной вирусом гепатита B. Дж. Гепатол . 2017; 67 (2): 370–398.
20. Уилкинс Т, Циммерман Д, Schade RR. Гепатит В: диагностика и лечение. Ам Фам Врач . 2010. 81 (8): 965–972.
21. Агорам Р., Цай П, Дикинсон JA. Альфа-фетопротеин и / или ультрасонография печени для скрининга гепатоцеллюлярной карциномы у пациентов с хроническим гепатитом B. Кокрановская база данных Syst Rev . 2012; (9): CD002799.
22. Zhang BH, Ян Б.Х., Тан З.Ы. Рандомизированное контролируемое исследование скрининга гепатоцеллюлярной карциномы. J Cancer Res Clin Oncol . 2004. 130 (7): 417–422.
23. Тан Л.С., Covert E, Уилсон Э, Коттилил С. Хроническая инфекция гепатита B: обзор. ДЖАМА . 2018; 319 (17): 1802–1813.
24. Heimbach JK, Кулик Л.М., Финн РС, и другие.Рекомендации AASLD по лечению гепатоцеллюлярной карциномы. Гепатология . 2018; 67 (1): 358–380.
25. Комитет по инфекционным болезням; Комитет по плодам и новорожденным. Ликвидация перинатального гепатита В: введение первой дозы вакцины в течение 24 часов после рождения. Педиатрия . 2017; 140 (3): e20171870.
26. Шилли С, Мерфи ТВ, Фенлон Н, Ко С, Ward JW. Обновление: сокращенный интервал серологического тестирования после вакцинации младенцев, рожденных от матерей, инфицированных гепатитом B. MMWR Morb Mortal Wkly Rep . 2015; 64 (39): 1118–1120.
27. Гани MG. Текущие рекомендации по лечению хронического гепатита B: роль аналогов нуклеоз (т) идов и пегинтерферона. Лучший Практик Рес Клин Гастроэнтерол . 2017; 31 (3): 299–309.
28. Ким В., Абреу Р.М., Накагава Д.М., Бальдассаре Р.М., Каррильо Ф.Дж., Оно СК. Пегилированный интерферон альфа при хроническом гепатите B: систематический обзор и метаанализ. Дж. Вирусный гепатит . 2016; 23 (3): 154–169.
29. Арендс Ю.Е., Ливельд Ф.И., Ахмад С, Устяновский А. Новые вирусные и иммунологические мишени для лечения и лечения гепатита B: обзор. Инфекция Dis Ther . 2017; 6 (4): 461–476.
30. Марселлин П., Бонино Ф, Лау Г.К., и другие.; Пегинтерферон альфа-2а в HBeAg-отрицательной группе исследования хронического гепатита B. Устойчивый ответ у пациентов с отрицательным антигеном гепатита В через 3 года после лечения пегинтерфероном альфа-2а. Гастроэнтерология . 2009. 136 (7): 2169–2179.e1–4.
31. Марселлин П., Лау Г.К., Бонино Ф, и другие.; Группа по изучению HBeAg-отрицательного хронического гепатита B по пегинтерферону альфа-2a. Один пегинтерферон альфа-2a, один ламивудин и их комбинация у пациентов с HBeAg-отрицательным хроническим гепатитом B. N Engl J Med . 2004. 351 (12): 1206–1217.
32. Лау ГК, Пиратвисут Т, Луо К.Х., и другие.; Пегинтерферон Альфа-2а HBeAg-позитивная группа по исследованию хронического гепатита B. Пегинтерферон альфа-2а, ламивудин и их комбинация для HBeAg-положительного хронического гепатита B. N Engl J Med . 2005. 352 (26): 2682–2695.
33. Ли В.С., Ван MR, Kong LB, Рен РГ, Чжан Ю.Г., Nan YM. Терапия хроническим гепатитом B на основе пегинтерферона альфа с акцентом на клиренс HBsAg или сероконверсию: метаанализ контролируемых клинических исследований. BMC Infect Dis . 2011; 11: 165.
34. Бедре Р.Х., Радж У, Мисра СП, Varadwaj PK. Противовирусная терапия с аналогами нуклеотидов / нуклеозидов при хроническом гепатите B: метаанализ проспективных рандомизированных исследований. Индийский Дж. Гастроэнтерол . 2016; 35 (2): 75–82.
35. Вигано М, Гросси Г, Логлио А, Лампертико П. Лечение гепатита В: есть ли еще роль интерферона? Печень Инт .2018; 38 (приложение 1): 79–83.
36. Lexicomp.com. https://online.lexi.com/lco/action/home. По состоянию на 3 ноября 2018 г.
37. Terrault NA, Лок АЧС, МакМахон Б.Дж., и другие. Обновленная информация о профилактике, диагностике и лечении хронического гепатита B: руководство AASLD 2018 по гепатиту B. Гепатология . 2018; 67 (4): 1560–1599.
38. Бути М, Гейн Э, Сето В.К., и другие.; GS-US-320-0108 Следователи.Сравнение тенофовира алафенамида и тенофовира дизопроксил фумарата для лечения пациентов с HBeAg-отрицательной хронической вирусной инфекцией гепатита B: рандомизированное, двойное слепое, фаза 3, исследование не меньшей эффективности [опубликованная поправка появилась в Lancet Gastroenterol Hepatol. 2016; 1 (3): e2]. Ланцет Гастроэнтерол Гепатол . 2016; 1 (3): 196–206.
39. Чан Х.Л., Fung S, Сето В.К., и другие.; GS-US-320-0110 Следователи. Сравнение тенофовира алафенамида и тенофовира дизопроксил фумарата для лечения HBeAg-положительной хронической вирусной инфекции гепатита B: рандомизированное двойное слепое исследование не меньшей эффективности фазы 3 [опубликованные поправки приведены в Lancet Gastroenterol Hepatol.2016; 1 (3): e2]. Ланцет Гастроэнтерол Гепатол . 2016; 1 (3): 185–195.
40. Чанг ТТ, Гиш Р.Г., де Ман Р, и другие.; BEHoLD AI463022 Исследовательская группа. Сравнение энтекавира и ламивудина при HBeAg-положительном хроническом гепатите B. N Engl J Med . 2006. 354 (10): 1001–1010.
41. Лай Ц.Л., Шуваль Д., Лок А.С., и другие.; BEHoLD AI463027 Исследовательская группа.Сравнение энтекавира и ламивудина у пациентов с HBeAg-отрицательным хроническим гепатитом B [опубликованная поправка опубликована в N Engl J Med. 2006; 354 (17): 1863]. N Engl J Med . 2006. 354 (10): 1011–1020.
42. Марселлин П., Хиткот Э.Дж., Но я, и другие. Тенофовир дизопроксил фумарат по сравнению с адефовир дипивоксилом при хроническом гепатите B. N Engl J Med . 2008; 359 (23): 2442–2455.
43. Всемирная организация здравоохранения.Руководство по профилактике, уходу и лечению лиц с хронической инфекцией гепатита В. Март 2015 г. http://www.who.int/hiv/pub/hepatitis/hepatitis-b-guidelines/en/.

