Острый лейкоз — причины, симптомы, диагностика и лечение
Острый лейкоз – опухолевое поражение кроветворной системы, морфологической основой которого выступают незрелые (бластные) клетки, вытесняющие нормальные гемопоэтические ростки. Клиническая симптоматика острого лейкоза представлена прогрессирующей слабостью, немотивированным подъемом температуры, артралгиями и оссалгиями, кровотечениями различных локализаций, лимфаденопатией, гепатоспленомегалией, гингивитами, стоматитами, ангинами. Для подтверждения диагноза необходимо исследование гемограммы, пунктата костного мозга, биоптата подвздошной кости и лимфоузлов. Основу лечения острых лейкозов составляют химиотерапевтические курсы и сопроводительная терапия.
Общие сведения
Острый лейкоз — форма лейкемии, при которой нормальное костномозговое кроветворение вытесняется мало дифференцированными клетками-предшественниками лейкоцитов с их последующим накоплением в периферической крови, инфильтрацией тканей и органов. Термины «острый лейкоз» и «хронический лейкоз» отражают не только длительность течения заболевания, но также морфологическую и цитохимическую характеристику опухолевых клеток. Острый лейкоз является наиболее частой формой гемобластозов: он развивается у 3-5 из 100 тыс. человек; соотношение взрослых и детей – 3:1. При этом у лиц старше 40 лет статистически чаще диагностируется острый миелоидный лейкоз, а у детей – острый лимфобластный лейкоз.
Острый лейкоз
Причины острого лейкоза
Первопричиной острого лейкоза является мутация гемопоэтической клетки, дающей начало опухолевому клону. Мутация кроветворной клетки приводит к нарушению ее дифференцировки на ранней стадии незрелых (бластных) форм с дальнейшей пролиферацией последних. Образующиеся опухолевые клетки замещают нормальные ростки гемопоэза в костном мозге, а в дальнейшем выходят в кровь и разносятся в различные ткани и органы, вызывая их лейкемическую инфильтрацию. Все бластные клетки несут в себе одинаковые морфологические и цитохимические признаки, что свидетельствует в пользу их клонального происхождения от одной клетки-родоначальницы.
Причины, запускающие мутационный процесс, не известны. В гематологии принято говорить о факторах риска, повышающих вероятность развития острого лейкоза. В первую очередь, это генетическая предрасположенность: наличие в семье больных с острым лейкозом практически утраивает риск заболевания у близких родственников. Риск возникновения острого лейкоза повышается при некоторых хромосомных аномалиях и генетических патологиях — болезни Дауна, синдроме Клайнфельтера, Вискотта-Олдрича и Луи-Барра, анемии Фанкони и др.
Вероятно, что активация генетической предрасположенности происходит под действием различных экзогенных факторов. В числе последних могут выступать ионизирующая радиация, химические канцерогены (бензол, мышьяк, толуол и др.), цитостатические препараты, используемые в онкологии. Нередко острый лейкоз становится следствием противоопухолевой терапии других гемобластозов – лимфогранулематоза, неходжкинских лимфом, миеломной болезни. Подмечена связь острых лейкозов с предшествующими вирусными инфекциями, угнетающими иммунную систему; сопутствующими гематологическими заболеваниями (некоторыми формами анемий, миелодисплазиями, пароксизмальной ночной гемоглобинурией и др.).
Классификация острого лейкоза
В онкогематологии общепринята международная FAB-классификация острых лейкозов, дифференцирующая различные формы заболевания в зависимости от морфологии опухолевых клеток на лимфобластные (вызываемые низкодифференцированными предшественниками лимфоцитов) и нелимфобластные (объединяющие остальные формы).
1. Острые лимфобластные лейкозы взрослых и детей:
- пре-В-форма
- В-форма
- пре-Т-форма
- Т-форма
- ни Т ни В-форма
2. Острые нелимфобластные (миелоидные) лейкозы:
- о. миелобластный (вызван неконтрорлируемой пролиферацией предшественников гранулоцитов)
- о. моно- и о. миеломонобластный (характеризуются усиленным размножением монобластов)
- о. мегакариобластный (связан с преобладанием недифференцированных мегакариоцитов – предшественников тромбоцитов)
3. Острый недифференцированный лейкоз.
Течение острых лейкозов проходит ряд стадий:
- I (начальную) — преобладают общие неспецифические симптомы.
- II (развернутую) — характеризуется четко выраженными клиническими и гематологическими симптомами гемобластоза. Включает: дебют или первую «атаку», неполную или полную ремиссию, рецидив или выздоровление
- III (терминальную) – характеризуется глубоким угнетением нормального гемопоэза.
Симптомы острого лейкоза
Манифестация острого лейкоза может быть внезапной или стертой. Типично начало, характеризующееся высокой лихорадкой, интоксикацией, потливостью, резким упадком сил, анорексией. Во время первой «атаки» больные отмечают упорные боли в мышцах и костях, артралгии. Иногда начальная стадия острого лейкоза маскируется под ОРВИ или ангину; первыми признаками лейкемии могут быть язвенный стоматит или гиперпластический гингивит. Довольно часто заболевание обнаруживается случайно при профилактическом исследовании гемограммы или ретроспективно, когда острый лейкоз переходит в следующую стадию.
В развернутом периоде острого лейкоза развиваются анемический, геморрагический, интоксикационный и гиперпластический синдромы.
Анемические проявления обусловлены нарушением синтеза эритроцитов, с одной стороны, и повышенной кровоточивостью – с другой. Они включают бледность кожных покровов и слизистых, постоянную усталость, головокружение, сердцебиение, повышенное выпадение волос и ломкость ногтей и др. Усиливается выраженность опухолевой интоксикации. В условиях абсолютной лейкопении и упадка иммунитета легко присоединяются различные инфекции: пневмонии, кандидоз, пиелонефрит и т. д.
В основе геморрагического синдрома лежит выраженная тромбоцитопения. Диапазон геморрагических проявлений колеблется от мелких единичных петехий и синяков до гематурии, десневых, носовых, маточных, желудочно-кишечных кровотечений и пр. По мере прогрессирования острого лейкоза кровотечения могут становиться все массивнее вследствие развития ДВС-синдрома.
Гиперпластический синдром связан с лейкемической инфильтрацией как костного мозга, так и других органов. У больных острым лейкозом наблюдается увеличение лимфоузлов (периферических, медиастинальных, внутрибрюшных), гипертрофия миндалин, гепатоспленомегалия. Могут возникать лейкозные инфильтраты кожи (лейкемиды), оболочек мозга (нейролейкоз), поражение легких, миокарда, почек, яичников, яичек и др. органов.
Полная клинико-гематологическая ремиссия характеризуется отсутствием внекостномозговых лейкемических очагов и содержанием бластов в миелограмме менее 5% (неполная ремиссия – менее 20%). Отсутствие клинико-гематологических проявлений в течение 5 лет расценивается как выздоровление. В случае увеличения бластных клеток в костном мозге более 20%, их появления в периферической крови, а также выявления внекостномозговых метастатических очагов диагностируется рецидив острого лейкоза.
Терминальная стадия острого лейкоза констатируется при неэффективности химиотерапевтического лечения и невозможности достижения клинико-гематологической ремиссии. Признаками данной стадии служат прогрессирование опухолевого роста, развитие несовместимых с жизнью нарушений функции внутренних органов. К описанным клиническим проявлениям присоединяются гемолитическая анемия, повторные пневмонии, пиодермии, абсцессы и флегмоны мягких тканей, сепсис, прогрессирующая интоксикация. Причиной смерти больных становятся некупируемые кровотечения, кровоизлияния в мозг, инфекционно-септические осложнения.
Диагностика острого лейкоза
Во главе диагностики острых лейкозов стоит оценка морфологии клеток периферической крови и костного мозга. Для гемограммы при лейкемии характерна анемия, тромбоцитопения, высокая СОЭ, лейкоцитоз (реже лейкопения), присутствие бластных клеток. Показателен феномен «лейкемического зияния» — промежуточные стадии между бластами и зрелыми клетками отсутствуют.
С целью подтверждения и идентификации разновидности острого лейкоза выполняется стернальная пункция с морфологическим, цитохимическим и иммунофенотипическим исследованием костного мозга. При исследовании миелограммы обращает внимание увеличение процента бластных клеток (от 5% и выше), лимфоцитоз, угнетение красного ростка кроветворения (кроме случаев о. эритромиелоза) и абсолютное снижение или отсутствие мегакариоцитов (кроме случаев о. мегакариобластного лейкоза). Цитохимические маркерные реакции и иммунофенотипирование бластных клеток позволяют точно установить форму острого лейкоза. При неоднозначности трактовки анализа костного мозга прибегают к проведению трепанобиопсии.
С целью исключения лейкемической инфильтрации внутренних органов производится спинномозговая пункция с исследованием ликвора, рентгенография черепа и органов грудной клетки, УЗИ лимфатических узлов, печени и селезенки. Кроме гематолога, больные острым лейкозом должны быть осмотрены неврологом, офтальмологом, отоларингологом, стоматологом. Для оценки тяжести системных нарушений может потребоваться исследование коагулограммы, биохимического анализа крови, проведение электрокардиографии, ЭхоКГ и др.
Дифференциально-диагностические мероприятия направлены на исключение ВИЧ-инфекции, инфекционного мононуклеоза, цитомегаловирусной инфекции, коллагенозов, тромбоцитопенической пурпуры, агранулоцитоза; панцитопении при апластической анемии, В12 и фолиеводефицитной анемии; лейкемоидных реакций при коклюше, туберкулезе, сепсисе и др. заболеваниях.
Лечение острого лейкоза
Пациентов с острым лейкозом лечат в стационарах онкогематологического профиля. В палатах организуется усиленный санитарно-дезинфекционный режим. Больные с острым лейкозом нуждаются в проведении гигиенической обработки полости рта, профилактики пролежней, туалета половых органов после физиологических отправлений; организации высококалорийного и витаминизированного питания.
Непосредственно лечение острых лейкозов проводится последовательно; основные этапы терапии включают достижение (индукцию) ремиссии, ее закрепление (консолидацию) и поддержание, профилактику осложнений. Для этого разработаны и используются стандартизированные схемы полихимиотерапии, которые подбираются гематологом с учетом морфологической и цитохимической формы острого лейкоза.
При благоприятной ситуации ремиссия обычно достигается в течение 4-6 недель усиленной терапии. Затем, в рамках консолидации ремиссии проводится еще 2-3 курса полихимиотерапии. Поддерживающая противорецидивная терапия осуществляется еще в течение не менее 3-х лет. Наряду с химиотерапией при остром лейкозе необходимо проведение сопроводительного лечения, направленного на предупреждение агранулоцитоза, тромбоцитопении, ДВС-синдрома, инфекционных осложнений, нейролейкемии (антибиотикотерапия, переливание эритроцитарной, тромбоцитарной массы и свежезамороженной плазмы, эндолюмбальное введение цитостатиков). При лейкемической инфильтрации глотки, средостения, яичек и др. органов проводится рентгенотерапия очагов поражения.
В случае успешного лечения достигается уничтожение клона лейкозных клеток, нормализация кроветворения, что способствует индукции длительного безрецидивного периода и выздоровления. Для предупреждения рецидивов острого лейкоза может быть проведена трансплантация костного мозга после предварительного кондиционирования путем химиотерапии и тотального облучения.
По имеющимся статистическим сведениям, использование современных цитостатических средств приводит к переходу острого лейкоза в фазу ремиссии у 60-80% больных; из них у 20-30% удается добиться полного выздоровления. В целом прогноз при острых лимфобластных лейкозах более благоприятен, чем при миелобластных.
www.krasotaimedicina.ru
Диагностика лейкоза: все основные методы
Лейкоз – онкологический процесс, нарушающий работу кроветворной системы, при котором деформируются и видоизменяются клетки крови. Количество незрелых лимфоцитов беспорядочно увеличивается. Продуцируемые атипичные клетки распространяются по кровотоку и провоцируют рост метастазов в любых органах тела. Накапливаясь в костном мозге, они постепенно заменяют здоровые клетки. Нарушается баланс лейкоцитов, тромбоцитов и эритроцитов. Для выявления диагноза используют комплексный подход. Проблемой занимаются онкогематологи.
Заболевание, при котором нарушен кроветворный процесс, делится на ряд видов. Лейкозы возникают из определённых клеток и формируют новообразования.
- Лимфобластная лейкемия протекает в острой форме. Кровь наполняют повреждённые лейкоциты. Рак лимфобластного типа чаще встречается у детей младшего возраста. Главный симптом заболевания – частые инфекционные болезни с высыпаниями на кожных покровах. При этом ребёнок вялый, отказывается от еды, возникают частые кровотечения, образуются кровоподтеки на теле. При подтверждении диагноза начинается незамедлительное лечение, способное побороть злокачественный процесс.
- Лимфобластный лейкоз имеет хронический характер. Развивается медленно, без ярко выраженных симптомов. Обычно диагностируется у взрослых старше 60 лет. Преимущественно у представителей сильного пола.
- При лейкозе миелобластного типа наблюдается острое течение болезни. Незрелые миелоидные клетки обнаруживаются в крови и костном мозге. Болезнь поражает взрослое население. Характерны симптомы инфекционных заболеваний разного генеза.
- Миелолейкоз выступает в качестве подтверждения диагноза. Хроническая патология медленно развивается и обычно обнаруживается при диагностике других заболеваний.
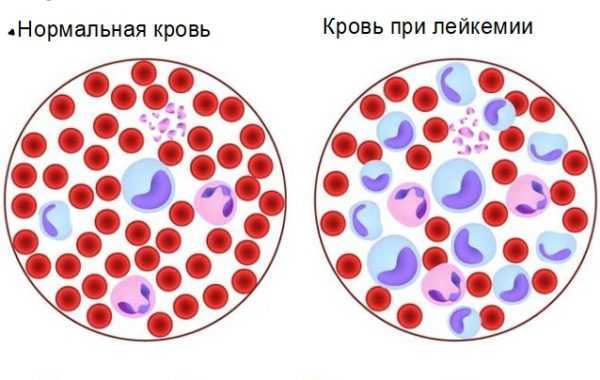
Хроническую стадию разделяют на 2 вида:
- Доброкачественный лейкоз диагностируется при наличии одного клона атипичной клетки.
- Для злокачественной формы характерно наличие вторичных клонов. Болезнь стремительно развивается с бесконтрольным делением бластов.
Причины возникновения болезни
Главная причина – аномальные процессы в кроветворящих органах, в частности в костном мозге. Развиваются на фоне аутоиммунных заболеваний, генетических нарушений на стадии формирования плода и под действием различных внешних факторов:
- Плохая экологическая обстановка;
- Вредные привычки;
- Вирусные поражения организма;
- Контакт с радиационным и ультрафиолетовым излучением.
Группа риска состоит из пожилых людей, больных с иммунодефицитом и хроническими воспалительными процессами в организме.
Методы лабораторной диагностики
Лейкемия признана опасным злокачественным заболеванием, требующим особого лечения. Из-за отсутствия ярких симптомов на первых стадиях болезни люди путают лейкозы с доброкачественными процессами. К примеру, частые простудные заболевания начинают пугать больного только после длительного времени развития болезни, усиления симптомов и при отсутствии положительной реакции на терапевтическое лечение. Если терапевт отмечает нарушения, свойственные болезням костного мозга, пациент направляется на консультацию и дальнейшее лечение к онкологу.

Лабораторные исследования назначают в начале определения проблемы. При результатах, отклоненных от нормы, наблюдается увеличение несозревших клеток. Их количество превышает 30%, эритроцитарные ростки занимают больше 50%. В костном мозге отмечаются атипичные промиелоциты.
Для диагностики уровня лейкоцитов, эритроцитов и тромбоцитов исследуют клинический анализ крови. Повышенный уровень лейкоцитов и снижение количества других клеток позволяют распознать рак на ранней стадии. При исследовании периферической крови обнаруживается нейтро- и тромбоцитопения, лимфоцитоз, азурофильные гранулы, нормохромная анемия и зрелые бласты с отсутствующим промежуточным созреванием.
- Для лейкоза характерно значительное снижение уровня гемоглобина. При этом больной исключает менструальные, обильные носовые кровотечения, потерю крови при хирургическом вмешательстве в ближайшее время. При онкологии гемоглобин падает в 2 раза. Показатель снижается при острой форме болезни.
- Отмечается снижение ретикулоцитов.
- Лимфоцитарная формула представлена серьёзными нарушениями. В зависимости от стадии рака, уровень лимфоцитов снижается и повышается.
- Врачи обращают внимание на скорость оседания эритроцитов (СОЭ). При онкологии она значительно увеличена.
- В формуле крови отсутствуют базофилы и эозинофилы.
- Если в крови отсутствуют переходные клетки, а формула представлена только большим количеством молодых и малым количеством зрелых форм, обнаруживается лейкемический провал.
Лейкоциты в крови человека
Совокупность нескольких признаков требует консультации гематолога. Если изменён один показатель в формуле крови, развитие онкологического процесса сводится к нулю.
Биохимия крови выявляет состояние и работоспособность внутренних органов под влиянием онкологического процесса.
При подозрении на лейкоз острой или хронической формы диагностика расширяется:
- Важно диагностировать степень злокачественности рака. Дифференциальная особенность клетки говорит о её природе и агрессивности. Эти особенности можно выявить с помощью гистологического исследования биоматериала.
- Костный мозг подвергается пункции с помощью иглы, введенной в полость кости. Обычно для биопсии выбирается грудная клетка. Исследование показывает наличие острого или хронического процесса. По анализу можно определить цитогенетический и морфологический вид болезни. С помощью данной процедуры выполняется проверка реакции пораженной клетки на химиопрепарат.
- Миеломограмма обнаруживает соотношение атипичных клеток с нормальными. Обследование показывает степень пораженности организма. У здорового человека бластные клетки не должны превышать 5%. Исследуемый материал представлен образцом костного мозга. Во время процедуры обнаруживаются лимфоцитоз и природа атипичных клеток. Отсутствуют мегакариоциты. Этот способ признан наиболее точным для постановки диагноза.
- Цитохимическая лабораторная диагностика основана на определении специфических ферментов. Метод незаменим при определении острых форм заболевания и прогнозировании их течения.
- Для диагностики острого лимфо- и миелобластного лейкоза проводят иммунофенотипирование. Тактика лечения этих видов лейкоза различна, поэтому важно уточнить диагноз.
- Необходимо исследовать ликвор (спинномозговую жидкость) для выявления повышенного количества клеток (цитоза).
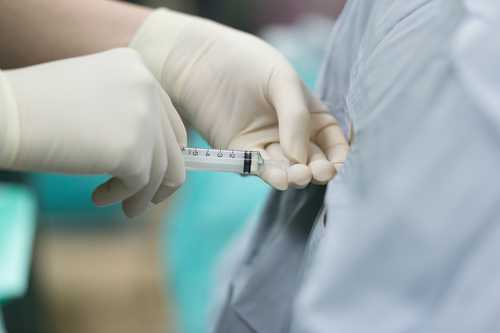
Забор спинномозговой жидкости
Инструментальные исследования
Диагностика лейкоза включает ряд инструментальных методов. Они не уступают по информативности лабораторным. Чтобы провериться на рак крови, пациент проходит следующие исследования:
- При помощи компьютерной томографии выявляются повреждения сосудов и метастазы в лимфатических узлах. Метод используется для масштабной диагностики организма путём послойного сканирования.
- Рентгенография грудной клетки назначается при характерных симптомах повреждения лёгких: регулярном кашле, отделении мокроты с включениями крови, боли в груди.
- Если онкологический процесс поразил головной мозг, рекомендовано проведение магнитно-резонансной томографии. Для болезни характерны симптомы: ухудшение зрения, онемение конечностей, нарушения памяти и сознания, головокружения и обмороки.
- Для выявления отклонений в работе сердечной мышцы проводят электрокардиограмму и эхокардиограмму.
- Диф диагностика основана на исключении возможных патологий с такими же симптомами, как при лейкозе. Исследование проводится с помощью компьютерных программ. Лейкемия схожа по симптоматике со следующими заболеваниями:

- Мононуклеоз инфекционного генеза провоцирует увеличение селезёнки. Увеличивается температура тела. В крови присутствуют недоразвитые лимфоциты. Эти же показатели встречаются при ангине и желтухе.
- ВИЧ не является онкологической болезнью, но тоже снижает иммунитет до 0. Человек страдает от частых инфекционных заболеваний. Наблюдается лимфаденопатия. Специальный анализ крови исключает вариант развития рака.
- При поражении человека токсичными веществами развивается апластическая анемия. Клетки костного мозга заменяются жировой тканью. Развивается панцитопения.
- Снижение количества всех клеток крови происходит после операций на органах желудочно-кишечного тракта.
Современные методы исследования распознают рак на каждом этапе развития. Для благоприятного исхода необходимо обращаться за медицинской помощью при любых нарушениях здоровья. Система кроветворения выполняет жизненно важную функцию, позволяющую людям противостоять болезнетворным бактериям.
Результаты исследований предоставляют возможность подобрать индивидуальное эффективное лечение. Обычно с раком крови борется химиотерапия. Для определённой разновидности лейкоза онкологи используют различные медикаменты.
При отдельных патологических процессах применяют трансплантацию костного мозга. Кроветворный процесс перезапускается, и пациент входит в стойкую ремиссию.
onko.guru
Хронический лейкоз — причины, симптомы, диагностика и лечение
Хронический лейкоз – первичное опухолевое заболевание системы кроветворения, субстратом которого выступают зрелые и созревающие клетки миелоидного или лимфоидного ряда. Различные формы хронического лейкоза протекают с преобладанием интоксикационного (слабость, артралгии, оссалгии, анорексия, похудание), тромбогеморрагического (кровоточивость, тромбозы различной локализации), лимфопролиферативного синдромов (увеличение лимфоузов, спленомегалия и др.). Решающее значение в диагностике хронического лейкоза принадлежит исследованию ОАК, биоптатов костного мозга и лимфоузлов. Лечение хронических лейкозов проводится методами химиотерапии, лучевой терапии, иммунотерапии, возможна трансплантация костного мозга.
Общие сведения
Хронический лейкоз – хронические лимфопролиферативные и миелопролиферативные заболевания, характеризующиеся избыточным увеличением количества кроветворных клеток, сохраняющих способность к дифференцировке. В отличие от острых лейкозов, при которых происходит пролиферация низкодифференцированных гемопоэтических клеток, при хронических лейкозах опухолевый субстрат представлен созревающими или зрелыми клетками. Для всех типов хронических лейкозов характерна длительная стадия доброкачественной моноклоновой опухоли.
Хронические лейкозы поражают преимущественно взрослых в возрасте 40-50 лет; мужчины болеют чаще. На долю хронического лимфоидного лейкоза приходится около 30% случаев, хронического миелоидного лейкоза — 20% всех форм лейкемии. Хронический лимфолейкоз в гематологии диагностируется в 2 раза чаще, чем хронический миелолейкоз. Лейкозы у детей протекают в хроническом варианте крайне редко — в 1-2% случаев.
Хронический лейкоз
Причины хронического лейкоза
Истинные причины, приводящие к развитию хронического лейкоза, неизвестны. В настоящее время наибольшее признание получила вирусно-генетическая теория гемобластозов. Согласно данной гипотезе, некоторые виды вирусов (в числе которых – вирус Эбштейна-Барр, ретровирусы и др.) способны проникать в незрелые кроветворные клетки и вызывать их беспрепятственное деление. Не подвергается сомнению и роль наследственности в происхождении лейкозов, поскольку доподлинно известно, что заболевание нередко носит семейный характер. Кроме этого, хронический миелолейкоз в 95% случаев ассоциирован с аномалией 22-й хромосомы (филадельфийской или Рh-хромосомы), фрагмент длинного плеча которой транслоцирован на 9-ю хромосому.
Наиболее значимыми предрасполагающими факторами к различным видам и формам хронических лейкозов выступают воздействия на организм высоких доз радиации, рентгеновского облучения, производственных химических вредностей (лаков, красок и др.), лекарственных препаратов (солей золота, антибиотиков, цитостатиков), длительный стаж курения. Риск развития хронического лимфоцитарного лейкоза повышается при длительном контакте с гербицидами и пестицидами, а хронического миелоидного лейкоза – при радиационном облучении.
В патогенезе хронического лимфолейкоза значимая роль принадлежит иммунологическим механизмам – об этом свидетельствует его частое сочетание с аутоиммунной гемолитической анемией и тромбоцитопенией, коллагенозами. Вместе с тем, у большинства больных хроническими лейкозами причинно значимых факторов выявить не удается.
Классификация хронического лейкоза
В зависимости от происхождения и клеточного субстрата опухоли хронические лейкозы делятся на лимфоцитарные, миелоцитарные (гранулоцитарные) и моноцитарные. К группе хронических лейкозов лимфоцитарного происхождения относятся: хронический лимфолейкоз, болезнь Сезари (лимфоматоз кожи), волосатоклеточный лейкоз, парапротеинемические гемобластозы (миеломная болезнь, макроглобулинемия Вальденстрема, болезни легких цепей, болезни тяжелых цепей).
Хронические лейкозы миелоцитарного происхождения включают следующие формы: хронический миелолейкоз, эритремию, истинную полицитемию, хронический эритромиелоз и др. К хроническим лейкозам моноцитарного происхождения относятся: хронический моноцитарный лейкоз и гистиоцитозы.
В своем развитии опухолевый процесс при хроническом лейкозе проходит две стадии: моноклоновую (доброкачественную) и поликлоновую (злокачественную). Течение хронического лейкоза условно подразделяется на 3 стадии: начальную, развернутую и терминальную.
Симптомы хронического миелоидного лейкоза
В начальном периоде хронического миелолейкоза клинические проявления отсутствуют или неспецифичны, гематологические изменения выявляются случайно при исследовании крови. В доклиническом периоде возможно нарастание слабости, адинамии, потливости, субфебрилитета, болей в левом подреберье.
Переход хронического миелоидного лейкоза в развернутую стадию знаменуется прогрессирующей гиперплазией селезенки и печени, анорексией, похуданием, выраженными болями в костях и артралгиями. Характерно образование лейкемических инфильтратов на коже, слизистых полости рта (лейкемический периодонтит), ЖКТ. Геморрагический синдром проявляется гематурией, меноррагией, метроррагией, кровотечениями после экстракции зубов, кровавыми поносами. В случае присоединения вторичной инфекции (пневмонии, туберкулеза, сепсиса и др.) температурная кривая приобретает гектический характер.
Терминальная стадия хронического миелоидного лейкоза протекает с резким обострением всех симптомов и выраженной интоксикацией. В этот период может развиваться плохо поддающееся терапии и угрожающее жизни состояние – бластный криз, когда из-за резкого увеличения количества бластных клеток течение заболевания становится похожим на острый лейкоз. Для бластного криза характерна агрессивная симптоматика: лейкемиды кожи, тяжелые кровотечения, вторичные инфекции, высокая температура, возможен разрыв селезенки.
Симптомы хронического лимфоидного лейкоза
Долгое время единственным признаком хронического лимфолейкоза может быть лимфоцитоз до 40-50%, незначительное увеличение одной-двух групп лимфоузлов. В развернутый период лимфаденит принимает генерализованную форму: увеличиваются не только периферические, но и медиастинальные, мезентериальные, забрюшинные узлы. Возникает сплено- и гепатомегалия; возможно сдавление холедоха увеличенными лимфатическими узлами с развитием желтухи, а также верхней полой вены с развитием отеков шеи, лица, рук (синдром ВПВ). Беспокоят упорные оссалгии, кожный зуд, рецидивирующие инфекции.
Тяжесть общего состояния больных хроническим лимфоидным лейкозом обусловлена прогрессированием интоксикации (слабость, потливость, лихорадка, анорексия) и анемического синдрома (головокружение, одышка, сердцебиение, обморочные состояния).
Терминальная стадия хронического лимфоидного лейкоза характеризуется присоединением геморрагического и иммунодефицитного синдромов. В этот период развивается тяжелая интоксикация, возникают кровоизлияния под кожу и слизистые, носовые, десневые, маточные кровотечения. Иммунодефицит, обусловленный неспособностью функционально незрелых лейкоцитов выполнять свои защитные функции, проявляется синдромом инфекционных осложнений. У больных хроническим лимфолейкозом часты легочные инфекции (бронхиты, бактериальные пневмонии, туберкулезные плевриты), грибковые поражения кожи и слизистых, абсцессы и флегмоны мягких тканей, пиелонефриты, герпетическая инфекция, сепсис.
Нарастают дистрофические изменения внутренних органов, кахексия, почечная недостаточность. Летальный исход при хроническом лимфоидном лейкозе наступает от тяжелых инфекционно-септических осложнений, кровотечений, анемии, истощения. Возможна трансформация хронического лимфолейкоза в острый лейкоз или лимфосаркому (неходжкинскую лимфому).
Диагностика хронического лейкоза
Предполагаемый диагноз устанавливается на основании анализа гемограммы, с результатами которой пациент должен быть немедленно направлен к гематологу. Типичные для хронического миелоидного лейкоза изменения включают: анемию, присутствие единичных миелобластов и гранулоцитов на разной стадии дифференцировки; в период бластного криза количество бластных клеток увеличивается более чем на 20%. При хроническом лимфолейкозе определяющими гематологическими признаками выступают выраженный лейкоцитоз и лимфоцитоз, наличие лимфобластов и клеток Боткина-Гумпрехта.
С целью определения морфологии опухолевого субстрата показано выполнение стернальной пункции, трепанобиопсии, биопсии лимфоузлов. В пунктате костного мозга при хроническом миелолейкозе увеличено количество миелокариоцитов за счет незрелых клеток гранулоцитарного ряда; в трепанобиоптате определяется замещение жировой ткани миелоидной. При хроническом лимфоидном лейкозе миелограмма характеризуется резким усилением лимфоцитарной метаплазии.
Для оценки выраженности лимфопролиферативного синдрома применяются инструментальные исследования: УЗИ лимфатических узлов, селезенки, рентгенография грудной клетки, лимфосцинтиграфия, МСКТ брюшной полости и ряд других.
Лечение и прогноз хронического лейкоза
На ранней доклинической стадии лечение неэффективно, поэтому больные подлежат динамическому наблюдению. Общережимные мероприятия предполагают исключение физических перегрузок, стрессов, инсоляции, электропроцедур и теплолечения; полноценное витаминизированное питание, длительные прогулки на свежем воздухе.
В развернутом периоде миелолейкоза назначается химиотерапевтическое лечение (бусульфан, митобронитол, гидроксимочевина и др.), при выраженной спленомегалии проводится облучение селезенки. Подобная тактика, хоть и не приводит к полному излечению, но существенно тормозит прогрессирование болезни и позволяет отсрочить наступление бластного криза. Кроме медикаментозной терапии, при хроническом миелоцитарном лейкозе используются процедуры лейкафереза. В ряде случаев излечение достигается с помощью трансплантации костного мозга.
При переходе хронического миелолейкоза в терминальную стадию назначается высокодозная полихимиотерапия. В среднем после установления диагноза больные хроническим миелолейкозом живут 3-5 лет, в отдельных случаях – 10-15 лет.
При хроническом лимфолейкозе также проводится цитостатическая терапия (хлорбутин, циклофосфамид), иногда в сочетании со стероидной терапией, облучением лимфоузлов, селезенки, кожи. При значительном увеличении селезенки выполняется спленэктомия. Применяется трансплантация стволовых клеток, однако ее эффективность еще требует подтверждения. Продолжительность жизни больных хроническим лимфоидным лейкозом может составлять от 2-3 лет (при тяжелых, неуклонно прогрессирующих формах) до 20-25 лет (при относительно благоприятном течении).
www.krasotaimedicina.ru
Симптомы и лечение лейкоза — Medside.ru
Закрыть- Болезни
- Инфекционные и паразитарные болезни
- Новообразования
- Болезни крови и кроветворных органов
- Болезни эндокринной системы
- Психические расстройства
- Болезни нервной системы
- Болезни глаза
- Болезни уха
- Болезни системы кровообращения
- Болезни органов дыхания
- Болезни органов пищеварения
- Болезни кожи
- Болезни костно-мышечной системы
- Болезни мочеполовой системы
- Беременность и роды
- Болезни плода и новорожденного
- Врожденные аномалии (пороки развития)
- Травмы и отравления
- Симптомы
- Системы кровообращения и дыхания
- Система пищеварения и брюшная полость
- Кожа и подкожная клетчатка
- Нервная и костно-мышечная системы
- Мочевая система
- Восприятие и поведение
- Речь и голос
- Общие симптомы и признаки
- Отклонения от нормы
- Диеты
- Снижение веса
- Лечебные
- Быстрые
- Для красоты и здоровья
- Разгрузочные дни
- От профессионалов
- Монодиеты
- Звездные
- На кашах
- Овощные
- Детокс-диеты
- Фруктовые
- Модные
- Для мужчин
- Набор веса
- Вегетарианство
- Национальные
- Лекарства
- Антибиотики
- Антисептики
- Витамины
- Гинекологические
- Гормональные
- Дерматологические
- Диабетические
- Для глаз
- Для крови
- Для нервной системы
- Для печени
- Для повышения потенции
- Для полости рта
- Для похудения
- Для суставов
- Для ушей
- Желудочно-кишечные
- Кардиологические
- Контрацептивы
- Мочегонные
- Обезболивающие
- От аллергии
- От кашля
- От насморка
- Повышение иммунитета
- Противовирусные
- Противогрибковые
- Противомикробные
- Противоопухолевые
- Противопаразитарные
- Противопростудные
- Сердечно-сосудистые
- Урологические
- Другие лекарства
- Врачи
- Клиники
- Справочник
- Аллергология
- Анализы и диагностика
- Беременность
- Витамины
- Вредные привычки
- Геронтология (Старение)
- Дерматология
- Дети
- Женское здоровье
- Инфекция
- Контрацепция
- Косметология
- Народная медицина
- Обзоры заболеваний
- Обзоры лекарств
- Ортопедия и травматология
- Питание
- Пластическая хирургия
- Процедуры и операции
- Психология
- Роды и послеродовый период
- Сексология
- Стоматология
- Травы и продукты
- Трихология
- Другие статьи
- Словарь терминов
- [А] Абазия .. Ацидоз
medside.ru
Острый лейкоз (клиника, диагностика, лечение)
Автор Статьи: Крючкова Оксана Александровна.
Клиническая картина, наблюдаемая при развитии острого лейкоза.
В практике врача принято выделять три стадии развития данной патологии.
1 стадия- начальная. В клинической картине преобладание общих симптомов, характерных для многих других заболеваний, кроме гематологической патологии.
2 стадия- развернутая клиническая картина. Именно в этой стадии врач видит клиническую картину развернутого острого заболевания. При этом наблюдается первая «атака», ремиссия различной степени выраженности, возможно выздоровление или вновь возвращение заболевания.
3 стадия- терминальная. Именно в этой стадии происходит полное угнетение нормального кроветворения.
Итак, какие же симптомы может видеть пациент, страдающий данной патологией, и какие симптомы могут навести врача на мысль о наличии острого лейкоза.
Острое внезапное начало заболевания, и быстрое развитие клинической картины патологии.Наличие высокой температуры. Кроме этого имеется интоксикация, повышенное потоотделение, пациент резко худеет.Если заболевание находится в периоде так называемой первой «атаки», то больной будет отмечать сильные мышечные боли, боли в костях, суставах. Данные признаки характерны более для вирусной инфекции, поэтому ни пациент ни врач не подозревают даже о наличии острого лейкоза.Возможно наличие изъязвление на слизистой полости рта, воспаление десен.
Когда заболевание переходит в развернутую стадию, то на первое место выходят несколько синдромов, характеризующих острый лейкоз.
Острый лейкоз (микрофотография крови)
Анемический синдром. Происходит нарушение образования красных кровяных телец-эритроцитов, наблюдается излишняя кровоточивость. Пациент бледен, жалуется на постоянные головокружения, усталость, ощущение биения сердца даже при совершении минимальной физической нагрузки. Кроме этого волосы и ногти становятся слишком ломкими, выпадают. Если иммунный статус организма резко снижен, то присоединяется инфекция, имеющая вторичный характер. Это пневмония, воспаление почек-пиелонефрит, обострение герпес-вирусной инфекции, грибковое поражение слизистых оболочек.Геморрагический синдром. Данный синдром характеризуется снижением числа тромбоцитов в организме пациента. Кровоточивость не просто повышается, возможны профузные кровотечения и остановить их достаточно трудно. При осмотре кожных покровов пациентов наблюдаются различные мелкие кровоизлияния, синяки, гематомы. При ухудшении состояния больного возможны кровотечения из полости матки, желудка, носа, десневые кровотечения. В крайне тяжелых случаях развивается синдром диссеминированного внутрисосудистого свертывания крови (ДВС-синдром). Тогда кровотечения начинаются просто отовсюду без видимой на то причины. В таких случаях требуется введение специальных препаратов для спасения жизни больного.Синдром гиперпластический. Развивается в результате того, что происходит инфильтрирование тканей лейкозными клетками. У пациента наблюдается гипертрофия и разрастание лимфоузлов, спленомегалия и гепатомегалия (увеличение селезенки и печени). Лимфоузлы, доступные пальпаторному исследованию, становятся плотными, они множественные, имеют эластическую консистенцию, причем отмечается то, что они спаяны между собой и образуют этакие конгломераты, при этом боли данный процесс не вызывает. При увеличении лимфатических узлов, находящихся в брюшной полости, появляются симптомы «острого живота». Если лимфатические узлы, расположенные в средостении увеличиваются, то появляются симптомы, вызванные механическим сдавлением крупных сосудов (верхняя полая вена) и тем самым нарушившие циркуляцию крови из сердца. При осмотре полости рта врач может отметить появление на слизистой оболочке язвочек, распространяющихся постепенно все ниже и затрагивающих миндалины и глотку. Если произвести небольшое надавливание на костные выступы, то пациент, страдающий острым лейкозом, отметит наличие болевого симптома. Боль появляется из-за того, что в надкостнице и под ней скапливаются бластные клетки и образуются инфильтраты. При осмотре кожных покровов отмечаются, так называемые, лейкемиды- образования красновато-синего цвета, имеющие форму папул. Отдалёнными и самыми тяжелыми проявлениями острого лейкоза считается метастазирование клеток и поражение половой системы (мошонка, яички у мужчин), нервной системы. При исследовании таких больных неврологом возможны как проявления легкой симптоматики общемозговой, так и признаки очаговых поражений (симптомы снижения сознания, нарушение координации, симтоматика, связанная с поражением зрительных путе й).Синдром интоксикации. Пациент жалуется на слабость, невозможность совершения привычной физической нагрузки, повышение температуры, головные боли и головокружения, тошноту, резкую потерю массы тела, боли в мышцах и костях, снижение силы мышц и их тонуса.Синдром иммунодефицита. Вся иммунная система организма пациента, страдающего от острого лейкоза, нарушена. Снижены защитные способности, лейкоциты крови не выполняют свойственную им роль. В результате происходит присоединение вторичной инфекции и развитие воспалений. Все воспалительные проявления сразу генерализуются и приобретают затяжное и тяжелое течение, возможно развитие сепсиса.
При наступлении ремиссии острого лейкоза отмечается то, что количество бластных клеток в миелограмме всего до пяти процентов (полная ремиссия), или до двадцати процентов (неполная ремиссия). Если после развернутой клиники острого лейкоза в анализе крови происходят подобные изменения и держатся они до пяти лет, то говорят о выздоровлении. Если же происходит вновь повышение уровня бластов, то происходит рецидивирование заболевания.
При развитии у пациента терминальной стадии острого лейкоза происходит стремительное усиление роста опухолевых клеток, даже при соответствующем лечении. Ни одна из схем лечебных мероприятий, предпринимаемых врачами не оказывает должного эффекта. Начинаются нарушения со стороны всех органов и систем, происходит присоединение вторичной инфекции и ее быстрая генерализация. Из-за нарушений в организме, несовместимых с жизнью пациента, происходит смерть больного.
Диагностические мероприятия, направленные на постановку диагноза острый лейкоз.
Общий (клинический) анализ крови. Отмечается сдвиг лейкоцитарной формулы влево, снижение количества тромбоцитов, эритроцитов, увеличение СОЭ, появление феномена «лейкемического провала» — когда между бластами и клетками зрелыми нет промежуточных форм. Коагулограмма, биохимический анализ крови.Пунктирование грудной клетки, для получения костного мозга. При исследовании получают повышение числа бластов, отмечается то, что красный кровяной росток угнетен, мегакариоциты снижены или полностью отсутствуют.Пунктирование спинного мозга.Рентгенографическое исследование органов грудной клетки, черепа.Ультразвуковое исследование органов брюшной полости, лимфоузлов.Осмотр смежных специалистов.
Острый лейкоз: дифференциальная диагностика.
При постановке диагноза острый лейкоз следует учитывать то, то подобные проявления характерны и для ряда других заболеваний. Поэтому необходимо проведение дифференциации острого лейкоза с ВИЧ-инфекцией, мононуклеозом, имеющим инфекционное происхождение, цитомегаловирусной инфекцией, коллагенозами, тромбоцитопенической пурпурой, агранулоцитозом. Кроме этого подобные клинические проявления возможны при анемиях, коклюшной инфекции, туберкулезном поражении.
Лечение острого лейкоза.
Лечебные мероприятия, используемые при остром лейкозе подразделяются на фазы.
1-я фаза- терапия индукционная. Ее суть заключается в том, что пациент в течение 2 месяцев получает препараты, воздействующие на костный мозг. Данный тип лекарств мощно и главное в короткие сроки индуцирует наступление ремиссии. Но эти препараты не панацея. Если не продолжить лечение после окончания их приема, то болезнь возвратится вновь.
2-я фаза- ее основная функция- закрепить тот эффект, который был получен при применении препаратов в первой фазе. При этом на данном этапе необходимо подавить рост и уничтожить все опухолевые клетки. Препараты, которые назначаются в данный период, направлены на снижение сопротивляемости организма к препаратам. При этом химиопрепараты принимаются около 3 лет. Это необходимо для того, чтобы закрепить полученный результат.
На всем протяжении лечения необходимо пребывание в стационаре. Так как иммунный ответ организма снижен или вовсе отсутствует, то возможно присоединение вторичной инфекции. Кроме этого необходимы переливания крови и ее компонентов, что тоже производится только в условиях круглосуточного стационара.
Кроме всего вышеперечисленного, не надо забывать о том, что одним из методов лечения служит трансплантация костного мозга или стволовых клеток от донора к больному. Данная манипуляция выполняется лишь после тщательной подготовки, установление полнейшей совместимости компонентов для пересадки и проводится только в условиях больницы.
В настоящее время острый лейкоз излечим практически в 60 % случаев.
Вы можете записаться к данным специалистам на консультацию по поводу этого заболевания:
Профессор Шатохин Юрий Васильевич
ДМН, Зав. кафедрой гематологии РостГМУ.
Подробнее / Отзывы
Профессор Лысенко Ирина Борисовна
ДМН, Зав. отд. гематологии Ростовского Онкологического Института.
Подробнее / Отзывы
Снежко Ирина Викторовна
Кандидат медицинских наук Ассистент кафедры гематологии РостГМУ Врач высшей квалификационной категории.
Подробнее / Отзывы
gematolog-ro.ru
Острый миелоидный лейкоз — Википедия
Острый миелоидный лейкоз (также ОМЛ, острый нелимфобластный лейкоз, острый миелогенный лейкоз) — это злокачественная опухоль миелоидного ростка крови, при которой быстро размножаются изменённые белые кровяные клетки. Накапливаясь в костном мозге, они подавляют рост нормальных клеток крови, что приводит к снижению количества эритроцитов, тромбоцитов, и нормальных лейкоцитов. Болезнь проявляется быстрой утомляемостью, одышкой, частыми мелкими повреждениями кожи, повышенной кровоточивостью, частыми инфекционными поражениями. До сих пор явная причина заболевания неизвестна, однако некоторые факторы риска его возникновения выявлены. ОМЛ является острым заболеванием, развивается быстро и без лечения приводит к смерти больного за несколько месяцев, иногда — недель.
Это самый распространённый вид острого лейкоза у взрослых, заболеваемость им с возрастом увеличивается. Хотя острый миелоидный лейкоз заболевание относительно редкое — на его долю приходится лишь 1,2 % смертельных случаев злокачественных опухолей в США[3], — ожидается его учащение вместе с постарением населения.
Встречаются несколько разновидностей ОМЛ, лечение и прогноз для них оказывается разным. Уровень выживаемости на протяжении пяти лет колеблется между 15 и 70 %, а частота ремиссии — от 78 до 33 % в зависимости от подвида заболевания. В начале ОМЛ лечат химиопрепаратами для того, чтобы добиться ремиссии; затем может проводиться поддерживающее химиолечение, или проводится пересадка кроветворных стволовых клеток. Последние исследования на генетическом уровне позволили разработать тесты, с помощью которых можно довольно точно определить вероятность выживания больного и эффективность того или иного лекарства для индивидуального случая ОМЛ.[источник не указан 746 дней]
Самые часто используемые схемы классификации ОМЛ — это давняя франко-американо-британская (ФАБ) система и более современная система Всемирной организации здравоохранения (ВОЗ).
Классификация острого миелоидного лейкоза по системе Всемирной системы здравоохранения[править | править код]
Система классификации острого миелоидного лейкоза ВОЗ разработана с учётом системы ФАБ и имеет целью более эффективное клиническое применение и учитывает наиболее прогностически значимые признаки заболевания. Каждый из видов (категорий) ОМЛ по классификации ВОЗ включает в себя несколько подвидов (подкатегорий) описательного характера, представляющих интерес для гематологов и онкологов; однако, бо́льшая часть клинически важной информации в классификации ВОЗ взаимосвязана через распределение по перечисленным ниже подвидам.
Подвиды острого миелоидного лейкоза по классификации ВОЗ:[4]
Название подвида Описание МКБ-О ОМЛ с характерными генетическими изменениями Включает: Несколько ОМЛ с изменениями, связанными с миелодисплазией Этот подвид включает больных с предшествующим миелодиспластическим синдромом (МДС) или миелопролиферативной болезнью (МПБ) или с характерными для него цитогенетическими изменениями. Этот подвид ОМЛ чаще встречается у пожилых людей и отличается неблагоприятным прогнозом.Включает в себя ОМЛ со следующими изменениями:
- Сложный кариотип
- Несбалансированные аномалии
- Сбалансированные аномалии
M9895/3 ОМЛ и МДС, связанные с предыдущим лечением Этот подвид ОМЛ включает больных, получавших химиотерапию и/или лучевое лечение, после которых возник ОМЛ или МДС. При этих лейкозах могут быть характерные изменения в хромосомах, прогноз при них часто бывает хуже. M9920/3 Миелоидная саркома Этот подвид включает больных с миелоидной саркомой Миелопролиферативные заболевания, связанные с Синдромом Дауна Этот подвид включает больных как с кратковременными (преходящими) миелопролиферативными состояниями на фоне синдрома Дауна, так и с ОМЛ на фоне синдрома Дауна Бластная плазмацитоидная дендритноклеточная опухоль Этот подвид включает больных с бластными дендритноклеточными опухолями ОМЛ, не подпадающие под признаки перечисленных подвидов Включает подвиды ОМЛ, не входящие в перечисленные выше, в том числе: M9861/3
Бывают такие подвиды острого лейкоза, при которых изменённые лейкоциты невозможно определить как лимфоциты или гранулоциты, или когда присутствуют злокачественно изменённые клетки обоих ростков. Такие лейкозы иногда называют бифенотипными острыми лейкозами.
Франко-американско-британская классификация[править | править код]
Франко-американско-британская классификационная (ФАБ) система разделяет ОМЛ на 9 подвидов, от М0 по M8, основываясь на типах клеток — предшественниц лейкоцитов, и на степени зрелости изменённых клеток. Определение злокачественных клеток проводят на основании внешних признаков при световой микроскопии и/или цитогенетически, выявляя лежащие в основе отклонений изменения в хромосомах. У разных подвидов ОМЛ разные прогноз и ответ на лечение. Несмотря на преимущества классификации ВОЗ, система ФАБ до сих пор широко применяется.
По ФАБ существует девять подтипов ОМЛ.
Необычные фенотипы острого миелоидного лейкоза[править | править код]
Морфологические подтипы ОМЛ включают многие исключительно редкие подтипы не включённые в классификацию ФАБ. Все они, за исключением острого миелоидного дендритноклеточного лейкоза включены в классификацию ВОЗ. В списке ниже перечислены эти подтипы.
 Инфильтрированная лейкоцитами печень при миелолейкозе
Инфильтрированная лейкоцитами печень при миелолейкозеБо́льшая часть симптомов ОМЛ вызывается замещением нормальных клеток крови лейкозными клетками. Недостаточное образование лейкоцитов обусловливает высокую восприимчивость больного к инфекциям — несмотря на то, что лейкемические клетки происходят от предшественников лейкоцитов, способность противостоять инфектам у них отсутствует.[5] Снижение количества красных кровяных телец (анемия) может вызывать усталость, бледность, и одышку. Недостаток тромбоцитов может привести к легкой повреждаемости кожи и повышенной кровоточивости.
Ранние признаки ОМЛ часто неопределённы и неспецифичны, и могут походить на признаки гриппа или других распространённых болезней. Вот некоторые общие симптомы ОМЛ: лихорадка, усталость, потеря веса или снижение аппетита, одышка, анемия, повышенная повреждаемость кожи и слизистых оболочек и кровоточивость, петехии (плоские, размером с булавочную головку пятнышки внутри кожи на месте кровоизлияний), гематомы, боль в костях и суставах, и стойкие или частые инфекции.[5]
При ОМЛ может быть увеличение селезёнки но обычно оно незначительно и бессимптомно. Увеличение лимфоузлов при ОМЛ случается нечасто, в отличие от острого лимфобластного лейкоза. В 10 % случаев развиваются изменения кожи в виде кожного лейкоза. Изредка при ОМЛ возникает Синдром Свита, он же паранеопластический синдром — воспаление кожи вокруг поражённых хлоромой участков.[5]
У некоторых больных ОМЛ появляется припухлость дёсен из-за инфильтрации тканей лейкозными клетками. Изредка первым признаком лейкоза оказывается хлорома — плотная лейкемическая масса за пределами костного мозга. Иногда заболевание протекает бессимптомно, и лейкоз выявляется общим анализом крови в ходе профилактического осмотра.[6]
Был выявлен ряд факторов, способствующих возникновению ОМЛ — иные расстройства системы кроветворения, воздействие вредных веществ, ионизирующее излучение, и генетическое влияние.
Пре-лейкоз[править | править код]
«Пре-лейкозные нарушения кроветворения, такие, как миелодиспластический синдром или миелопролиферативный синдром могут привести к ОМЛ; вероятность заболевания зависит от формы миелодиспластического или миелопролиферативного синдрома.[7]
Воздействие химических веществ[править | править код]
Противоопухолевое химиотерапевтическое воздействие, особенно алкилирующими веществами, может увеличивать вероятность возникновения ОМЛ в последующем. Наивысшая вероятность заболевания приходится на 3—5 лет после химиотерапии.[8] Другие химиотерапевтические препараты особенно эпиподофилотоксины и антрациклины, также связываются с постхимиотерапевтическими лейкозами. лейкозы такого вида часто объясняют специфическими изменениями в хромосомах лейкозных клеток.[9]
Воздействие бензола и других ароматических органических растворителей, связанное с профессиональной деятельностью, в качестве возможной причины ОМЛ остаётся спорным. Бензол и многие его производные проявляют канцерогенные свойства in vitro. Данные некоторых наблюдений подтверждают возможность влияния профессиональных контактов с этими веществами на вероятность развития ОМЛ, однако другие исследования подтверждают, что если и существует такая опасность, то она является лишь добавочным фактором.[10][11]
Ионизирующее излучение[править | править код]
Воздействие ионизирующего излучения повышает вероятность заболеваня ОМЛ. У переживших атомную бомбардировку Хиросимы и Нагасаки заболеваемость ОМЛ повышена,[12] так же как у рентгенологов, получивших высокие дозы рентгеновского излучения в то время, когда меры радиологической защиты были недостаточными.[13]
Генетические факторы[править | править код]
Вероятно, существует наследственно повышенная вероятность заболевания ОМЛ. Есть большое количество сообщений о множестве семейных случаев ОМЛ, когда заболеваемость превышала среднестатистическую.[14][15][16][17] Вероятность возникновения ОМЛ у ближайших родственников больного втрое выше.[18]
Ряд врождённых состояний может повышать вероятность ОМЛ. Чаще всего это синдром Дауна, при котором вероятность ОМЛ повышена в 10 — 18 раз.[19]
Изменения соотношения клеточных элементов в общем анализе крови — первое, что наводит на мысль о возможности ОМЛ. Наиболее частым оказывается лейкоцитоз- повышение общего количества лейкоцитов, иногда с появлением бластных (незрелых) форм, но бывает так, что ОМЛ проявляется изолированным снижением тромбоцитов, эритроцитов, а количество лейкоцитов может оказаться даже сниженным (лейкопения).[20] Предварительный диагноз ОМЛ может быть определён в случае выявления в мазках периферической крови бластных форм лейкоцитов, но для окончательного диагноза должны быть выявлены соответствующие изменения в анализе аспирационного биоптата костного мозга.
Костный мозг и кровь исследуют световым микроскопированием и поточной цитометрией для установления диагноза и дифференцирования ОМЛ от других лейкозов, например, от острого лимфобластного лейкоза, а также для уточнения подтипа ОМЛ. Образец крови или костного мозга обычно проверяют на присутствие хромосомных транслокаций обычными цитогененитческими способами, или способом флуоресцентной гибридизации in situ. Генетические исследования проводят и для выявления характерных мутаций, которые могут влиять на исход заболевания — например, в FLT3, в нуклеоплазмине, или в KIT.[21]
Цитохимические красители для мазков крови и костного мозга оказываются очень полезными для дифференциальной диагностики ОМЛ и ОЛЛ, а также для выделения подтипов ОМЛ. Сочетание миелопероксидазы или красителя Суданский чёрный и неспцифического эстеразного красителя обеспечивает получение нужной информации в большинстве случаев. Реакции миелопероксидазы или Суданского чёрного оказываются самыми полезными для установления диагноза ОМЛ и его дифференцирования от ОЛЛ. Неспецифический краситель эстеразы используется для моноцитаронй составляющей острых миелолейкозов и для дифференцирования от незрелой формы монобластного лейкоза от ОЛЛ.[4]
Диагноз и классификация ОМЛ может оказаться непростой задачей, этим должен должен заниматься квалифицированный гематопатолог или гематолог. В явных случаях наличие некоторых характерный морфологических признаков, таких, как тельца Ауэра, или специфическия для АМЛ результаты поточной цитометрии дают возможность надёжно отделять ОМЛ от других лейкозов; однако при отсутствии такх явных признаков диагностика существенно осложняется.[22]
В соответствии с широко используемыми критериями классификации ВОЗ диагноз ОМЛ устанавливаетсяв том случае, если доказано если в крови и/или костном мозге более 20 % клеток представлены миелобластами.[23] ОМЛ следует тщательно дифференцировать от так называемых прелейкозных состояний, в частности, от миелодиспластического синдрома или миелопролиферативного синдрома, которые лечатся по-разному.
Поскольку острый промиелоцитарный лейкоз (ОПЛ), требуя уникального способа лечения очень хорошо ему поддаётся, очень важно быстро подтвердить или отвергнуть этот подвид лейкоза. Для этого часто используют флюоресцентную гибридизацию in situ, выполненную на крови или костном мозге, поскольку ею легко выявляется хромосомная транслокация (t[15;17]) специфичная для ОПЛ.[24]
Злокачественными клетками при ОМЛ выступают миелобласты. В нормальном гемопоэзе миелобласты являются незрелыми предшественниками лейкоцитов миелоидного ряда;нормальные миелобласты постепенно созревают, превращаясь в нормальные лейкоциты. Однако при ОМЛ в каком — то из миелобластов накапливаются генетические изменения, которые «замораживают» клетку в незрелом состоянии, останавливая процесс клеточной дифференциации. [25] Сама по себе такая мутация не вызывает лейкоз, но когда «остановка дифференциации» сочетается с другими мутациями, которые приводят к утрате генетического контроля над ростом клеток, результатом оказывается неуправляемое размножение незрелого клеточного клона, определяющего клиническую сущность ОМЛ.[26]
Большое разнообразие и генетическая неоднородность ОМЛ происходит от того, что лейкозная трансформация может возникнуть на множестве этапов дифференциации клетки.[27] Современные схемы классификации ОМЛ признают факт зависимости свойств и поведения лейкозных клеток, а также течения лейкоза от того, на каком этапе остановилась дифференциация.
Специфические цитогенетическиеотклонения обнаруживаются у многих больных ОМЛ. Виды изменений хромосом часто прогностически значимы.[28] Хромосомные транслокации кодируют синтез гибридных белков, чаще всего, факторов транскрипции — вспомогательных белков — помощников РНК-полимераз, изменённые свойства которых могут привести к останову дифференциации.[29] Например, при остром промиелоцитарном лейкозе транслокация t(15; 17) вызывает синтез гибридного протеина PML-RARα, который связывается с рецептором ретиноевой кислоты в промоторах некоторых специфических для миелоидных клеток генов и останавливает в этих клетках дифференциацию.[30]
Схема транслокации хромосом.Клинические проявления и симптомы ОМЛ возникают потому что, умножаясь, клетки лейкозного клона мешают деятельности нормальных клеток и стремятся вытеснить их из костного мозга.[31] Это приводит к нейтропении, анемии, и тромбоцитопении. Чаще всего симптомы ОМЛ определяются недостаточностью нормальных клеток крови. В редких случаях у больных развиваются хлоромы — плотные опухоли из лейкозных клеток за прелами костного мозга, которые могут вызывать различные симптомы в зависимости от локализации хлоромы.[5]
Лечение ОМЛ состоит в основном из химиотерапии, и делится на два этапа: индукция и постремиссионное лечение(или консолидация). Цель индукционной терапии является достижение полной ремиссии за счет уменьшения количества лейкозных клеток до не обнаруживаемого уровня; цель консолидирующей терапии заключается в ликвидации остаточных, не обнаруживаемых современными методами остатками болезни и излечение.[32]
Индукция[править | править код]
Для всех подтипов ОМЛ за исключением M3 по классификации ФАБ, обычно используют индукционную химиотерапию цитарабином и антрациклиновым антибиотиком (например, даунорубицином или идарубицином).[33] Этот способ индукционной химиотерапии известен под названием «7+3». Название происходит от того, что в этом режиме предусматриваются 7 дней непрерывного инфузионного вливания цитарабина, при этом в первые три дня одновременно болюсно вводится антрациклиновый антибиотик. При таком способе лечения ремиссия наступает почти у 70 % больных ОМЛ.[34] Могут применяться и другие способы индукционного лечения, включая режимы FLAG, DAT, ADE и подобные, или монотерапию высокими дозами цитарабина, или лечение препаратами, находящимися на стадии исследования.[35][36] Вследствие токсического воздействия лечения, в том числе подавления миелоидного ростка и повышения вероятности инфекционных осложнений очень старым больным индукционная химиотерапия не предлагается, и назначается менее интенсивное паллиативное лечение химиопрепаратами.
Подвид ОМЛ M3, также известный под названием острый промиелоцитарный лейкоз, почти во всех случаях лечится препаратом ПТРК (полностью транс- ретиноевая кислота) в дополнение к индукционной терапии.[37][38][39] При лечении острого промиелоцитарного лейкоза нужно учитывать возможность развития синдрома диссеминированного внутрисосудистого свёртывания вследствие поступления содержимого гранул промиелоцитов в периферическую кровь. Лечение острого промиелоцитарного лейкоза исключительно эффективно, это достоверно доказано множеством документированных случаев лечения.
3 августа 2017 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США(FDA) одобрило к применению VYXEOS (Jazz Pharmaceuticals, Inc) для лечения взрослых с недавно диагностированными двумя подвидами ОМЛ (t- AML и AML-MRC). VYXEOS представляет собой липосомальную комбинацию цитарабина и даунорубицина и показало себя намного эффективнее при лечении этих двух подтипов , чем применение стандартной 7+3 комбинации. Лекарство продемонстрировало среднюю общую выживаемость 9,6 месяцев по сравнению с 5,9 месяцами при комбинации 7+3 [40]
В 2018 году FDA одобрила применение гласдегиба (glasdegib) в комбинации с низкодозным цитарабином для лечения пациентов в возрасте старше 75 лет, которым невозможно провести интенсивную химиотерапию. Одобрение препарат получил с условием размещения в инструкции предупреждения о высоком риске токсичности для плода.[41]
Целью индукционного этапа лечения является достижение полной ремиссии. Полная ремиссия не означает, что заболевание полностью вылечено. Скорее, состояние полной ремиссии говорит о невозможности обнаружить спящую болезнь существующими способами диагностики.[33] Полная ремиссия достигается у 50-70 % взрослых больных с впервые выявленным ОМЛ, разница зависит от прогностических факторов, о которых сказано выше.[42] Длительность ремиссии зависит от прогностических качеств исходного лейкоза. В основном, все случаи ремиссии без дополнительного, консолидирующего лечения закачиваются рецидивом.[43]
Консолидационное лечение[править | править код]
Даже после достижения полной ремиссии вероятно, немногие лейкозные клетки всё же выживают. Их так мало, что обнаружить их пока невозможно. В случае не проведения послеремиссионно
ru.wikipedia.org
Острый лимфобластный лейкоз — причины, симптомы, диагностика и лечение, прогноз
Острый лимфобластный лейкоз – злокачественное поражение системы кроветворения, сопровождающееся неконтролируемым увеличением количества лимфобластов. Проявляется анемией, симптомами интоксикации, увеличением лимфоузлов, печени и селезенки, повышенной кровоточивостью и дыхательными расстройствами. Из-за снижения иммунитета при остром лимфобластном лейкозе часто развиваются инфекционные заболевания. Возможно поражение ЦНС. Диагноз выставляется на основании клинических симптомов и данных лабораторных исследований. Лечение – химиотерапия, радиотерапия, пересадка костного мозга.
Общие сведения
Острый лимфобластный лейкоз (ОЛЛ) – самое распространенное онкологическое заболевание детского возраста. Доля ОЛЛ составляет 75-80% от общего количества случаев болезней системы кроветворения у детей. Пик заболеваемости приходится на возраст 1-6 лет. Мальчики страдают чаще девочек. Взрослые пациенты болеют в 8-10 раз реже детей. У пациентов детского возраста острый лимфобластный лейкоз возникает первично, у взрослых нередко является осложнением хронического лимфоцитарного лейкоза. По своим клиническим проявлениям ОЛЛ схож с другими острыми лейкозами. Отличительной особенностью является более частое поражение оболочек головного и спинного мозга (нейролейкоз), при отсутствии профилактики развивающееся у 30-50% пациентов. Лечение осуществляют специалисты в области онкологии и гематологии.
В соответствии с классификацией ВОЗ различают четыре типа ОЛЛ: пре-пре-В-клеточный, пре-В-клеточный, В-клеточный и Т-клеточный. В-клеточные острые лимфобластные лейкозы составляют 80-85% от общего количества случаев заболевания. Первый пик заболеваемости приходится на возраст 3 года. В последующем вероятность развития ОЛЛ повышается после 60 лет. Т-клеточный лейкоз составляет 15-20% от общего количества случаев болезни. Пик заболеваемости приходится на возраст 15 лет.
Острый лимфобластный лейкоз
Причины острого лимфобластного лейкоза
Непосредственной причиной острого лимфобластного лейкоза является образование злокачественного клона – группы клеток, обладающих способностью к неконтролируемому размножению. Клон образуется в результате хромосомных аберраций: транслокации (обмена участками между двумя хромосомами), делеции (утраты участка хромосомы), инверсии (переворота участка хромосомы) или амплификации (образования дополнительных копий участка хромосомы). Предполагается, что генетические нарушения, вызывающие развитие острого лимфобластного лейкоза, возникают еще во внутриутробном периоде, однако для завершения процесса формирования злокачественного клона нередко требуются дополнительные внешние обстоятельства.
В числе факторов риска возникновения острого лимфобластного лейкоза обычно в первую очередь указывают лучевые воздействия: проживание в зоне с повышенным уровнем ионизирующей радиации, радиотерапию при лечении других онкологических заболеваний, многочисленные рентгенологические исследования, в том числе во внутриутробном периоде. Уровень связи, а также доказанность наличия зависимости между различными лучевыми воздействиями и развитием острого лимфобластного лейкоза сильно различаются.
Так, взаимосвязь между лейкозами и лучевой терапией в наши дни считается доказанной. Риск возникновения острого лимфобластного лейкоза после радиотерапии составляет 10%. У 85% пациентов болезнь диагностируется в течение 10 лет после окончания курса лучевой терапии. Связь между рентгенологическими исследованиями и развитием острого лимфобластного лейкоза в настоящее время остается на уровне предположений. Достоверных статистических данных, подтверждающих эту теорию, пока не существует.
Многие исследователи указывают на возможную связь между ОЛЛ и инфекционными заболеваниями. Вирус возбудителя острого лимфобластного лейкоза пока не выявлен. Существуют две основные гипотезы. Первая – ОЛЛ вызывается одним пока не установленным вирусом, однако болезнь возникает только при наличии предрасположенности. Вторая – причиной развития острого лимфобластного лейкоза могут стать разные вирусы, риск развития лейкоза у детей повышается при недостатке контактов с патогенными микроорганизмами в раннем возрасте (при «нетренированности» иммунной системы). Пока обе гипотезы не доказаны. Достоверные сведения о наличии связи между лейкозами и вирусными заболеваниями получены только для Т-клеточных лейкозов у взрослых больных, проживающих в странах Азии.
Вероятность развития острого лимфобластного лейкоза повышается при контакте матери с некоторыми токсическими веществами в период гестации, при некоторых генетических аномалиях (анемии Фанкони, синдроме Дауна, синдроме Швахмана, синдроме Клайнфельтера, синдроме Вискотта-Олдрича, нейрофиброматозе, целиакии, наследственно обусловленных иммунных нарушениях), наличии онкологических заболеваний в семейном анамнезе и приеме цитостатиков. Некоторые специалисты отмечают возможное негативное влияние курения.
Симптомы острого лимфобластного лейкоза
Болезнь развивается стремительно. К моменту постановки диагноза суммарная масса лимфобластов в организме может составлять 3-4% от общей массы тела, что обусловлено бурной пролиферацией клеток злокачественного клона на протяжении 1-3 предыдущих месяцев. В течение недели количество клеток увеличивается примерно вдвое. Различают несколько синдромов, характерных для острого лимфобластного лейкоза: интоксикационный, гиперпластический, анемический, геморрагический, инфекционный.
Интоксикационный синдром включает в себя слабость, утомляемость, лихорадку и потерю веса. Повышение температуры может провоцироваться как основным заболеванием, так и инфекционными осложнениями, которые особенно часто развиваются при наличии нейтропении. Гиперпластический синдром при остром лимфобластном лейкозе проявляется увеличением лимфоузлов, печени и селезенки (в результате лейкемической инфильтрации паренхимы органов). При увеличении паренхиматозных органов могут появляться боли в животе. Увеличение объема костного мозга, инфильтрация надкостницы и тканей суставных капсул могут становиться причиной ломящих костно-суставных болей.
О наличии анемического синдрома свидетельствуют слабость, головокружения, бледность кожи и учащение сердечных сокращений. Причиной развития геморрагического синдрома при остром лимфобластном лейкозе становятся тромбоцитопения и тромбозы мелких сосудов. На коже и слизистых выявляются петехии и экхимозы. При ушибах легко возникают обширные подкожные кровоизлияния. Наблюдаются повышенная кровоточивость из ран и царапин, кровоизлияния в сетчатку, десневые и носовые кровотечения. У некоторых больных острым лимфобластным лейкозом возникают желудочно-кишечные кровотечения, сопровождающиеся кровавой рвотой и дегтеобразным стулом.
Иммунные нарушения при остром лимфобластном лейкозе проявляются частым инфицированием ран, царапин и следов от уколов. Могут развиваться различные бактериальные, вирусные и грибковые инфекции. При увеличении лимфатических узлов средостения отмечаются нарушения дыхания, обусловленные уменьшением объема легких. Дыхательная недостаточность чаще обнаруживается при Т-клеточном остром лимфобластном лейкозе. Нейролейкозы, спровоцированные инфильтрацией оболочек спинного и головного мозга, чаще отмечаются во время рецидивов.
При вовлечении ЦНС выявляются положительные менингеальные симптомы и признаки повышения внутричерепного давления (отек дисков зрительных нервов, головная боль, тошнота и рвота). Иногда поражение ЦНС при остром лимфобластном лейкозе протекает бессимптомно и диагностируется только после исследования цереброспинальной жидкости. У 5-30% мальчиков появляются инфильтраты в яичках. У пациентов обоих полов на коже и слизистых оболочках могут возникать багрово-синюшные инфильтраты (лейкемиды). В редких случаях наблюдаются выпотной перикардит и нарушения функции почек. Описаны случаи поражений кишечника.
С учетом особенностей клинической симптоматики можно выделить четыре периода развития острого лимфобластного лейкоза: начальный, разгара, ремиссии, терминальный. Продолжительность начального периода составляет 1-3 месяца. Преобладает неспецифическая симптоматика: вялость, утомляемость, ухудшение аппетита, субфебрилитет и нарастающая бледность кожи. Возможны головные боли, боли в животе, костях и суставах. В период разгара острого лимфобластного лейкоза выявляются все перечисленные выше характерные синдромы. В период ремиссии проявления болезни исчезают. Терминальный период характеризуется прогрессирующим ухудшением состояния больного и завершается летальным исходом.
Диагностика острого лимфобластного лейкоза
Диагноз выставляют с учетом клинических признаков, результатов анализа периферической крови и данных миелограммы. В периферической крови пациентов с острым лимфобластным лейкозом выявляются анемия, тромбоцитопения, повышение СОЭ и изменение количества лейкоцитов (обычно – лейкоцитоз). Лимфобласты составляют 15-20 и более процентов от общего количества лейкоцитов. Количество нейтрофилов снижено. В миелограмме преобладают бластные клетки, определяется выраженное угнетение эритроидного, нейтрофильного и тромбоцитарного ростка.
В программу обследования при остром лимфобластном лейкозе входят люмбальная пункция (для исключения нейролейкоза), УЗИ органов брюшной полости (для оценки состояния паренхиматозных органов и лимфатических узлов), рентгенография грудной клетки (для обнаружения увеличенных лимфоузлов средостения) и биохимический анализ крови (для выявления нарушений функции печени и почек). Дифференциальный диагноз острого лимфобластного лейкоза проводят с другими лейкозами, отравлениями, состояниями при тяжелых инфекционных заболеваниях, инфекционным лимфоцитозом и инфекционным мононуклеозом.
Лечение и прогноз при остром лимфобластном лейкозе
Основой терапии являются химиопрепараты. Выделяют два этапа лечения ОЛЛ: этап интенсивной терапии и этап поддерживающей терапии. Этап интенсивной терапии острого лимфобластного лейкоза включает в себя две фазы и длится около полугода. В первой фазе осуществляют внутривенную полихимиотерапию для достижения ремиссии. О состоянии ремиссии свидетельствуют нормализация кроветворения, наличие не более 5% бластов в костном мозге и отсутствие бластов в периферической крови. Во второй фазе проводят мероприятия для продления ремиссии, замедления или прекращения пролиферации клеток злокачественного клона. Введение препаратов также осуществляют внутривенно.
Продолжительность этапа поддерживающей терапии при остром лимфобластном лейкозе составляет около 2 лет. В этот период больного выписывают на амбулаторное лечение, назначают препараты для перорального приема, осуществляют регулярные обследования для контроля над состоянием костного мозга и периферической крови. План лечения острого лимфобластного лейкоза составляют индивидуально с учетом уровня риска у конкретного больного. Наряду с химиотерапией используют иммунохимиотерапию, радиотерапию и другие методики. При низкой эффективности лечения и высоком риске развития рецидивов осуществляют трансплантацию костного мозга. Средняя пятилетняя выживаемость при В-клеточном остром лимфобластном лейкозе в детском возрасте составляет 80-85%, во взрослом – 35-40%. При Т-лимфобластном лейкозе прогноз менее благоприятен.
www.krasotaimedicina.ru
gematolog-ro.ru
Острый миелоидный лейкоз — Википедия
Острый миелоидный лейкоз (также ОМЛ, острый нелимфобластный лейкоз, острый миелогенный лейкоз) — это злокачественная опухоль миелоидного ростка крови, при которой быстро размножаются изменённые белые кровяные клетки. Накапливаясь в костном мозге, они подавляют рост нормальных клеток крови, что приводит к снижению количества эритроцитов, тромбоцитов, и нормальных лейкоцитов. Болезнь проявляется быстрой утомляемостью, одышкой, частыми мелкими повреждениями кожи, повышенной кровоточивостью, частыми инфекционными поражениями. До сих пор явная причина заболевания неизвестна, однако некоторые факторы риска его возникновения выявлены. ОМЛ является острым заболеванием, развивается быстро и без лечения приводит к смерти больного за несколько месяцев, иногда — недель.
Это самый распространённый вид острого лейкоза у взрослых, заболеваемость им с возрастом увеличивается. Хотя острый миелоидный лейкоз заболевание относительно редкое — на его долю приходится лишь 1,2 % смертельных случаев злокачественных опухолей в США[3], — ожидается его учащение вместе с постарением населения.
Встречаются несколько разновидностей ОМЛ, лечение и прогноз для них оказывается разным. Уровень выживаемости на протяжении пяти лет колеблется между 15 и 70 %, а частота ремиссии — от 78 до 33 % в зависимости от подвида заболевания. В начале ОМЛ лечат химиопрепаратами для того, чтобы добиться ремиссии; затем может проводиться поддерживающее химиолечение, или проводится пересадка кроветворных стволовых клеток. Последние исследования на генетическом уровне позволили разработать тесты, с помощью которых можно довольно точно определить вероятность выживания больного и эффективность того или иного лекарства для индивидуального случая ОМЛ.[источник не указан 746 дней]
Самые часто используемые схемы классификации ОМЛ — это давняя франко-американо-британская (ФАБ) система и более современная система Всемирной организации здравоохранения (ВОЗ).
Классификация острого миелоидного лейкоза по системе Всемирной системы здравоохранения[править | править код]
Система классификации острого миелоидного лейкоза ВОЗ разработана с учётом системы ФАБ и имеет целью более эффективное клиническое применение и учитывает наиболее прогностически значимые признаки заболевания. Каждый из видов (категорий) ОМЛ по классификации ВОЗ включает в себя несколько подвидов (подкатегорий) описательного характера, представляющих интерес для гематологов и онкологов; однако, бо́льшая часть клинически важной информации в классификации ВОЗ взаимосвязана через распределение по перечисленным ниже подвидам.
Подвиды острого миелоидного лейкоза по классификации ВОЗ:[4]
Название подвида Описание МКБ-О ОМЛ с характерными генетическими изменениями Включает: Несколько ОМЛ с изменениями, связанными с миелодисплазией Этот подвид включает больных с предшествующим миелодиспластическим синдромом (МДС) или миелопролиферативной болезнью (МПБ) или с характерными для него цитогенетическими изменениями. Этот подвид ОМЛ чаще встречается у пожилых людей и отличается неблагоприятным прогнозом.Включает в себя ОМЛ со следующими изменениями:
- Сложный кариотип
- Несбалансированные аномалии
- Сбалансированные аномалии
M9895/3 ОМЛ и МДС, связанные с предыдущим лечением Этот подвид ОМЛ включает больных, получавших химиотерапию и/или лучевое лечение, после которых возник ОМЛ или МДС. При этих лейкозах могут быть характерные изменения в хромосомах, прогноз при них часто бывает хуже. M9920/3 Миелоидная саркома Этот подвид включает больных с миелоидной саркомой Миелопролиферативные заболевания, связанные с Синдромом Дауна Этот подвид включает больных как с кратковременными (преходящими) миелопролиферативными состояниями на фоне синдрома Дауна, так и с ОМЛ на фоне синдрома Дауна Бластная плазмацитоидная дендритноклеточная опухоль Этот подвид включает больных с бластными дендритноклеточными опухолями ОМЛ, не подпадающие под признаки перечисленных подвидов Включает подвиды ОМЛ, не входящие в перечисленные выше, в том числе: M9861/3
Бывают такие подвиды острого лейкоза, при которых изменённые лейкоциты невозможно определить как лимфоциты или гранулоциты, или когда присутствуют злокачественно изменённые клетки обоих ростков. Такие лейкозы иногда называют бифенотипными острыми лейкозами.
Франко-американско-британская классификация[править | править код]
Франко-американско-британская классификационная (ФАБ) система разделяет ОМЛ на 9 подвидов, от М0 по M8, основываясь на типах клеток — предшественниц лейкоцитов, и на степени зрелости изменённых клеток. Определение злокачественных клеток проводят на основании внешних признаков при световой микроскопии и/или цитогенетически, выявляя лежащие в основе отклонений изменения в хромосомах. У разных подвидов ОМЛ разные прогноз и ответ на лечение. Несмотря на преимущества классификации ВОЗ, система ФАБ до сих пор широко применяется.
По ФАБ существует девять подтипов ОМЛ.
Необычные фенотипы острого миелоидного лейкоза[править | править код]
Морфологические подтипы ОМЛ включают многие исключительно редкие подтипы не включённые в классификацию ФАБ. Все они, за исключением острого миелоидного дендритноклеточного лейкоза включены в классификацию ВОЗ. В списке ниже перечислены эти подтипы.
 Инфильтрированная лейкоцитами печень при миелолейкозе
Инфильтрированная лейкоцитами печень при миелолейкозеБо́льшая часть симптомов ОМЛ вызывается замещением нормальных клеток крови лейкозными клетками. Недостаточное образование лейкоцитов обусловливает высокую восприимчивость больного к инфекциям — несмотря на то, что лейкемические клетки происходят от предшественников лейкоцитов, способность противостоять инфектам у них отсутствует.[5] Снижение количества красных кровяных телец (анемия) может вызывать усталость, бледность, и одышку. Недостаток тромбоцитов может привести к легкой повреждаемости кожи и повышенной кровоточивости.
Ранние признаки ОМЛ часто неопределённы и неспецифичны, и могут походить на признаки гриппа или других распространённых болезней. Вот некоторые общие симптомы ОМЛ: лихорадка, усталость, потеря веса или снижение аппетита, одышка, анемия, повышенная повреждаемость кожи и слизистых оболочек и кровоточивость, петехии (плоские, размером с булавочную головку пятнышки внутри кожи на месте кровоизлияний), гематомы, боль в костях и суставах, и стойкие или частые инфекции.[5]
При ОМЛ может быть увеличение селезёнки но обычно оно незначительно и бессимптомно. Увеличение лимфоузлов при ОМЛ случается нечасто, в отличие от острого лимфобластного лейкоза. В 10 % случаев развиваются изменения кожи в виде кожного лейкоза. Изредка при ОМЛ возникает Синдром Свита, он же паранеопластический синдром — воспаление кожи вокруг поражённых хлоромой участков.[5]
У некоторых больных ОМЛ появляется припухлость дёсен из-за инфильтрации тканей лейкозными клетками. Изредка первым признаком лейкоза оказывается хлорома — плотная лейкемическая масса за пределами костного мозга. Иногда заболевание протекает бессимптомно, и лейкоз выявляется общим анализом крови в ходе профилактического осмотра.[6]
Был выявлен ряд факторов, способствующих возникновению ОМЛ — иные расстройства системы кроветворения, воздействие вредных веществ, ионизирующее излучение, и генетическое влияние.
Пре-лейкоз[править | править код]
«Пре-лейкозные нарушения кроветворения, такие, как миелодиспластический синдром или миелопролиферативный синдром могут привести к ОМЛ; вероятность заболевания зависит от формы миелодиспластического или миелопролиферативного синдрома.[7]
Воздействие химических веществ[править | править код]
Противоопухолевое химиотерапевтическое воздействие, особенно алкилирующими веществами, может увеличивать вероятность возникновения ОМЛ в последующем. Наивысшая вероятность заболевания приходится на 3—5 лет после химиотерапии.[8] Другие химиотерапевтические препараты особенно эпиподофилотоксины и антрациклины, также связываются с постхимиотерапевтическими лейкозами. лейкозы такого вида часто объясняют специфическими изменениями в хромосомах лейкозных клеток.[9]
Воздействие бензола и других ароматических органических растворителей, связанное с профессиональной деятельностью, в качестве возможной причины ОМЛ остаётся спорным. Бензол и многие его производные проявляют канцерогенные свойства in vitro. Данные некоторых наблюдений подтверждают возможность влияния профессиональных контактов с этими веществами на вероятность развития ОМЛ, однако другие исследования подтверждают, что если и существует такая опасность, то она является лишь добавочным фактором.[10][11]
Ионизирующее излучение[править | править код]
Воздействие ионизирующего излучения повышает вероятность заболеваня ОМЛ. У переживших атомную бомбардировку Хиросимы и Нагасаки заболеваемость ОМЛ повышена,[12] так же как у рентгенологов, получивших высокие дозы рентгеновского излучения в то время, когда меры радиологической защиты были недостаточными.[13]
Генетические факторы[править | править код]
Вероятно, существует наследственно повышенная вероятность заболевания ОМЛ. Есть большое количество сообщений о множестве семейных случаев ОМЛ, когда заболеваемость превышала среднестатистическую.[14][15][16][17] Вероятность возникновения ОМЛ у ближайших родственников больного втрое выше.[18]
Ряд врождённых состояний может повышать вероятность ОМЛ. Чаще всего это синдром Дауна, при котором вероятность ОМЛ повышена в 10 — 18 раз.[19]
Изменения соотношения клеточных элементов в общем анализе крови — первое, что наводит на мысль о возможности ОМЛ. Наиболее частым оказывается лейкоцитоз- повышение общего количества лейкоцитов, иногда с появлением бластных (незрелых) форм, но бывает так, что ОМЛ проявляется изолированным снижением тромбоцитов, эритроцитов, а количество лейкоцитов может оказаться даже сниженным (лейкопения).[20] Предварительный диагноз ОМЛ может быть определён в случае выявления в мазках периферической крови бластных форм лейкоцитов, но для окончательного диагноза должны быть выявлены соответствующие изменения в анализе аспирационного биоптата костного мозга.
Костный мозг и кровь исследуют световым микроскопированием и поточной цитометрией для установления диагноза и дифференцирования ОМЛ от других лейкозов, например, от острого лимфобластного лейкоза, а также для уточнения подтипа ОМЛ. Образец крови или костного мозга обычно проверяют на присутствие хромосомных транслокаций обычными цитогененитческими способами, или способом флуоресцентной гибридизации in situ. Генетические исследования проводят и для выявления характерных мутаций, которые могут влиять на исход заболевания — например, в FLT3, в нуклеоплазмине, или в KIT.[21]
Цитохимические красители для мазков крови и костного мозга оказываются очень полезными для дифференциальной диагностики ОМЛ и ОЛЛ, а также для выделения подтипов ОМЛ. Сочетание миелопероксидазы или красителя Суданский чёрный и неспцифического эстеразного красителя обеспечивает получение нужной информации в большинстве случаев. Реакции миелопероксидазы или Суданского чёрного оказываются самыми полезными для установления диагноза ОМЛ и его дифференцирования от ОЛЛ. Неспецифический краситель эстеразы используется для моноцитаронй составляющей острых миелолейкозов и для дифференцирования от незрелой формы монобластного лейкоза от ОЛЛ.[4]
Диагноз и классификация ОМЛ может оказаться непростой задачей, этим должен должен заниматься квалифицированный гематопатолог или гематолог. В явных случаях наличие некоторых характерный морфологических признаков, таких, как тельца Ауэра, или специфическия для АМЛ результаты поточной цитометрии дают возможность надёжно отделять ОМЛ от других лейкозов; однако при отсутствии такх явных признаков диагностика существенно осложняется.[22]
В соответствии с широко используемыми критериями классификации ВОЗ диагноз ОМЛ устанавливаетсяв том случае, если доказано если в крови и/или костном мозге более 20 % клеток представлены миелобластами.[23] ОМЛ следует тщательно дифференцировать от так называемых прелейкозных состояний, в частности, от миелодиспластического синдрома или миелопролиферативного синдрома, которые лечатся по-разному.
Поскольку острый промиелоцитарный лейкоз (ОПЛ), требуя уникального способа лечения очень хорошо ему поддаётся, очень важно быстро подтвердить или отвергнуть этот подвид лейкоза. Для этого часто используют флюоресцентную гибридизацию in situ, выполненную на крови или костном мозге, поскольку ею легко выявляется хромосомная транслокация (t[15;17]) специфичная для ОПЛ.[24]
Злокачественными клетками при ОМЛ выступают миелобласты. В нормальном гемопоэзе миелобласты являются незрелыми предшественниками лейкоцитов миелоидного ряда;нормальные миелобласты постепенно созревают, превращаясь в нормальные лейкоциты. Однако при ОМЛ в каком — то из миелобластов накапливаются генетические изменения, которые «замораживают» клетку в незрелом состоянии, останавливая процесс клеточной дифференциации. [25] Сама по себе такая мутация не вызывает лейкоз, но когда «остановка дифференциации» сочетается с другими мутациями, которые приводят к утрате генетического контроля над ростом клеток, результатом оказывается неуправляемое размножение незрелого клеточного клона, определяющего клиническую сущность ОМЛ.[26]
Большое разнообразие и генетическая неоднородность ОМЛ происходит от того, что лейкозная трансформация может возникнуть на множестве этапов дифференциации клетки.[27] Современные схемы классификации ОМЛ признают факт зависимости свойств и поведения лейкозных клеток, а также течения лейкоза от того, на каком этапе остановилась дифференциация.
Специфические цитогенетическиеотклонения обнаруживаются у многих больных ОМЛ. Виды изменений хромосом часто прогностически значимы.[28] Хромосомные транслокации кодируют синтез гибридных белков, чаще всего, факторов транскрипции — вспомогательных белков — помощников РНК-полимераз, изменённые свойства которых могут привести к останову дифференциации.[29] Например, при остром промиелоцитарном лейкозе транслокация t(15; 17) вызывает синтез гибридного протеина PML-RARα, который связывается с рецептором ретиноевой кислоты в промоторах некоторых специфических для миелоидных клеток генов и останавливает в этих клетках дифференциацию.[30]
Схема транслокации хромосом.Клинические проявления и симптомы ОМЛ возникают потому что, умножаясь, клетки лейкозного клона мешают деятельности нормальных клеток и стремятся вытеснить их из костного мозга.[31] Это приводит к нейтропении, анемии, и тромбоцитопении. Чаще всего симптомы ОМЛ определяются недостаточностью нормальных клеток крови. В редких случаях у больных развиваются хлоромы — плотные опухоли из лейкозных клеток за прелами костного мозга, которые могут вызывать различные симптомы в зависимости от локализации хлоромы.[5]
Лечение ОМЛ состоит в основном из химиотерапии, и делится на два этапа: индукция и постремиссионное лечение(или консолидация). Цель индукционной терапии является достижение полной ремиссии за счет уменьшения количества лейкозных клеток до не обнаруживаемого уровня; цель консолидирующей терапии заключается в ликвидации остаточных, не обнаруживаемых современными методами остатками болезни и излечение.[32]
Индукция[править | править код]
Для всех подтипов ОМЛ за исключением M3 по классификации ФАБ, обычно используют индукционную химиотерапию цитарабином и антрациклиновым антибиотиком (например, даунорубицином или идарубицином).[33] Этот способ индукционной химиотерапии известен под названием «7+3». Название происходит от того, что в этом режиме предусматриваются 7 дней непрерывного инфузионного вливания цитарабина, при этом в первые три дня одновременно болюсно вводится антрациклиновый антибиотик. При таком способе лечения ремиссия наступает почти у 70 % больных ОМЛ.[34] Могут применяться и другие способы индукционного лечения, включая режимы FLAG, DAT, ADE и подобные, или монотерапию высокими дозами цитарабина, или лечение препаратами, находящимися на стадии исследования.[35][36] Вследствие токсического воздействия лечения, в том числе подавления миелоидного ростка и повышения вероятности инфекционных осложнений очень старым больным индукционная химиотерапия не предлагается, и назначается менее интенсивное паллиативное лечение химиопрепаратами.
Подвид ОМЛ M3, также известный под названием острый промиелоцитарный лейкоз, почти во всех случаях лечится препаратом ПТРК (полностью транс- ретиноевая кислота) в дополнение к индукционной терапии.[37][38][39] При лечении острого промиелоцитарного лейкоза нужно учитывать возможность развития синдрома диссеминированного внутрисосудистого свёртывания вследствие поступления содержимого гранул промиелоцитов в периферическую кровь. Лечение острого промиелоцитарного лейкоза исключительно эффективно, это достоверно доказано множеством документированных случаев лечения.
3 августа 2017 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США(FDA) одобрило к применению VYXEOS (Jazz Pharmaceuticals, Inc) для лечения взрослых с недавно диагностированными двумя подвидами ОМЛ (t- AML и AML-MRC). VYXEOS представляет собой липосомальную комбинацию цитарабина и даунорубицина и показало себя намного эффективнее при лечении этих двух подтипов , чем применение стандартной 7+3 комбинации. Лекарство продемонстрировало среднюю общую выживаемость 9,6 месяцев по сравнению с 5,9 месяцами при комбинации 7+3 [40]
В 2018 году FDA одобрила применение гласдегиба (glasdegib) в комбинации с низкодозным цитарабином для лечения пациентов в возрасте старше 75 лет, которым невозможно провести интенсивную химиотерапию. Одобрение препарат получил с условием размещения в инструкции предупреждения о высоком риске токсичности для плода.[41]
Целью индукционного этапа лечения является достижение полной ремиссии. Полная ремиссия не означает, что заболевание полностью вылечено. Скорее, состояние полной ремиссии говорит о невозможности обнаружить спящую болезнь существующими способами диагностики.[33] Полная ремиссия достигается у 50-70 % взрослых больных с впервые выявленным ОМЛ, разница зависит от прогностических факторов, о которых сказано выше.[42] Длительность ремиссии зависит от прогностических качеств исходного лейкоза. В основном, все случаи ремиссии без дополнительного, консолидирующего лечения закачиваются рецидивом.[43]
Консолидационное лечение[править | править код]
Даже после достижения полной ремиссии вероятно, немногие лейкозные клетки всё же выживают. Их так мало, что обнаружить их пока невозможно. В случае не проведения послеремиссионно
ru.wikipedia.org
Острый лимфобластный лейкоз — причины, симптомы, диагностика и лечение, прогноз
Острый лимфобластный лейкоз – злокачественное поражение системы кроветворения, сопровождающееся неконтролируемым увеличением количества лимфобластов. Проявляется анемией, симптомами интоксикации, увеличением лимфоузлов, печени и селезенки, повышенной кровоточивостью и дыхательными расстройствами. Из-за снижения иммунитета при остром лимфобластном лейкозе часто развиваются инфекционные заболевания. Возможно поражение ЦНС. Диагноз выставляется на основании клинических симптомов и данных лабораторных исследований. Лечение – химиотерапия, радиотерапия, пересадка костного мозга.
Общие сведения
Острый лимфобластный лейкоз (ОЛЛ) – самое распространенное онкологическое заболевание детского возраста. Доля ОЛЛ составляет 75-80% от общего количества случаев болезней системы кроветворения у детей. Пик заболеваемости приходится на возраст 1-6 лет. Мальчики страдают чаще девочек. Взрослые пациенты болеют в 8-10 раз реже детей. У пациентов детского возраста острый лимфобластный лейкоз возникает первично, у взрослых нередко является осложнением хронического лимфоцитарного лейкоза. По своим клиническим проявлениям ОЛЛ схож с другими острыми лейкозами. Отличительной особенностью является более частое поражение оболочек головного и спинного мозга (нейролейкоз), при отсутствии профилактики развивающееся у 30-50% пациентов. Лечение осуществляют специалисты в области онкологии и гематологии.
В соответствии с классификацией ВОЗ различают четыре типа ОЛЛ: пре-пре-В-клеточный, пре-В-клеточный, В-клеточный и Т-клеточный. В-клеточные острые лимфобластные лейкозы составляют 80-85% от общего количества случаев заболевания. Первый пик заболеваемости приходится на возраст 3 года. В последующем вероятность развития ОЛЛ повышается после 60 лет. Т-клеточный лейкоз составляет 15-20% от общего количества случаев болезни. Пик заболеваемости приходится на возраст 15 лет.
Острый лимфобластный лейкоз
Причины острого лимфобластного лейкоза
Непосредственной причиной острого лимфобластного лейкоза является образование злокачественного клона – группы клеток, обладающих способностью к неконтролируемому размножению. Клон образуется в результате хромосомных аберраций: транслокации (обмена участками между двумя хромосомами), делеции (утраты участка хромосомы), инверсии (переворота участка хромосомы) или амплификации (образования дополнительных копий участка хромосомы). Предполагается, что генетические нарушения, вызывающие развитие острого лимфобластного лейкоза, возникают еще во внутриутробном периоде, однако для завершения процесса формирования злокачественного клона нередко требуются дополнительные внешние обстоятельства.
В числе факторов риска возникновения острого лимфобластного лейкоза обычно в первую очередь указывают лучевые воздействия: проживание в зоне с повышенным уровнем ионизирующей радиации, радиотерапию при лечении других онкологических заболеваний, многочисленные рентгенологические исследования, в том числе во внутриутробном периоде. Уровень связи, а также доказанность наличия зависимости между различными лучевыми воздействиями и развитием острого лимфобластного лейкоза сильно различаются.
Так, взаимосвязь между лейкозами и лучевой терапией в наши дни считается доказанной. Риск возникновения острого лимфобластного лейкоза после радиотерапии составляет 10%. У 85% пациентов болезнь диагностируется в течение 10 лет после окончания курса лучевой терапии. Связь между рентгенологическими исследованиями и развитием острого лимфобластного лейкоза в настоящее время остается на уровне предположений. Достоверных статистических данных, подтверждающих эту теорию, пока не существует.
Многие исследователи указывают на возможную связь между ОЛЛ и инфекционными заболеваниями. Вирус возбудителя острого лимфобластного лейкоза пока не выявлен. Существуют две основные гипотезы. Первая – ОЛЛ вызывается одним пока не установленным вирусом, однако болезнь возникает только при наличии предрасположенности. Вторая – причиной развития острого лимфобластного лейкоза могут стать разные вирусы, риск развития лейкоза у детей повышается при недостатке контактов с патогенными микроорганизмами в раннем возрасте (при «нетренированности» иммунной системы). Пока обе гипотезы не доказаны. Достоверные сведения о наличии связи между лейкозами и вирусными заболеваниями получены только для Т-клеточных лейкозов у взрослых больных, проживающих в странах Азии.
Вероятность развития острого лимфобластного лейкоза повышается при контакте матери с некоторыми токсическими веществами в период гестации, при некоторых генетических аномалиях (анемии Фанкони, синдроме Дауна, синдроме Швахмана, синдроме Клайнфельтера, синдроме Вискотта-Олдрича, нейрофиброматозе, целиакии, наследственно обусловленных иммунных нарушениях), наличии онкологических заболеваний в семейном анамнезе и приеме цитостатиков. Некоторые специалисты отмечают возможное негативное влияние курения.
Симптомы острого лимфобластного лейкоза
Болезнь развивается стремительно. К моменту постановки диагноза суммарная масса лимфобластов в организме может составлять 3-4% от общей массы тела, что обусловлено бурной пролиферацией клеток злокачественного клона на протяжении 1-3 предыдущих месяцев. В течение недели количество клеток увеличивается примерно вдвое. Различают несколько синдромов, характерных для острого лимфобластного лейкоза: интоксикационный, гиперпластический, анемический, геморрагический, инфекционный.
Интоксикационный синдром включает в себя слабость, утомляемость, лихорадку и потерю веса. Повышение температуры может провоцироваться как основным заболеванием, так и инфекционными осложнениями, которые особенно часто развиваются при наличии нейтропении. Гиперпластический синдром при остром лимфобластном лейкозе проявляется увеличением лимфоузлов, печени и селезенки (в результате лейкемической инфильтрации паренхимы органов). При увеличении паренхиматозных органов могут появляться боли в животе. Увеличение объема костного мозга, инфильтрация надкостницы и тканей суставных капсул могут становиться причиной ломящих костно-суставных болей.
О наличии анемического синдрома свидетельствуют слабость, головокружения, бледность кожи и учащение сердечных сокращений. Причиной развития геморрагического синдрома при остром лимфобластном лейкозе становятся тромбоцитопения и тромбозы мелких сосудов. На коже и слизистых выявляются петехии и экхимозы. При ушибах легко возникают обширные подкожные кровоизлияния. Наблюдаются повышенная кровоточивость из ран и царапин, кровоизлияния в сетчатку, десневые и носовые кровотечения. У некоторых больных острым лимфобластным лейкозом возникают желудочно-кишечные кровотечения, сопровождающиеся кровавой рвотой и дегтеобразным стулом.
Иммунные нарушения при остром лимфобластном лейкозе проявляются частым инфицированием ран, царапин и следов от уколов. Могут развиваться различные бактериальные, вирусные и грибковые инфекции. При увеличении лимфатических узлов средостения отмечаются нарушения дыхания, обусловленные уменьшением объема легких. Дыхательная недостаточность чаще обнаруживается при Т-клеточном остром лимфобластном лейкозе. Нейролейкозы, спровоцированные инфильтрацией оболочек спинного и головного мозга, чаще отмечаются во время рецидивов.
При вовлечении ЦНС выявляются положительные менингеальные симптомы и признаки повышения внутричерепного давления (отек дисков зрительных нервов, головная боль, тошнота и рвота). Иногда поражение ЦНС при остром лимфобластном лейкозе протекает бессимптомно и диагностируется только после исследования цереброспинальной жидкости. У 5-30% мальчиков появляются инфильтраты в яичках. У пациентов обоих полов на коже и слизистых оболочках могут возникать багрово-синюшные инфильтраты (лейкемиды). В редких случаях наблюдаются выпотной перикардит и нарушения функции почек. Описаны случаи поражений кишечника.
С учетом особенностей клинической симптоматики можно выделить четыре периода развития острого лимфобластного лейкоза: начальный, разгара, ремиссии, терминальный. Продолжительность начального периода составляет 1-3 месяца. Преобладает неспецифическая симптоматика: вялость, утомляемость, ухудшение аппетита, субфебрилитет и нарастающая бледность кожи. Возможны головные боли, боли в животе, костях и суставах. В период разгара острого лимфобластного лейкоза выявляются все перечисленные выше характерные синдромы. В период ремиссии проявления болезни исчезают. Терминальный период характеризуется прогрессирующим ухудшением состояния больного и завершается летальным исходом.
Диагностика острого лимфобластного лейкоза
Диагноз выставляют с учетом клинических признаков, результатов анализа периферической крови и данных миелограммы. В периферической крови пациентов с острым лимфобластным лейкозом выявляются анемия, тромбоцитопения, повышение СОЭ и изменение количества лейкоцитов (обычно – лейкоцитоз). Лимфобласты составляют 15-20 и более процентов от общего количества лейкоцитов. Количество нейтрофилов снижено. В миелограмме преобладают бластные клетки, определяется выраженное угнетение эритроидного, нейтрофильного и тромбоцитарного ростка.
В программу обследования при остром лимфобластном лейкозе входят люмбальная пункция (для исключения нейролейкоза), УЗИ органов брюшной полости (для оценки состояния паренхиматозных органов и лимфатических узлов), рентгенография грудной клетки (для обнаружения увеличенных лимфоузлов средостения) и биохимический анализ крови (для выявления нарушений функции печени и почек). Дифференциальный диагноз острого лимфобластного лейкоза проводят с другими лейкозами, отравлениями, состояниями при тяжелых инфекционных заболеваниях, инфекционным лимфоцитозом и инфекционным мононуклеозом.
Лечение и прогноз при остром лимфобластном лейкозе
Основой терапии являются химиопрепараты. Выделяют два этапа лечения ОЛЛ: этап интенсивной терапии и этап поддерживающей терапии. Этап интенсивной терапии острого лимфобластного лейкоза включает в себя две фазы и длится около полугода. В первой фазе осуществляют внутривенную полихимиотерапию для достижения ремиссии. О состоянии ремиссии свидетельствуют нормализация кроветворения, наличие не более 5% бластов в костном мозге и отсутствие бластов в периферической крови. Во второй фазе проводят мероприятия для продления ремиссии, замедления или прекращения пролиферации клеток злокачественного клона. Введение препаратов также осуществляют внутривенно.
Продолжительность этапа поддерживающей терапии при остром лимфобластном лейкозе составляет около 2 лет. В этот период больного выписывают на амбулаторное лечение, назначают препараты для перорального приема, осуществляют регулярные обследования для контроля над состоянием костного мозга и периферической крови. План лечения острого лимфобластного лейкоза составляют индивидуально с учетом уровня риска у конкретного больного. Наряду с химиотерапией используют иммунохимиотерапию, радиотерапию и другие методики. При низкой эффективности лечения и высоком риске развития рецидивов осуществляют трансплантацию костного мозга. Средняя пятилетняя выживаемость при В-клеточном остром лимфобластном лейкозе в детском возрасте составляет 80-85%, во взрослом – 35-40%. При Т-лимфобластном лейкозе прогноз менее благоприятен.
www.krasotaimedicina.ru
Включает в себя ОМЛ со следующими изменениями:
- Сложный кариотип
- Несбалансированные аномалии
- Сбалансированные аномалии

 Инфильтрированная лейкоцитами печень при миелолейкозе
Инфильтрированная лейкоцитами печень при миелолейкозе