6.5. Система регуляции агрегатного состояния крови (раск)
Система РАСК — это система организма, которая обеспечивает: 1) сохранение жидкого состояния крови в норме; 2) свертывание крови в экстремальных состояниях; 3) своевременное восстановление стенок капилляров и других сосудов, которые повреждаются под действием тех или иных факторов. В настоящее время существует много противоречивых определений процессов свертывания крови и системы (систем), обеспечивающих остановку кровотечения, антисвертывание и фибринолиз. Идет дискуссия о целесообразности выделять отдельные системы или подсистемы. С введением понятия «система РАСК» (имеется одна система) существующая проблема решается путем выделения основных механизмов деятельности системы РАСК: 1) механизмы гемостаза обеспечивают остановку кровотечения; 2) механизмы антисвертывания поддерживают жидкое состояние крови; 3) механизмы фибринолиза обеспечивают растворение тромба (кровяного сгустка) и восстановление просвета сосуда (рекана-лизация).
138
139
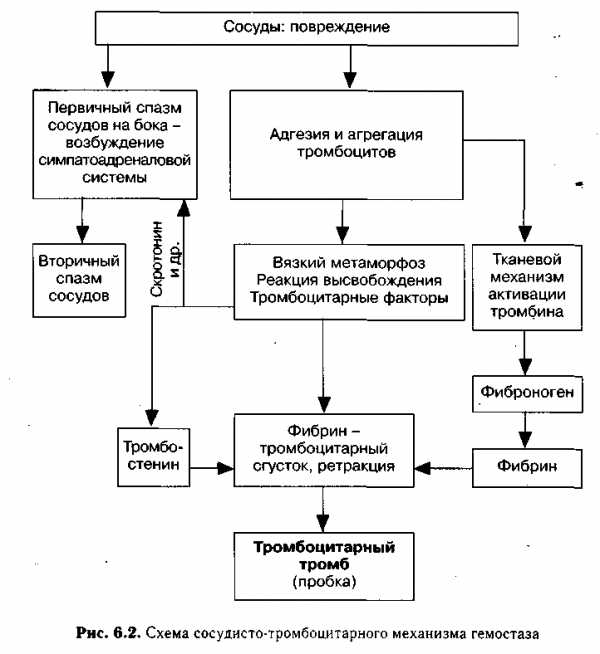
Сосудисто-тромбоцитарный гемостаз
140
Этот вид гемостаза называют также первичным, он обеспечивает остановку кровотечения из мелких сосудов с низким кровяным давлением, диаметр которых не превышает 100 мкм. В норме кровотечение из мелких сосудов останавливается в течение 2-4 мин. Сосудисто-тромбоцитарный гемостаз осуществляется с помощью образования тромбоцитарной пробки (тромбоцитарного тромба). Он проходит в три стадии (рис. 6.2).1. Первичный спазм сосудов обусловлен выбросом в кровь в ответ на болевое раздражение адреналина и норадреналина и длит ся не более 10-15 с. В дальнейшем наступает вторичный спазм сосудов, обусловленный активацией тромбоцитов и отдачей в кровь сосудосуживающих агентов — адреналина, серотонина. Поврежде ние сосудов сопровождается немедленной активацией тромбоци тов, что обусловлено появлением высоких концентраций АДФ (из разрушающихся эритроцитов и травмированных сосудов), а также с обнажением субэндотелия, коллагеновых и фибриллярных струк тур. В результате создаются условия для адгезии, агрегации и об разования тромбоцитарной пробки.
Образование тромбоцитарной пробки. Адгезия тромбоцитов обусловлена наличием в плазме и тромбоцитах особого белка — фактора Виллебранда (Р\\0. Одновременно с адгезией происходит агрегация тромбоцитов, осуществляемая с помощью фибриногена — белка, содержащегося в плазме и тромбоцитах и образующего между ними связующие мостики, что и приводит к появлению тромбоцитарной пробки. Агрегация тромбоцитов может быть обратимой, что зависит от недостаточной дозы агрегирующего (активирующего) агента. Из тромбоцитов, подвергшихся адгезии и агрегации, усиленно секретируются гранулы и содержащиеся в них биологически активные соединения — АДФ, адреналин, норадреналин, серотонин и др., что приводит к вторичной, необратимой агрегации. Одновременно с высвобождением тромбоцитарных факторов происходит образование тромбина, резко усиливающего агрегацию и приводящего к появлению сети фибрина, в которой застревают эритроциты и лейкоциты. При этом тромбоциты подтягиваются друг к другу, тромбоцитарная пробка сокращается и уплотняется.
Ретракция тромбоцитарной пробки осуществляется благодаря контрактильному белку тромбостенину.
Существенную роль в сосудисто-тромбоцитарном гемостазе играют производные арахидоновой кислоты.
Коагуляционный механизм гемостаза
Коагуляционный (вторичный) гемостаз осуществляется с помощью свертывания крови (гемокоагуляции). При этом растворимый белок плазмы крови фибриноген переходит в нерастворимое состояние — фибрин, в результате чего образуется студнеобразный сгусток, закрывающий просвет поврежденного сосуда. В свертывании крови принимают участие много факторов свертывания крови. Они содержатся в плазме крови, форменных элементах и в тканях. Как правило, плазменные факторы свертывания крови об-
141
разуются в печени, и для образования большинства из них необходим витамин К. Плазменные факторы обозначаются римскими цифрами. Все факторы свертывания крови — в основном белки, большинство из них являются ферментами, в крови находятся в неактивном состоянии, активируются друг другом в процессе свертывания крови. Активные факторы обозначаются с буквой а, например, 1а, Па и т.д.
Фактор I (фибриноген) — белок плазмы крови, под влиянием тромбина переходит в фибрин, волокна которого составляют основу тромба. Принимает участие в агрегации тромбоцитов.
Фактор III (тромбопластин) входит в состав мембран клеток всех тканей и форменных элементов крови. Активирует фактор VII и, вступая с ним в комплекс, переводит фактор X в Ха. В плазме в физиологических условиях практически не содержится.
Фактор IV (Са2+) участвует в образовании комплексов факторов свертывания крови, входит в состав протромбиназы. Способствует агрегации тромбоцитов, связывает гепарин. Принимает участие в ретракции сгустка и тромбоцитарной пробки, тормозит фибринолиз.
Фактор V (проакцелерин) — глобулин, активируется тромбином. Усиливает действие фактора Ха на протромбин (входит в состав протромбиназы).
Фактор VI исключен из классификации, так как это фактор Уа.
Фактор VII (проконвертин) принимает участие в формировании протромбиназы по внешнему механизму. Активируется факторами III, ХНа, 1Ха, Ха.
Фактор VIII (антигемофилъный глобулин А)
Фактор IX (антигемофилъный глобулин В) активирует факторы X и VII.
Фактор X (Стюарта — Прауэра) является составной частью протромбина.
Фактор XI (предшественник тромбопластина) активируется фактором ХПа. Необходим для активации фактора IX.
Фактор XII (Хагемана, или контакта)
142
Фактор XIII (фибринстабилизирующий фактор, фибри-наза). Содержится практически во всех тканях и форменных элементах. Стабилизирует фибрин.
Фактор XIV (фактор Флетчера — прокалликреин). Участвует в активации факторов XII, IX и плазминогена. Переводит кининоген в кинин. Активируется фактором ХПа.
143
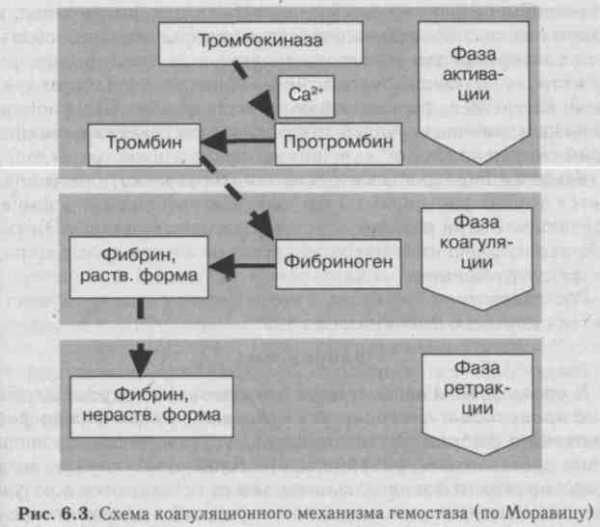
Процесс свертывания крови — это ферментативный, цепной (каскадный), матричный процесс перехода растворимого белка фибриногена в нерастворимый фибрин. Каскадным он называется потому, что в процессе гемокоагуляции происходит последовательная цепная активация факторов свертывания крови. Свертывание крови является матричным процессом, так как активация факторов гемокоагуляции осуществляется на матрице. Матрицей могут быть фосфолипиды мембран разрушенных форменных элементов (главным образом тромбоцитов) и обломки клеток тканей. Процесс свертывания крови осуществляется
Первая фаза — образование протромбиназы — может проходить по внешнему и внутреннему механизму. Внешний механизм предполагает обязательное присутствие тромбопластина (фактор III), внутренний же связан с участием тромбоцитов (фактор Р3) или разрушенных эритроцитов. Вместе с тем внутренний и внешний пути образования протромбиназы имеют много общего, так как активируются одними и теми же факторами и приводят в конечном итоге к появлению одного и того же активного фермента — фактора Ха, выполняющего функции протромбиназы. При этом тромбопла-стин служит матрицей, на которой в присутствии ионов Са
Вторая фаза процесса свертывания крови — переход фактора II в фактор Па — осуществляется под влиянием протромбиназы (фактор Ха) в присутствии фактора Уа и сводится к проте-олитическому расщеплению протромбина, благодаря чему появляется активный фермент тромбин.
Третья фаза процесса свертывания крови — переход фибриногена в фибрин — протекает в три этапа. На первом этапе под влиянием фактора Па от фибриногена отщепляются фибринопеп-тиды и образуется фибрин-мономер (фактор 1т). На втором, неферментативном, этапе благодаря процессу полимеризации фибрина-мономера формируются олигомеры и димеры фибрина, из которых за счет продольного и поперечного связывания образуются протофибриллы — легкорастворимый фибрин, или фибрин 5, быстро лизирующийся под влиянием протеаз (плазмина, трипсина). На третьем, ферментативном, этапе фактор XIII (фибрина-за, фибринстабилизирующий фактор) после активации тромбином в присутствии ионов Са2+ «прошивает» фибринополимеры дополнительными перекрестными связями, в результате чего появляется трудно растворимый фибрин, или фибрин 1 0п5о1иЫе). В результате этой реакции сгусток становится резистентным к фибринолитическим (протеолитическим) агентам и плохо поддается разрушению.
Восстановление кровотока в поврежденном сосуде осуществляется с помощью фибринолиза.
studfile.net
СИСТЕМА РЕГУЛЯЦИИ АГРЕГАТНОГО СОСТОЯНИЯ КРОВИ И ТРОМБОГЕМОРРАГИЧЕСКИЙ СИНДРОМ
Система свёртывания крови входит в состав функциональной системы — системы регуляции агрегатного состояния крови (система РАСК), которая поддерживает гомеостаз внутренней среды организма и её агрегатное состояние на таком уровне, который необходим для нормальной жизнедеятельности. Система РАСК обеспечивает жидкое состояние крови и восстановление стенок сосудов, изменяющихся даже при нормальном функционировании. Она же поддерживает на оптимальном уровне содержание факторов свёртывания на случай катастрофы — повреждения сосудов, органов и тканей.
Конечным результатом действия системы РАСК, является гемостатический потенциал, адекватный внешним и внутренним условиям существования организма.
Система РАСК мозаична, то есть гемостатические потенциалы в различных участках кровотока и органах неодинаковы. Это естественное, нормальное состояние этой функциональной системы.
Основные компоненты системы РАСК
Центральные органы. К ним относятся костный мозг, печень и селезенка. Костный мозг продуцирует клеточные компоненты системы гемостаза: тромбоциты, эритроциты, лейкоциты. В печени синтезируются плазменные факторы, участвующие в образовании тромбов и их лизисе, такие как: фибриноген, протромбин, проконвертин, IX, X и др. Селезенка влияет на гемопоэз в костном мозге и выход клеток крови из костного мозга в кровоток. В ней осуществляется эритродиерез. Селезенка регулирует тромбоцитопоэз.
Периферические органы. Это сосудистая стенка и кровь. Эндотелий сосудовсинтезирует и выделяет в кровоток простациклин, компоненты кинин-каллекреиновой системы, фосфолипиды. Клетки крови выделяют в плазму тромбопластические и другие вещества, участвующие в свертывании крови. Тромбоциты играют роль клеточного триггера в системе гемостаза.
Регулирующий аппарат. Местные регуляторы. Главными местными регуляторами являются хемо- и барорецептивные зоны сосудов различных органов. Внутренние органы и мышцы способны продуцировать тромбопластин, прокоагулянты, активаторы и ингибиторы фибринолиза.
Центральные регуляторы: гормоны желез внутренней секреции, вегетативная нервная система, ЦНС. Кора головного мозга осуществляет афферентный синтез сигналов, поступающих с периферии и свидетельствующих о состоянии гемостатических потенциалов в любом органе, участке кровотока. Эндокринная система через соответствующие рецепторы клеток влияет на синтез факторов свертывания крови и фибринолиза.
Все компоненты системы РАСК взаимосвязаны. Взаимодействуя, они в естественных условиях обеспечивают соответствующий гемостатический потенциал. Нарушения морфологии и функций образующих её частей приводят к патологии этой системы. Кроме того, любой вид патологии влияет на систему РАСК.
При многих заболеваниях, сопровождающихся разрушением эритроцитов, лейкоцитов, тромбоцитов и тканей и/или гиперпродукцией апопротеина III стимулированными эндотелиоцитами, моноцитами и макрофагами, развивается ДВС-синдром, который значительно отягощает течение патологического процесса и даже приводит к смерти больного. Наиболее часто ДВС-синдром возникает при переливании несовместимой крови, обширных травмах, отморожениях, ожогах, длительных оперативных вмешательствах на лёгких, печени, сердце, предстательной железе, всех видах шока, краш-синдроме (длительное сдавление конечностей), а также в акушерской практике при попадании в кровоток матери околоплодных вод, насыщенных тромбопластином плацентарного происхождения. При этом возникает гиперкоагулемия, которая из-за интенсивного потребления тромбоцитов, факторов I, V, VIII, XIII в результате внутрисосудистого свёртывания крови сменяется вторичной гипокоагулемией вплоть до полной неспособности крови к образованию фибрина, что приводит к трудно поддающимся терапии кровотечениям.
Эти динамичные нарушения свёртывания крови подробно изучены М.С. Мачабели, которая создала учение о синдромности нарушений гемостаза — о тромбогеморрагическом синдроме (ТГС). ТГС является обязательным компонентом любого заболевания. Его первопричиной являются нарушения электрообмена в организме (уменьшение мембранного потенциала клеточных структур). ТГС развивается и в тканях, и в крови в 4 последовательные стадии.
1. Гиперкоагулемия. Уменьшается отрицательный заряд, наблюдается гипоксия, дистрофия с освобождением тканевого тромбопластина и ионов кальция во внутри- и внеклеточные среды. В клетках это проявляется изменением коллоидного состояния цитоплазмы в сторону геля, а в кровотоке — гиперкоагулемией.
2. Нарастающая коагулопатия потребления. Происходит коагуляция клеточных структур под влиянием тканевого тромбопластина и ионов кальция в результате продолжающегося падения электрического заряда в форме обратимой дистрофии. В кровотоке вследствие поступления тканевого тромбопластина развивается гиперкоагулемия и внутрисосудистое свёртывание, слайдж-синдром и тромбоэмболии во многих органах.
3. Гипокоагуляция и вторичный фибринолиз. Наблюдается местная или диффузная потеря отрицательного заряда с необратимым расслоением клеточных структур, повреждение мембран, развитие кариолизиса и плазмолизиса. В кровотоке продолжается интравазальная гемокоагуляция и защитная активация фибринолиза (последний процесс наблюдается не всегда).
4. Восстановительная стадия. Она проявляется либо восстановлением физиологического состояния, либо необратимой дистрофией, либо некрозом с последующей соединительно-тканной организацией.
Первые 2 стадии могут перейти в 4-ю, минуя самую тяжёлую 3-ю. Во время 2-й и 3-й стадий развивается ДВС-синдром, который проявляется профузными кровотечениями.
Моделирование ТГС и его изучение при различных состояниях проводили в лаборатории нашей кафедры ассистенты: Н. С. Русейкин, И. И. Азрапкин, Г. Ф. Вдовина; врач Л. В. Костюнина, аспирант С. П. Голышенков и многие другие сотрудники и соискатели под руководством профессора, доктора медицинских наук В. П. Скипетрова.
ТГС — это проявление полного рассогласования в системе РАСК. Высшей формой такого рассогласования при ТГС является нивелировка гемостатического потенциала во всех участках кровотока — это катастрофа для организма (тотальный фибринолиз и несвёртывамость крови). Даже погибая, организм стремится сохранить жидкое состояние крови. Поэтому эту последнюю фазу можно назвать фазой полного паралича системы РАСК.
Знание основ физиологии гемостаза позволяет клиницисту избрать оптимальные варианты борьбы с заболеваниями, сопровождающимися тромбозами, тромбоэмболиями, повышенной кровоточивостью, т. е. влиять на все стадии ТГС.
studopedia.net
Система резус (Rh) и другие
В 1940 г. К.Ландштейнер и А.Винер обнаружили в эритроцитах обезьяны макаки- резус антиген, названный ими резус–фактором.Оказалось, что примерно у 85 % людей имеется такой же антиген на эритроцитах – это резус-положительная группа (Rh+) и около 15 % людей такого антигена не имели (Rh-).В крови людей в норме нет антител-агглютининов против резус-антигенов , но они могут появиться, если резус-отрицательному человеку перелить резус-положительную кровь. Резус фактор передается по наследству. Если женщина Rh-, а мужчина Rh+, то плод в 50 – 100 % будет наследовать резус-фактор отца и тогда мать и плод будут несовместимы. При такой беременности плацента будет проницаема для эритроцитов плода. Они в крови матери будут стимулировать образование антител. Попадая в плод, такие антитела будут вызывать агглютинацию и гемолиз (разрушение) его эритроцитов. Несовместимость матери и плода по группам крови может быть причиной выкидышей и преждевременных родов. Помимо перечисленных систем гематологи выделяют еще несколько важных антигенных систем совместимости тканей у человека – MNSs, P, Лютеран (Lu), Келл-Келлано (Кк), Льюис (Le), Даффи (Fy) и Кид (Jk).
4.4. Система раск
Система PACK ( регуляция аггрегатного состояния крови) включает в себя свертывающие, противосвертывающие и фибринолитические( растворение кровяного сгустка) механизмы.
Свертывание крови(гемокоагуляция, гемостаз) -жизненно важная защитная реакция, предотвращающая гибель организма от кровопотери при травме сосудов. Сущность этого процесса заключается в переходе растворимого белка крови фибриногена в нерастворимый фибрин, в результате чего образуется прочный фибриновый тромб.
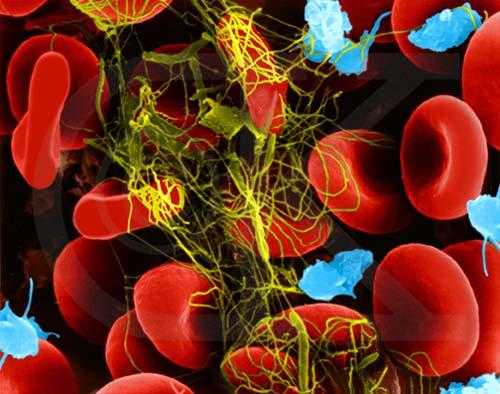
Фиг. Вид сгустка крови (тромба)
В остановке кровотечения участвуют сосуды, ткани, окружающие сосуды, а также физиологически активные вещества плазмы крови, форменные элементы и прежде всего тромбоциты, нейрогуморальный аппарат регуляции.
В остановке кровотечения выделяют два этапа: первый — сосудисто-тромбоцитарный и второй — коагуляционный. Коагуляционный гемостаз — цепной ферментативный процесс последовательной активации ферментов и белков свертывания и образования их комплексов.
Под термином «гемостаз» понимают комплекс реакций, направленных на остановку кровотечения при травмах сосудов. Однако физиологическое значение системы свертывания намного шире и включает в себя феномены поддержания гомеостаза крови, транскапиллярного обмена, устойчивости сосудистой стенки, восстановительных процессов в организме. Кровотечение из раны в норме прекращается через три — четыре минуты. В течение этого времени она свертывается. Процесс свертывания весьма сложен и представляет собой цепь последовательных событий. В упрощенном виде он состоит из следующих трех фаз: 1- комплекс последовательных реакций образования фермента тромбокиназы, 2 — переход фермента протромбина (фактора 2) в тромбин (фактор 2а) и 3 – образование фибрина из фибриногена и формирование сгустка крови. Цепь событий следующая: при ранении стенки сосуда в месте разрыва происходит разрушение тромбоцитов и выделение биологически активных веществ — серотонина, АДФ (аденозиндифосфат), адреналина. Эти вещества стимулируют сужение просвета сосудов с одновременным выделением из тромбоцитов белка тромбопластина и активизацию фермента тромбокиназы. Тромбокиназа переводит следующий белок (но теперь уже из плазмы крови) протромбин в его активную форму — тромбин. В свою очередь тромбин воздействует на растворенный в плазме фибриноген и переводит его в нерастворимую форму – фибрин. Этот белок полимеризуется в виде нитей, из которых и образуется сгусток крови вместе с эритроцитами и тромбоцитами. Схема свертывания крови представлена на рис.6.

Противосвертывающая система. Несмотря на то, что в циркулирующей крови есть все факторы для ее свертывания, в естественных условиях кровь в сосудах остается жидкой. Это объясняется наличием в кровотоке противосвертывающих веществ, получивших название антикоагулянтов, или системы фибринолиза. Основными макромолекулами этой системы являются гепарин, антитромбин, антиплазмин, антитрипсин, ингибитор самосборки фибрина. Являясь важной защитной реакцией фибринолиз предотвращает закупорку кровеносных сосудов фибриновыми сгустками. При многих заболеваниях, сопровождающихся разрушением эритроцитов, лейкоцитов, тромбоцитов и тканей, происходит нарушение процесса свертывания крови, что часто является тяжелым осложнением течения заболевания. Особенно часто такие нарушения имеют место при переливании несовместимой крови, обширных травмах, отморожениях, ожогах, длительных оперативных вмешательствах на легких, печени, сердце, а также в акушерской практике при попадании в кровоток матери околоплодных вод.
Фибринолиз — это обязательная часть системы гемостаза, которая всегда сопровождает процесс свертывания крови и активируется факторами, принимающими участие в этом процессе. Являясь важной защитной реакцией фибринолиз предотвращает закупорку кровеносных сосудов фибриновыми сгустками. Ферментом, разрушающим фибрин, являетсяплазмин (илифибринолизин), находящийся в крови в неактивном состоянии в виде профермента плазминогена. В плазме находятся и ингибиторы фибринолиза. Важнейшими из них являются антиплазмин, трипсин, калликреин, урокиназа.
Лимфа.
Лимфа ( от лат. Lympha- влага) представляет собой жидкость желтоватого цвета, содержащуюся в лимфатических сосудах и капиллярах. Лимфа состоит из плазмы белковой природы и клеточных элементов. По химическому составу плазма лимфы близка к плазме крови, однако содержание белков меньшее. В белковой фракции лимфы альбумины преобладают над глобулинами. В лимфе содержатся ферменты, такие как диастаза, липаза и гликолитические ферменты. В плазме лифы содержатся также нейтральные жиры, простые сахара, неорганические компоненты в виде хлористого и углекислого натрия а также различные соединения с ионами кальция, магния и железа.
Клеточный состав лимфы представлен в основном лимфоцитами а также моноцитами и другими видами лейкоцитов. Лимфа циркулирует в лимфатических капиллярах тканей и органов. Из капилляров лимфа перемещается в периферические лимфатические сосуды, по ним – в лимфатические узлы, откуда поступает в крупные лимфатические сосуды и затем вливается в кровь . Так же, как и кровь, лимфа выполняет различные функции, осуществляя регуляцию гомеостаза в организме. Процесс лимфообразования тесно связан с поступлением жидкости и питательных веществ из крови в межклеточное тканевое пространство и образованием тканевой жидкости.
studfiles.net
Система РАСК Гемостаз 1 Поддержание жидкого состояния крови
 Система РАСК Гемостаз 1. Поддержание жидкого состояния крови (противосветывающая система) 2. Сосудисто-тромбоцитарный гемостаз 3. Свертывающая система крови 4. Фибринолитическая система 5. Методы исследования гемостаза 6. Принципы медикаментозных влияний на систему гемостаза
Система РАСК Гемостаз 1. Поддержание жидкого состояния крови (противосветывающая система) 2. Сосудисто-тромбоцитарный гемостаз 3. Свертывающая система крови 4. Фибринолитическая система 5. Методы исследования гемостаза 6. Принципы медикаментозных влияний на систему гемостаза
 Поддержание жидкого состояния крови Неповрежденный эндотелий препятствует свертыванию крови: — Нет контактной активации свертывания; — Эндотелием выделяются факторы препятствующие агрегации тромбоцитов (простациклин) и активирующие фибринолиз; — Антитромбин III активируется гепариноподобными молекулами на стенке сосуда.
Поддержание жидкого состояния крови Неповрежденный эндотелий препятствует свертыванию крови: — Нет контактной активации свертывания; — Эндотелием выделяются факторы препятствующие агрегации тромбоцитов (простациклин) и активирующие фибринолиз; — Антитромбин III активируется гепариноподобными молекулами на стенке сосуда.
 Антитромбины • Синтезируются в печени и эндотелии • Наиболее активен антитромбин III? , связанный с гепарином или гепариноподобными центрами на эндотелии • Инактивирует тромбин и другие факторы свертывания (IX, X, XI…) • Постоянно активирован • При недостатке возникают тромбозы IX X XI
Антитромбины • Синтезируются в печени и эндотелии • Наиболее активен антитромбин III? , связанный с гепарином или гепариноподобными центрами на эндотелии • Инактивирует тромбин и другие факторы свертывания (IX, X, XI…) • Постоянно активирован • При недостатке возникают тромбозы IX X XI
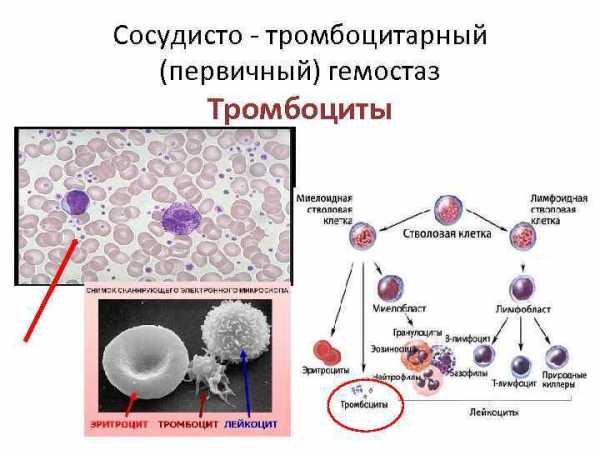 Сосудисто — тромбоцитарный (первичный) гемостаз Тромбоциты
Сосудисто — тромбоцитарный (первичный) гемостаз Тромбоциты
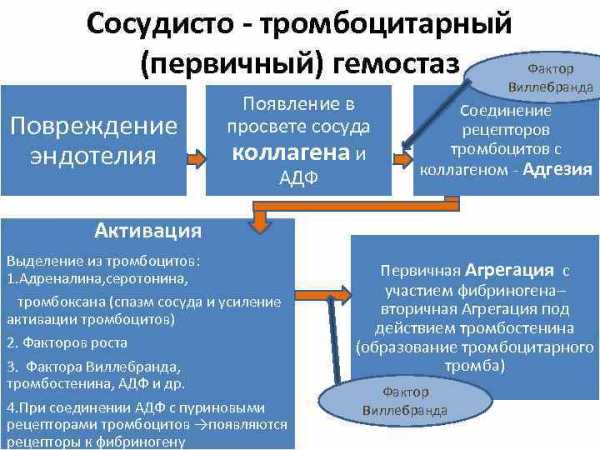 Сосудисто — тромбоцитарный (первичный) гемостаз Повреждение эндотелия Появление в просвете сосуда коллагена и АДФ Фактор Виллебранда Соединение рецепторов тромбоцитов с коллагеном — Адгезия Активация Выделение из тромбоцитов: 1. Адреналина, серотонина, тромбоксана (спазм сосуда и усиление активации тромбоцитов) 2. Факторов роста 3. Фактора Виллебранда, тромбостенина, АДФ и др. 4. При соединении АДФ с пуриновыми рецепторами тромбоцитов →появляются рецепторы к фибриногену Первичная Агрегация с участием фибриногена– вторичная Агрегация под действием тромбостенина (образование тромбоцитарного тромба) Фактор Виллебранда
Сосудисто — тромбоцитарный (первичный) гемостаз Повреждение эндотелия Появление в просвете сосуда коллагена и АДФ Фактор Виллебранда Соединение рецепторов тромбоцитов с коллагеном — Адгезия Активация Выделение из тромбоцитов: 1. Адреналина, серотонина, тромбоксана (спазм сосуда и усиление активации тромбоцитов) 2. Факторов роста 3. Фактора Виллебранда, тромбостенина, АДФ и др. 4. При соединении АДФ с пуриновыми рецепторами тромбоцитов →появляются рецепторы к фибриногену Первичная Агрегация с участием фибриногена– вторичная Агрегация под действием тромбостенина (образование тромбоцитарного тромба) Фактор Виллебранда
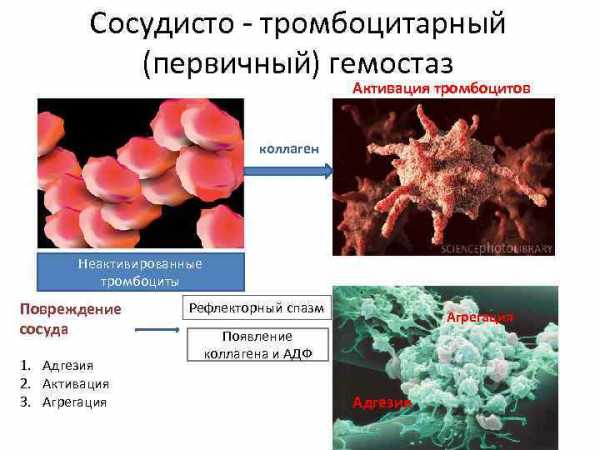 Сосудисто — тромбоцитарный (первичный) гемостаз Активация тромбоцитов коллаген Неактивированные тромбоциты Повреждение сосуда 1. Адгезия 2. Активация 3. Агрегация Рефлекторный спазм Агрегация Появление коллагена и АДФ Адгезия
Сосудисто — тромбоцитарный (первичный) гемостаз Активация тромбоцитов коллаген Неактивированные тромбоциты Повреждение сосуда 1. Адгезия 2. Активация 3. Агрегация Рефлекторный спазм Агрегация Появление коллагена и АДФ Адгезия
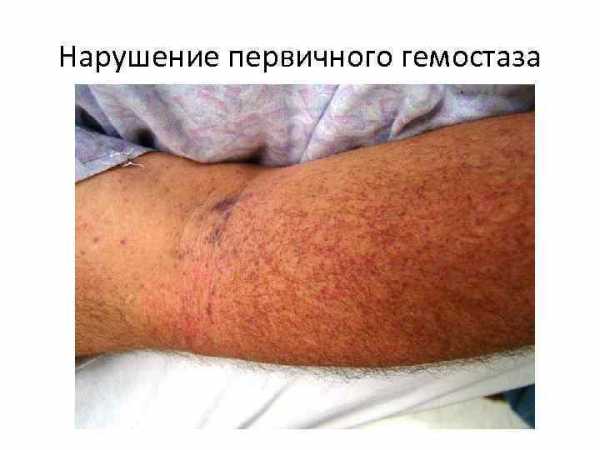 Нарушение первичного гемостаза
Нарушение первичного гемостаза
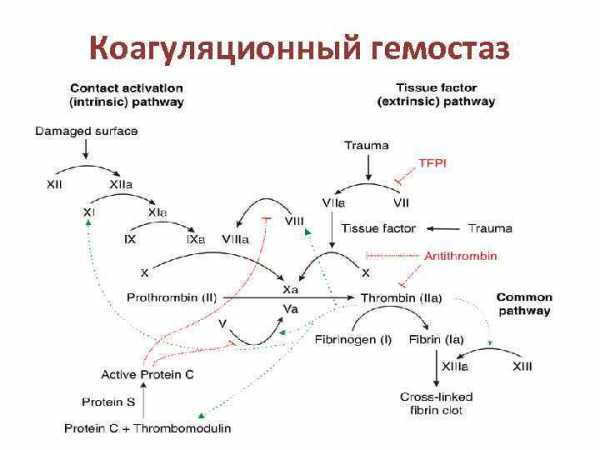 Коагуляционный гемостаз
Коагуляционный гемостаз
 Международная номенклатура факторов свертывания
Международная номенклатура факторов свертывания
 Кофакторы • Ионы кальция (Фактор IV). В процессе свертывания не расходуется. Процесс свертывания остается нормальным даже при снижении концентрации кальция , при котором наблюдается судорожный синдром. Ионы кальция участвуют во всех трех фазах свертывания крови. Кальций способен связывать гепарин, благодаря чему свертывание крови ускоряется. При отсутствии кальция нарушаются агрегация тромбоцитов и ретракция кровяного сгустка. Ионы кальция ингибируют фибринолиз. • Фактор V – проакцелерин. Образуется в печени, но, в отличие от других печеночных факторов протромбинового комплекса (II, VII, и X) не зависит от витамина K. Активирует фактор X и превращение протромбина в тромбин. При появлении следов тромбина переходит в активную форму. • Фактор VIII – антигемофильный глобулин А. Вырабатывается в печени, селезенке, клетках эндотелия, лейкоцитах, почках. Участвует во «внутреннем» пути, усиливая активирующее действие фактора IХа на фактор X. Фактор VIII циркулирует в крови, будучи связанным с фактором Виллебранда.
Кофакторы • Ионы кальция (Фактор IV). В процессе свертывания не расходуется. Процесс свертывания остается нормальным даже при снижении концентрации кальция , при котором наблюдается судорожный синдром. Ионы кальция участвуют во всех трех фазах свертывания крови. Кальций способен связывать гепарин, благодаря чему свертывание крови ускоряется. При отсутствии кальция нарушаются агрегация тромбоцитов и ретракция кровяного сгустка. Ионы кальция ингибируют фибринолиз. • Фактор V – проакцелерин. Образуется в печени, но, в отличие от других печеночных факторов протромбинового комплекса (II, VII, и X) не зависит от витамина K. Активирует фактор X и превращение протромбина в тромбин. При появлении следов тромбина переходит в активную форму. • Фактор VIII – антигемофильный глобулин А. Вырабатывается в печени, селезенке, клетках эндотелия, лейкоцитах, почках. Участвует во «внутреннем» пути, усиливая активирующее действие фактора IХа на фактор X. Фактор VIII циркулирует в крови, будучи связанным с фактором Виллебранда.
 Первая стадия коагуляционного гемомтаза Внешний путь активации Внутренний путь активации • Активируется повреждением эндотелия • Из эндотелия и гладкомышечных клеток выделяются фосфолипиды – тканевый фактор свертывания • Активация VII фактора свертывания • Активация X фактора (при участии солей Са и фосфолипидов) • Останавливается под влиянием ингибитора внешнего механизма свертывания (ИВМС) • Активируется повреждением эндотелия • XII фактор (Хагемана) в присутствии калликреина и высокомолекулярного кининогена соединяется с чужеродной поверхностью и активируется • Последовательная активация XI→IX факторов • → Активация X фактора (при участии солей Са, фосфолипидов, и VIIIa фактора(активируеся тромбином, образованным при внешнем пути) )
Первая стадия коагуляционного гемомтаза Внешний путь активации Внутренний путь активации • Активируется повреждением эндотелия • Из эндотелия и гладкомышечных клеток выделяются фосфолипиды – тканевый фактор свертывания • Активация VII фактора свертывания • Активация X фактора (при участии солей Са и фосфолипидов) • Останавливается под влиянием ингибитора внешнего механизма свертывания (ИВМС) • Активируется повреждением эндотелия • XII фактор (Хагемана) в присутствии калликреина и высокомолекулярного кининогена соединяется с чужеродной поверхностью и активируется • Последовательная активация XI→IX факторов • → Активация X фактора (при участии солей Са, фосфолипидов, и VIIIa фактора(активируеся тромбином, образованным при внешнем пути) )
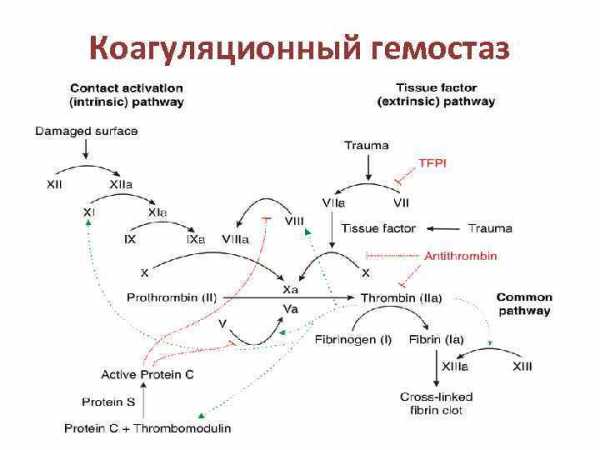 Коагуляционный гемостаз
Коагуляционный гемостаз
 Вторая фаза свертывания • Переход протромбина → в тромбин, катализируемый фактором Ха в присутствии Фл, ионов Са и Vа • Протромбин синтезируется в печени с участием витамина К • Тромбин − активирует агрегацию тромбоцитов (активирует фактор Виллебранда), активирует XI, V, VIII и XIII факторы и ИВМС. − запускает третью стадию свертывания − связывается с тромбомодулином на эндотелии: → активирует противосвертывающий протеин С и инактивируется антитромбином
Вторая фаза свертывания • Переход протромбина → в тромбин, катализируемый фактором Ха в присутствии Фл, ионов Са и Vа • Протромбин синтезируется в печени с участием витамина К • Тромбин − активирует агрегацию тромбоцитов (активирует фактор Виллебранда), активирует XI, V, VIII и XIII факторы и ИВМС. − запускает третью стадию свертывания − связывается с тромбомодулином на эндотелии: → активирует противосвертывающий протеин С и инактивируется антитромбином
 Третья фаза коагуляционного гемостаза • Переход фибриногена в фибрин под действием тромбина + ионы Са и ФЛ Водородные связи и т. п. Ковалентные связи
Третья фаза коагуляционного гемостаза • Переход фибриногена в фибрин под действием тромбина + ионы Са и ФЛ Водородные связи и т. п. Ковалентные связи
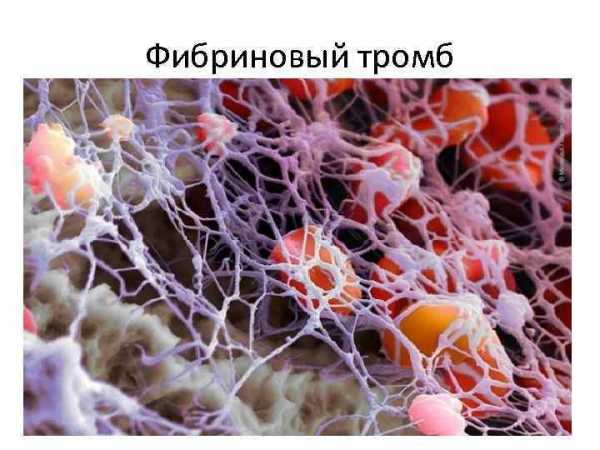 Фибриновый тромб
Фибриновый тромб
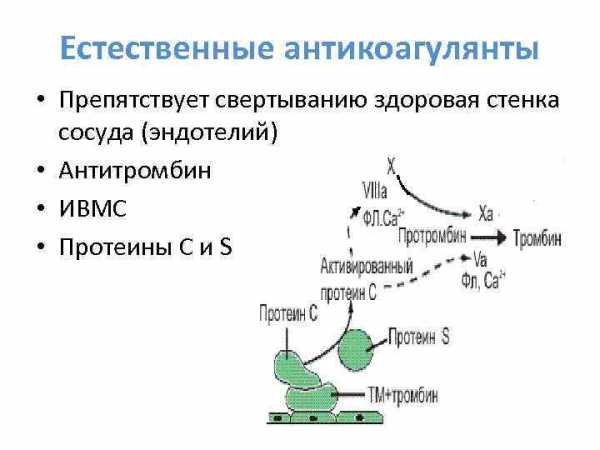 Естественные антикоагулянты • Препятствует свертыванию здоровая стенка сосуда (эндотелий) • Антитромбин • ИВМС • Протеины С и S
Естественные антикоагулянты • Препятствует свертыванию здоровая стенка сосуда (эндотелий) • Антитромбин • ИВМС • Протеины С и S
 Коагуляционный гемостаз
Коагуляционный гемостаз
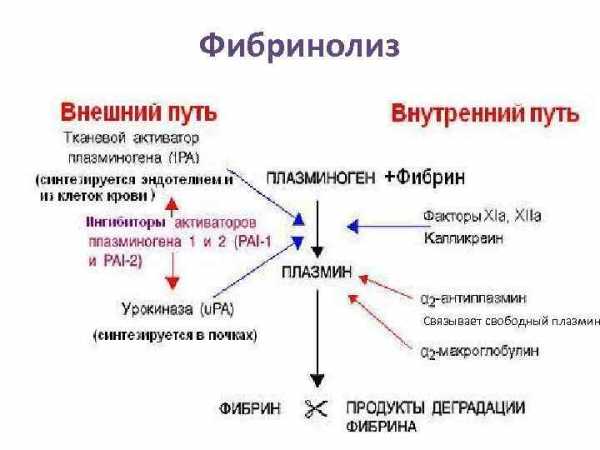 Фибринолиз Связывает свободный плазмин
Фибринолиз Связывает свободный плазмин
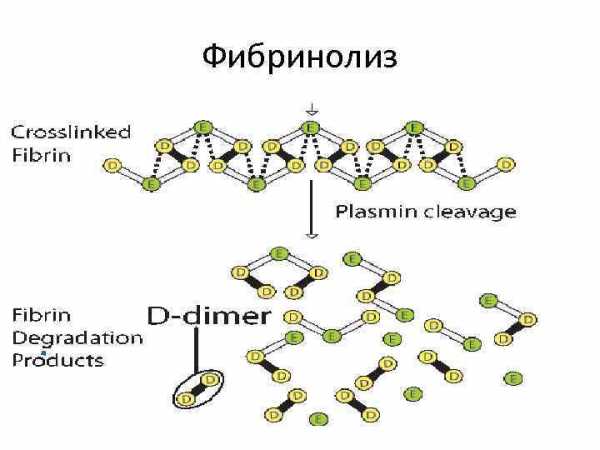 Фибринолиз
Фибринолиз
 Антикоагулянты Прямого действия Антитромбин Гепарин Непрямого действия Антагонисты витамина К Свертывание крови снижает цитрат натрия (связывает ионы Са) и антиагреганты, например ацетилсалициловая кислота (блокирует агрегацию тромбоцитов, подавляя синтез тромбоксана) и блокаторы пуриновых рецепторов (препятствуют появлению рецептров тромбоцитов к фибриногену)
Антикоагулянты Прямого действия Антитромбин Гепарин Непрямого действия Антагонисты витамина К Свертывание крови снижает цитрат натрия (связывает ионы Са) и антиагреганты, например ацетилсалициловая кислота (блокирует агрегацию тромбоцитов, подавляя синтез тромбоксана) и блокаторы пуриновых рецепторов (препятствуют появлению рецептров тромбоцитов к фибриногену)
 Методы исследования гемостаза • Исследование сосудисто- тромбоцитарного гемостаза: Время кровотечения (до 5 минут по Дьюку) • Исследование коагуляционного гемостаза: 1. Время свертывания (4 – 8 минут) 2. Протромбиновое время (внешний путь и общий) (11 -16 секунд) 3. Активированное частичное тромбопластиновое время (внутренний путь и общий) (25 – 35 секунд)
Методы исследования гемостаза • Исследование сосудисто- тромбоцитарного гемостаза: Время кровотечения (до 5 минут по Дьюку) • Исследование коагуляционного гемостаза: 1. Время свертывания (4 – 8 минут) 2. Протромбиновое время (внешний путь и общий) (11 -16 секунд) 3. Активированное частичное тромбопластиновое время (внутренний путь и общий) (25 – 35 секунд)
 Протромбиновое время • Исследование проводят с использованием плазмы крови, в которую ранее был добавлен цитрат натрия (предупреждение свертывания при хранении) • Добавляют соли Са и тканевый фактор, т. е. активируют внешний путь запуска. • Производные от протромбинового времени: 1. Протромбиновый индекс (ПТВ N ПТВ исследуемая плазма) 2. Международное нормализованное отношение – МНО (МНО=ПТВ исследуемоеПТВ N) МИЧ — индекс чувствительности для данного вида реагента.
Протромбиновое время • Исследование проводят с использованием плазмы крови, в которую ранее был добавлен цитрат натрия (предупреждение свертывания при хранении) • Добавляют соли Са и тканевый фактор, т. е. активируют внешний путь запуска. • Производные от протромбинового времени: 1. Протромбиновый индекс (ПТВ N ПТВ исследуемая плазма) 2. Международное нормализованное отношение – МНО (МНО=ПТВ исследуемоеПТВ N) МИЧ — индекс чувствительности для данного вида реагента.
 Активированное частичное тромбопластиновое время • Исследование проводят с использованием плазмы крови, в которую ранее был добавлен цитрат натрия (предупреждение свертывания при хранении) • Добавляют соли Са, фосфолипиды и мелкие частицы (песок – для активации XII фактора), т. е. не добавляется тканевый фактор (апопротеин III и фосфолипиды)
Активированное частичное тромбопластиновое время • Исследование проводят с использованием плазмы крови, в которую ранее был добавлен цитрат натрия (предупреждение свертывания при хранении) • Добавляют соли Са, фосфолипиды и мелкие частицы (песок – для активации XII фактора), т. е. не добавляется тканевый фактор (апопротеин III и фосфолипиды)
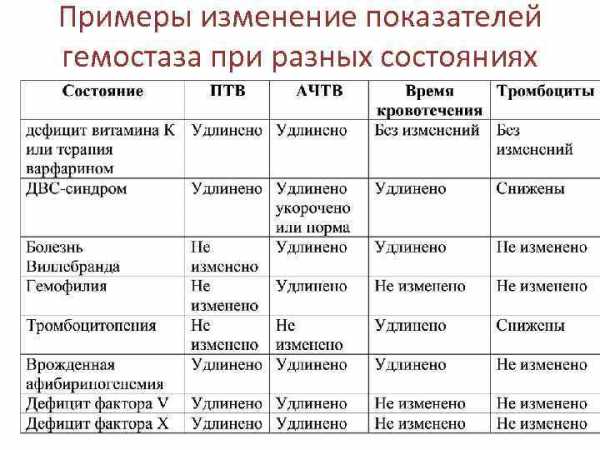 Примеры изменение показателей гемостаза при разных состояниях
Примеры изменение показателей гемостаза при разных состояниях
present5.com
Составление схемы «Система РАСК ( регуляция агрегатного
⇐ ПредыдущаяСтр 2 из 6Следующая ⇒Состояния крови)».
Составление сообщения «Донорство в России»
Семинар внутренней среде организма и
Морфофункциональной характеристики
Крови.
22. Сердечнососудистая система. •Анатомия сердца.
Составление глоссария.
Работа с атласом«Круги кровообращения», «Строение сердца».
Составление рисунков-схем по теме занятия.
Физиология сердца. Сердечный цикл. Основные
Характеристики работы сердца.
Составление глоссария.
Заполнение таблицы: «Характеристика фаз сердечного цикла».
Работа с атласом.
Рисунки-схемы по теме занятия.
Процесс кровообращения. Сосуды малого и коронарного
Кругов кровообращения. Артерии большого круга
Кровообращения
Составление глоссария.
Работа с атласом.
Составление рисунков-схем по теме занятия.
Вены большого круга кровообращения.
Составление глоссария.
Работа с атласом схем-рисунков: «Образование и притоки
Верхней полой вены», «Образование и притоки нижней полой
Вены», «Образование и притоки воротной вены».
Составление рисунков-схем по теме занятия.
Основы гемодинамики.
Составление глоссария.
Выполнение схемы: «Факторы, влияющие на величину артериального давления».
Функциональная анатомия лимфатической системы.
Составление глоссария.
Работа с атласом.
Эссе роль лимфатической системы в работе ССС.
Схемы-рисунки по теме занятия.
Анатомия и физиология иммунной системы.
Составление глоссария.
Работа с атласом.
Рисунки-схемы по теме занятия.
4..Реферативные работы по выбору студентов.
Анатомия и физиология дыхательной системы.
Воздухоносные пути.
Составление глоссария.
Работа с атласом.
Рисунки-схемы по теме занятия.
30. Анатомия и физиология легких. •Плевра. Плевральные
Полости.
Составление глоссария.
Работа с атласом.
Физиологические показатели работы легких.
Рисунки-схемы по теме занятия.
Физиологические показатели работы легких.
Регуляция процесса дыхания.
Составление глоссария.
Работа с атласом.
Таблица «Физиологические показатели работы легких.»
4. По выбору студентов презентация.
Анатомия органов пищеварения. Анатомия и физиология
Полости рта.
Составление глоссария.
Работа с атласом.
Рисунки-схемы по теме занятия.
Таблица-схема « Пищеварение в полости рта».
Образец таблиц по разделу пищеварение
Анатомия и физиология органов пищеварительного тракта
(глотка, пищевод, желудок).
Составление глоссария.
Работа с атласом.
Рисунки-схемы по теме занятия.
Таблица «Пищеварение в желудке».
Анатомия и физиология больших пищеварительных желез.
Составление глоссария.
Работа с атласом.
Свободный выбор тем реферативных работ.
Рисунки-схемы по теме занятия.
Анатомия и физиология тонкого кишечника.
Составление глоссария.
Работа с атласом.
Рисунки-схемы по теме занятия.
Схема пристеночного переваривания пищи.
Анатомия и физиология толстого кишечника. Брюшина.
Составление глоссария.
Работа с атласом.
Рисунки-схемы по теме занятия.
Схемы: « Формирования каловых масс», « Процессы
Пищеварения в толстом кишечнике».
Обмен веществ. Витамины.
Составление глоссария.
Таблица: «Витамины».
Схемы обмена углеводов, белков и жиров.
Обмен энергии в организме. Терморегуляция.
Составление глоссария.
Эссе « Обмен энергии в организме человека»,
« Терморегуляция организма теплокровных».
39.
Семинар по темам « Анатомия и физиология пищеварительной системы», « Обмен веществ».
Анатомия и физиология мочевыделительной системы.
Почки. Мочеточники. Мочевой пузырь.
Составление глоссария.
Работа с атласом.
Рисунки-схемы по теме занятия.
Строение и функция нефрона. Почки – центр водно-
Электролитного обмена.
Составление глоссария.
Схема строения нефрона.
Сообщение « Почки — центр водно-электролитного обмена».
Анатомия и физиология мужской репродуктивной системы человека.
Составление глоссария.
Работа с атласом.
infopedia.su
