Грипп? Коронавирус? ОРВИ? Симптомы, осложнения, профилактика. — Городская поликлиника 69, город Москва
Что такое коронавирусы?
Коронавирусы — это семейство вирусов, которые преимущественно поражают животных, но в некоторых случаях могут передаваться человеку. Обычно заболевания, вызванные коронавирусами, протекают в лёгкой форме, не вызывая тяжёлой симптоматики. Однако, бывают и тяжёлые формы, такие как ближневосточный респираторный синдром (Mers) и тяжёлый острый респираторный синдром (Sars).
Каковы симптомы заболевания, вызванного новым коронавирусом?
Чувство усталости
Затруднённое дыхание
Высокая температура
Кашель и / или боль в горле
Симптомы во многом сходны со многими респираторными заболеваниями, часто имитируют обычную простуду, могут походить на грипп.
Если у вас есть аналогичные симптомы, подумайте о следующем:
Вы посещали в последние две недели в зоны повышенного риска (Китай и прилегающие регионы)?
Вы были в контакте с кем-то, кто посещал в последние две недели в зоны повышенного риска (Китай и прилегающие регионы)?
Если ответ на эти вопросы положителен — к симптомам следует отнестись максимально внимательно.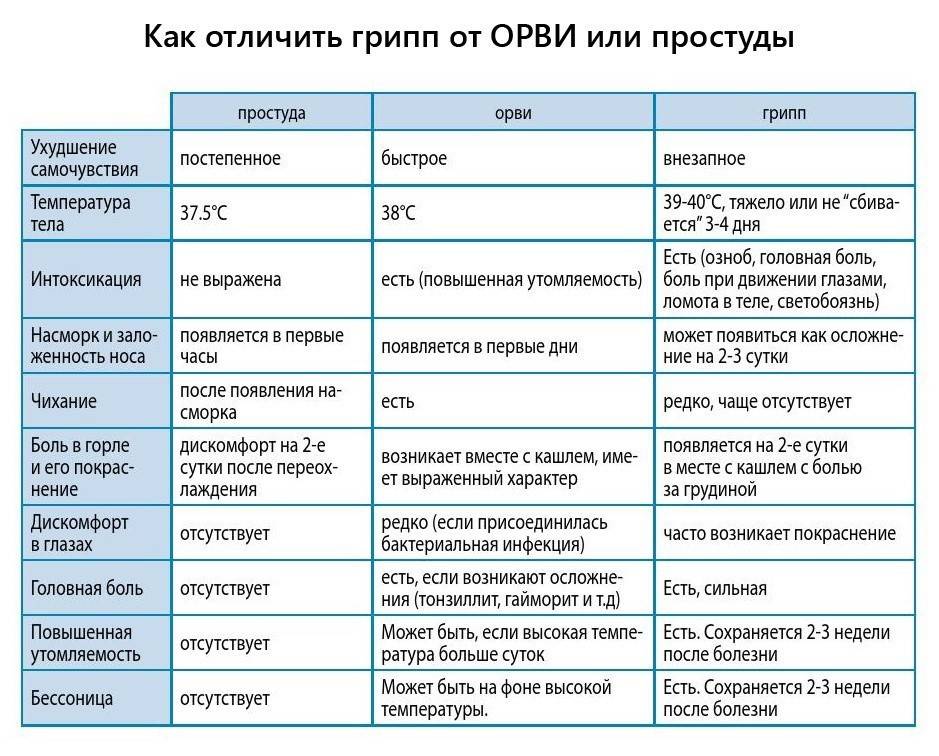
Как передаётся коронавирус?
Как и другие респираторные вирусы, коронавирус распространяется через капли, которые образуются, когда инфицированный человек кашляет или чихает. Кроме того, он может распространяться, когда кто-то касается любой загрязнённой поверхности, например дверной ручки. Люди заражаются, когда они касаются загрязнёнными руками рта, носа или глаз.
Изначально, вспышка произошла от животных, предположительно, источником стал рынок морепродуктов в Ухани, где шла активная торговля не только рыбой, но и такими животными, как сурки, змеи и летучие мыши.
Как защитить себя от заражения коронавирусом?
Самое важное, что можно сделать, чтобы защитить себя, — это поддерживать чистоту рук и поверхностей.
Держите руки в чистоте, часто мойте их водой с мылом или используйте дезинфицирующее средство.
Также старайтесь не касаться рта, носа или глаз немытыми руками (обычно такие прикосновения неосознанно свершаются нами в среднем 15 раз в час).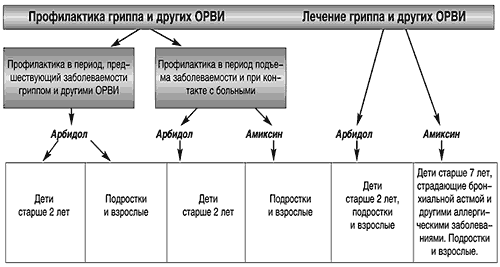
Носите с собой дезинфицирующее средство для рук, чтобы в любой обстановке вы могли очистить руки.
Всегда мойте руки перед едой.
Будьте особенно осторожны, когда находитесь в людных местах, аэропортах и других системах общественного транспорта. Максимально сократите прикосновения к находящимся в таких местах поверхностям и предметам, и не касайтесь лица.
Носите с собой одноразовые салфетки и всегда прикрывайте нос и рот, когда вы кашляете или чихаете, и обязательно утилизируйте их после использования.
Не ешьте еду (орешки, чипсы, печенье и другие снеки) из общих упаковок или посуды, если другие люди погружали в них свои пальцы.
Избегайте приветственных рукопожатий и поцелуев в щеку, пока эпидемиологическая ситуация не стабилизируется.
На работе регулярно очищайте поверхности и устройства, к которым вы прикасаетесь (клавиатура компьютера, панели оргтехники общего использования, экран смартфона, пульты, дверные ручки и поручни).
Как правильно носить медицинскую маску?
- Аккуратно закройте нос и рот маской и закрепите её, чтобы уменьшить зазор между лицом и маской.
- Не прикасайтесь к маске во время использования. После прикосновения к использованной маске, например, чтобы снять её, вымойте руки.
- После того, как маска станет влажной или загрязнённой, наденьте новую чистую и сухую маску.
- Не используйте повторно одноразовые маски. Их следует выбрасывать после каждого использования и утилизировать сразу после снятия.
Что можно сделать дома?
Расскажите детям о профилактике коронавируса.
Объясните детям, как распространяются микробы, и почему важна хорошая гигиена рук и лица.
Убедитесь, что у каждого в семье есть своё полотенце, напомните, что нельзя делиться зубными щётками и другими предметами личной гигиены.
Часто проветривайте помещение.
Можно ли вылечить новый коронавирус?
Да, разумеется.
Вирусную пневмонию, основное и самое опасное осложнение коронавирусной инфекции, нельзя лечить антибиотиками. В случае развития пневмонии — лечение направлено на поддержание функции лёгких.
Кто в группе риска?
Люди всех возрастов рискуют заразиться вирусом. В заявлении комиссии по здравоохранению Ухани говорится, что возраст 60 самых последних случаев составляет от 15 до 88 лет.
Однако, как и в случае большинства других вирусных респираторных заболеваний, дети и люди старше 65 лет, люди с ослабленной иммунной системой — в зоне риска тяжёлого течения заболевания.
Есть ли вакцина для нового коронавируса?
В настоящее время такой вакцины нет, однако, в ряде стран, в том числе в России в научных организациях Роспотребнадзора уже начаты её разработки.
В чем разница между коронавирусом и вирусом гриппа?
Коронавирус и вирус гриппа могут иметь сходные симптомы, но генетически они абсолютно разные.
Вирусы гриппа размножаются очень быстро — симптомы проявляются через два-три дня после заражения, а коронавирусу требуется для этого до 14 дней.
Как определить у себя наличие коронавируса?
Своевременная диагностика является одним из важнейших мероприятий при возникновении угрозы появления и распространения нового коронавируса на территории России. Научными организациями Роспотребнадзора менее чем за 7 дней с момента появления информации о структуре генов нового коронавируса разработаны два варианта диагностических наборов для определения присутствия вируса в организме человека. Наборы основаны на молекулярно-генетическом методе исследования, так называемой полимеразной цепной реакции (ПЦР). Использование этого метода дает тест-системам значительные преимущества. Первое это высокая чувствительность – с использованием разработанных тест-систем возможно обнаруживать единичные копии вирусов.
Коронавирус 2019 nCoV — поможет маска!
В условиях сложившейся ситуации в отношении увеличения потенциального риска завоза и распространения на территории Российской Федерации нового коронавируса 2019 — nCoV, напоминаем о целесообразности использования одноразовой медицинской маски в качестве эффективной меры профилактики заражения и распространения инфекции.
Коронавирус 2019 — nCoV передаётся от человека к человеку при близком контакте, через микрокапли респираторных выделений, которые образуются, когда инфицированные люди говорят, чихают или кашляют.
Также, заражение может происходить в результате непосредственного или косвенного контакта здорового человека с респираторными выделениями инфицированного.
Использование одноразовой медицинской маски предотвращает попадание в организм здорового человека капель респираторных выделений, которые могут содержать вирусы, через нос и рот.
Надевайте маску, когда ухаживаете за членом семьи с симптомами вирусного респираторного заболевания.
Если вы больны, или у вас симптомы вирусного респираторного заболевания, наденьте маску перед тем, как приближаться к другим людям.
Если у вас симптомы вирусного респираторного заболевания и вам необходимо обратиться к врачу, заблаговременно наденьте маску, чтобы защитить окружающих в зоне ожидания.
Носите маску, когда находитесь в людных местах.
Используйте маску однократно, повторное использование маски недопустимо. Меняйте маску каждые 2-3 часа или чаще.
Если маска увлажнилась, её следует заменить на новую.
После использования маски, выбросьте её и вымойте руки.
Одноразовая медицинская маска, при правильном использовании — надёжный и эффективный метод снижения риска заражения коронавирусом и предотвращения распространения гриппа.
Грипп 2020: симптомы, лечение, как передается и как отличить от простуды
По данным Центра общественного здоровья министерства здравоохранения Украины по состоянию на начало января 2020 года с диагнозом грипп госпитализированы более 53 тысяч человек, 79% из которых дети.
С начала эпидемиологического сезона острыми респираторными вирусными инфекциями в Украине заболели более 170 тысяч человек разного возраста.
Также зарегистрированы два летальных исхода от осложнений гриппа. В первом случае мужчина заболел 20 декабря 2019, а уже 31 декабря 2019 скончался. Диагноз подтвержден лабораторно: причиной болезни был вирус гриппа типа А.
Второй случай смерти от гриппа зарегистрирован 3 января 2020 года. Известно, что умершая женщина принадлежала к группе риска и имела сопутствующие заболевания, от гриппа не была вакцинирована. Диагноз также был подтвержден лабораторно – вирус гриппа типа А(Н1) pdm09.
Министерство здравоохранения напоминает о том, что лучшей профилактикой гриппа является ежегодная вакцинация, которая позволяет снизить риск заболевания или развития его серьезных осложнений, в том числе и летального исхода.
С начала октября 2019 года проведена вакцинация против гриппа 227 417 гражданам.
По данным на середину декабря 2019 года в большинстве регионов Украины активность гриппа и ОРВИ не превышала эпидемический порог. А в некоторых областях (Винницкая и Запорожская) зарегистрирована низкая эпидемиологическая активность данных заболеваний.
В прошлом эпидемиологическом сезоне (1 октября 2018 – 19 мая 2019) переболели гриппом и ОРВИ около 5,4 млн. украинцев. Зарегистрировано 64 летальных исходов. Большая часть заболевших – дети до 17 лет. При этом каждый пятый обратился уже при критическом ухудшении состояния здоровья.
Были вакцинированы более 161,5 тыс. человек, но ни один из 64 умерших не прививались от гриппа. Лабораторные исследования установили доминирование вирусов гриппа типа А.
Симптомы гриппа:
- интоксикация на протяжении всего периода заболевания, проявляющаяся ломотой, ознобом, болью в голове и мышцах;
- слезотечение, светобоязнь, покраснение и дискомфорт в глазах;
- одышка, ощущение нехватки воздуха.

Симптомы острой формы гриппа у взрослых:
- затрудненное дыхание;
- боль и дискомфорт в груди или животе;
- головокружение;
- растерянность;
- повторяющаяся рвота;
- затихание симптомов с последующим возвращением с лихорадкой и сильным кашлем.
У детей острая форма гриппа сопровождается несколько другими симптомами:
- нарушение дыхания;
- синюшность кожных покровов;
- уменьшение объема потребляемой жидкости;
- сонливость, заторможенность;
- уменьшение симптомов заболевания с последующим поднятием температуры и усилением кашля;
- лихорадка;
- сыпь на коже.
Отличие гриппа от простуды:
- внезапное и стремительное начало заболевания;
- в начальном периоде болезни отсутствуют типичные для простуды симптомы, такие как насморк или боль в горле;
- боль в голове, ломота в суставах и мышцах;
- боль в горле появляется на 3-4 день от начала болезни, кашель;
- появление насморка только на 2-3 день от начала болезни;
- повышение температуры тела до 38 градусов и выше (при простуде температура как правило не превышает 37,5 градусов).

Способы передачи вируса гриппа
Источником и переносчиком вируса является зараженный человек, который наиболее опасен для окружающих в первые дни болезни. Заразным человек начинает быть еще за несколько дней до появления первых симптомов и до их окончания. В основном этот период занимает около двух недель. Путь передачи инфекции – воздушно капельный. Заразиться можно при общении, рукопожатии, разговоре, чихании. Также возможен контактно-бытовой путь передачи через предметы домашнего обихода и т.д.
Медики настоятельно рекомендуют при первых симптомах обращаться к семейному врачу или терапевту и не заниматься самолечением.
Также рекомендуем обратить внимание на симптомы коронавируса и источники получения достоверной информации по этой проблеме, например, медбот Марта.
Что делать если вы все же заболели?
МБУЗ г. Сочи « Городская больница №1»
Режим: спокойный полупостельный. Комната должна обязательно регулярно проветриваться.
Комната должна обязательно регулярно проветриваться.
Обильное теплое питье(не менее 2л в сутки), лучше богатое витамином С — чай с лимоном, настой шиповника, морс. Выпивая ежедневно большое количество жидкости, больной человек проводит дезинтоксикацию – т.е. ускоренное выведение из организма токсинов, которые образуются в результате жизнедеятельности вирусов.
Нестероидные противовоспалительные препараты.Эти препараты обладают противовоспалительным действием, снижают температуру тела, уменьшают боль. Следует помнить, что снижать температуру ниже 38 градусов по Цельсию не стоит, поскольку именно при этой температуре тела в организме активизируются защитные механизмы против инфекции. Исключения составляют больные, склонные к судорогам, и маленькие дети.
Антигистаминные препараты – это лекарственные средства, которые применяются для лечения аллергии. Они обладают мощным противовоспалительным эффектом, поэтому уменьшают все признаки воспаления: заложенность носа, отек слизистых.
Капли для носа.Сосудосуживающие капли для носа уменьшают отек, снимают заложенность. Однако это не столь безопасный препарат, как может показаться. С одной стороны, во время ОРВИ необходимо применять капли, чтобы уменьшить отек и улучшить отток жидкости из носовых пазух для предотвращения развития гайморита. Однако частое и длительное применение сосудосуживающих капель опасно в отношении развития хронического ринита. Бесконтрольный прием препаратов вызывает значительное утолщение слизистой носовых ходов, что приводит к зависимости от капель, а затем и к постоянной заложенности носа. Лечение этого осложнения – только хирургическое. Поэтому нужно строго соблюдать режим употребления капель: не дольше 5-7 дней, не более 2-3 раз в сутки.
Лечение боли в горле. Самое эффективное средство (оно же самое нелюбимое многими) – это полоскание горла. Можно использовать настои шалфея, ромашки, а также готовые растворы, такие как фурациллин. Полоскание должно быть частым – раз в 2 часа.
Препараты от кашля.Цель лечения кашля – снизать вязкость мокроты, сделать ее жидкой и легкой для откашливания. Немаловажен для этого питьевой режим – теплое питье разжижает мокроту. При трудностях с откашливанием можно принимать отхаркивающие препараты.
Иммуномодулирующие и противовирусные препараты.Для рекомбинантного интерферона — противовирусная активность является основной и наиболее детально изученной. Многолетнее клиническое применение позволяет говорить об универсально широком диапазоне противовирусного действия и возможности использования их при самых различных вирусных инфекциях (грипп и другие ОРВИ, герпес, вирусные гепатиты, вирус папилломы человека). Препараты рекомбинантного интерферона лишены недостатков химиопрепаратов. Они обладают универсально широким спектром антивирусной активности и не вызывают формирования резистентных форм вирусов. Применяются при первых признаках гриппа и ОРВИ. При выборе препарата следует учитывать, чтобы он содержит еще и антиоксиданты (мембраностабилизирующие компоненты), для усиления противовирусного действия основного вещества в составе — интерферона. Так, рекомбинантныйпрепарат ВИФЕРОН®для лечения гриппа и ОРВИ выпускается в форме суппозиториев ректальных. Наличие нескольких дозировок позволяет лечить как новорожденных, так и взрослых, включая беременных. Наличие местной формы в виде геля позволяет применять препарат, как во время лечения в комплексной схеме гриппа и ОРВИ, так и в профилактических целях, особенно в период массовых острых респираторных вирусных заболеваний.
Так, рекомбинантныйпрепарат ВИФЕРОН®для лечения гриппа и ОРВИ выпускается в форме суппозиториев ректальных. Наличие нескольких дозировок позволяет лечить как новорожденных, так и взрослых, включая беременных. Наличие местной формы в виде геля позволяет применять препарат, как во время лечения в комплексной схеме гриппа и ОРВИ, так и в профилактических целях, особенно в период массовых острых респираторных вирусных заболеваний.
Таблетки или постельный режим? Как надо лечить простуду и грипп
Клинический фармаколог с полувековым стажем, профессор Михаил Кевра рекомендует при сезонных респираторных инфекциях не увлекаться лекарственными препаратами.
Специалист высказал озабоченность растущей фармакоманией среди населения и врачей, а также прокомментировал несколько мифов, касающихся методов профилактики и лечения простудных заболеваний и гриппа.
Лекарство создали, а вирус изменился
— Михаил Константинович, в холодный сезон народ активно скупает таблетки «от простуды», т. е. противовирусные, которые продаются без рецепта врача. Типичная просьба к работнику аптеки — посоветуйте лучшее. А если судить по рекламе, то все препараты «мощные и действуют безотказно». Как специалист, всю жизнь изучающий влияние лекарственных препаратов на организм человека, что рекомендуете?
е. противовирусные, которые продаются без рецепта врача. Типичная просьба к работнику аптеки — посоветуйте лучшее. А если судить по рекламе, то все препараты «мощные и действуют безотказно». Как специалист, всю жизнь изучающий влияние лекарственных препаратов на организм человека, что рекомендуете?
— Сегодня из моих уст не прозвучит ни одного названия. И не только из-за нежелания поддерживать коммерческие интересы производителей. Дело в том, что большинство существующих т. н. противовирусных средств только облегчают симптомы заболевания, но на сам вирус не оказывают губительного действия.
К сожалению, созданные недавно препараты, задерживающие размножение вирусов, стремительно теряют свою эффективность.
Это в первую очередь объясняется быстрой изменчивостью антигенной структуры вируса. Например, установлено, что вирус гриппа под действием различных факторов внешней среды уже через 6–10 месяцев может кардинально измениться и приобрести устойчивость к тем лексредствам, которые еще недавно были эффективны. За такой срок разработать новый препарат нереально, а вирус опять станет другим… И этот процесс бесконечен.
За такой срок разработать новый препарат нереально, а вирус опять станет другим… И этот процесс бесконечен.
Лежать — и никакой работы!
—То есть Вы хотите сказать, что если простуду лечить, то она проходит за 7 дней, а если нет, то болеть будешь неделю?
— С возбудителем ОРИ борется сам организм. Ему надо помочь. Первое, что следует сделать, — обеспечить полный покой (особенно в первые три дня заболевания). Раньше в клинических руководствах по лечению респираторных инфекций первым пунктом обязывали прописывать постельный режим, а уж затем лекарственные препараты. Почему? Потому что вирус сильно ослабляет организм, и если человек будет продолжать вести обычный образ жизни или, что еще хуже, подвергать себя повышенным нагрузкам, то сил на борьбу с возбудителем попросту не останется. Чем слабее иммунитет, тем активнее цепляются патогенные вирусы и усиленнее размножается условно-патогенная флора.
Сегодня, к сожалению, акцент в лечении сместился на употребление лекарств. Заболевший вооружается таблетками и продолжает ходить на работу. К чему это приводит? К затяжному течению и возникновению осложнений. В цейтноте побороть возбудителя весьма затруднительно.
Заболевший вооружается таблетками и продолжает ходить на работу. К чему это приводит? К затяжному течению и возникновению осложнений. В цейтноте побороть возбудителя весьма затруднительно.
Второе важное условие борьбы против вируса — обильное согревающее питье (чай с лимоном, медом, малиной, молоко с медом, травяной чай). С жидкостью выводятся токсины, которые продуцирует патоген.
— Услышать подобные рекомендации от клинического фармаколога, прямо скажем, неожиданно…
—В обществе наблюдается фармакомания: многие не представляют выздоровления без таблеток, инъекций и капельниц. И врачей, которым пациент «указывает», что ему назначили мало лекарственных средств или не те, что помогают, несложно понять: иногда специалисты прописывают требуемые лекарства под моральным давлением, опасаясь конфликтов и жалоб. В какой-то степени они правы: если человек верит, что такой препарат действенен, плацебо поможет выздороветь. Но с реальной эффективностью лекарства это не имеет ничего общего.
Надо понимать, что любое химическое средство организм воспринимает как чужеродное, враждебное. Первая реакция клеток, которые встречают его, — протест и борьба. Получается, вместо того, чтобы сохранять силы, нужные организму для подавления и уничтожения возбудителя, мы заставляем наше тело тратить их на приспособление к лекарствам.
В Великобритании провели сравнительное исследование: одних пациентов с респираторной вирусной инфекцией лечили противовирусными препаратами, а других — горячим куриным бульоном со специями. В группе тех, кто «химии» не принимал, результаты были лучше. Объяснили это не только согревающим действием жидкости, но и наличием в бульоне экстрактивных веществ, которые помогают организму справиться с инфекцией.
— Возможна ли при ОРИ медикаментозная профилактика? Одно из лексредств, если верить инструкции, можно принимать для предупреждения инфекции.
— С помощью препарата остановить распространение вируса очень сложно. Куда более реальным вариантом я считаю обычное мытье рук и лица. Чаще всего мы получаем вирус не с вдыхаемым воздухом, а посредством рук. Почесал нос, потер глаза — и возбудитель проник на слизистую оболочку. Приходя с улицы, пообщавшись с больным, надо сразу вымыть руки — и риск уменьшится. Но жизнь показывает, что фармакоманов в этом не убедить!
Чаще всего мы получаем вирус не с вдыхаемым воздухом, а посредством рук. Почесал нос, потер глаза — и возбудитель проник на слизистую оболочку. Приходя с улицы, пообщавшись с больным, надо сразу вымыть руки — и риск уменьшится. Но жизнь показывает, что фармакоманов в этом не убедить!
В народе для профилактики вирусных инфекций с глубокой древности используют растения, содержащие фитонциды (чеснок, лук).
— Нередки случаи, когда заболевшие ОРИ для профилактики осложнений пьют антибиотики типа амоксициллина, который можно купить без рецепта…
— Если осложнения не развились, воспаления, вызванного именно бактериями, нет, то на уничтожение чего нацелен противомикробный препарат? На другую флору, в т. ч. на микроорганизмы, которые приносят пользу в борьбе с болезнью. На слизистых оболочках, помимо патогенов, живут т. н. сапрофитные микроорганизмы, которые сами по себе не вызывают заболевания, но помогают бороться с вирусом. Если их уничтожить, появляется дополнительная возможность вирусу выживать. Иммунитет, и без того переживший удар, слабеет еще больше.
Иммунитет, и без того переживший удар, слабеет еще больше.
Применение антибиотиков «для профилактики» ведет к тому, что микробы становятся все более устойчивыми к антимикробным препаратам.
Есть ли польза от иммуномодуляторов
— Напрашивается вывод: надо поддержать иммунитет. Немало препаратов, которые его стимулируют…
— Лучший иммунитет против острой респираторной инфекции вырабатывается в организме после того, как человек ею переболеет. Поэтому у детей и молодых людей грипп протекает «ярче» и чаще вызывает осложнения, ведь у их иммунной системы меньше опыта борьбы. Но поскольку возбудителей ОРВИ очень много, человек заболевает снова и снова.
Второе по эффективности средство — вакцинация: ослабленный возбудитель заболевания или его антигенные детерминанты специально внедряют в организм, «подогревая» тем самым выработку антител.
Эффект лекарственных средств, которые позиционируются как иммуностимуляторы и иммуномодуляторы, сомнителен. Клинические испытания, проведенные на малых группах людей, еще не доказательство!
Клинические испытания, проведенные на малых группах людей, еще не доказательство!
На Западе препаратов, которые якобы стимулируют активность иммунной системы, не назначают, потому что большинство страховых компаний не оплачивают такую терапию, не видя от нее реальной пользы. Существует также предположение, что стимуляция продукции лимфоцитов и других защитных клеток одновременно может активизировать и рост раковых клеток.
Суперустойчивые мифы о витаминах
— Что скажете о целесообразности витаминной поддержки при ОРИ, в первую очередь аскорбиновой кислотой? Многие уверены, что это способствует скорейшему выздоровлению, укреплению защитных сил.
— Если в крови не хватает витаминов (дефицит подтвержден лабораторными тестами), то восполнение даст положительный эффект. Но с таким же успехом будут «стимулировать» иммунитет и прочие незаменимые вещества — аминокислоты, натрий, кальций и другие микроэлементы!
Применять большие дозы витамина С (до 3 г в сутки) для профилактики простудных заболеваний предложил известный химик, дважды лауреат Нобелевской премии Лайнус Карл Полинг.
Первые впечатления о таком применении аскорбиновой кислоты были оптимистичными. Однако при более глубоких исследованиях, опирающихся на метод двойного «слепого» контроля (когда ни пациент, ни врач не знают, какой препарат применяется), выяснилось, что частота простуд под влиянием высоких доз аскорбиновой кислоты не уменьшается. И все же до сих пор среди населения бытует мнение о чудодейственных свойствах витамина С. К сожалению, подобные советы можно встретить и в СМИ.
Множеством клинических исследований еще в 1970-е годы было убедительно доказано, что назначение высоких доз аскорбиновой кислоты людям с нормальным уровнем ее в организме не уменьшает частоты возникновения и тяжести течения простудных заболеваний ни у взрослых, ни у детей.
Следует, однако, отметить, что есть ситуации с ОРИ, когда высокие дозы витаминов действительно помогают. Например, при гриппе, скарлатине, кори с геморрагическими проявлениями. В данном случае способствуют укреплению стенок капилляров.
Витамины — незаменимые органические вещества. Они должны постоянно поступать с пищей, поскольку организм человека не может запасать их впрок. Но их нужно мало.
Витамины, созданные искусственным путем, — это химические вещества, обладающие выраженной фармакологической активностью. В терапевтических дозах (которые в 2–3 раза выше профилактических) витамин С способен вызвать нарушения проницаемости капилляров, что ухудшает питание органов и тканей. Нужно быть осторожными в назначении этих средств беременным и тем, кто планирует зачатие: неразумное применение чревато нарушениями течения беременности и даже угрожает гибелью эмбриона.
— Очень любят обращаться к витаминам мамы и педиатры… Они тоже не правы?
— Ребенок вялый и уставший — принимаются пичкать «для поднятия тонуса», не зная уровня этих веществ в крови. Тем временем ребенок перегружен в школе и на кружках, ему попросту хочется отдохнуть, побыть на свежем воздухе. Синтетические вещества этого дефицита не скомпенсируют, а вот нарушения здоровья вызвать могут.
Установлено, что длительный прием витамина С в высоких дозах (для дошкольников и учеников младших классов это 100–200 мг в сутки, т. е. 2–4 таблетки аскорбиновой кислоты с глюкозой) может привести к снижению количества эритроцитов и гемоглобина в крови, повышению содержания лейкоцитов и уменьшению числа лимфоцитов. Даже однократный прием высокой дозы аскорбиновой кислоты способен спровоцировать тахикардию (увеличение числа сердечных сокращений в минуту), а длительный — нарушить питание сердечной мышцы, что легко установить по электрокардиограмме.
— В конце зимы многие из нас приучены покупать витаминные комплексы…
— Сезонные колебания содержания витаминов в крови являются нормой, а не патологией. Летом и осенью уровень витаминов в крови обязательно повысится и без приема комплексов, а зимой и весной — понизится.
Витамины известны человечеству около 100 лет, а научились их получать искусственным путем немногим более 50 лет назад. А вот лето и осень, зима и весна были всегда, а вместе с ними сезонные колебания содержания витаминов в организме. Это нормальные природные биоритмы, в которые не следует вторгаться. Никому ведь в голову не придет «выравнивать» уровень половых гормонов в течение месячного цикла у женщины!
Если уж так нужно подпитывать организм, то лучше путем употребления свежих фруктов, овощей и других продуктов, которые содержат витамины. Создать гипервитаминоз через обычную пищу практически невозможно, а вот с помощью искусственно созданных веществ — запросто.
Елена Клещенок
Медицинский вестник, 26 января 2017
Поделитесь
Как терапевты разных стран лечат ОРВИ и грипп
ОРВИ — группа инфекционных заболеваний дыхательной системы, объединяющая более 200 видов разнородных вирусов. Столь высокая частота заболеваний респираторного тракта объясняется именно многообразием этиологических факторов, а также легкостью передачи возбудителя и высокой изменчивостью вирусов.
Анализ заболеваемости гриппом и ОРВИ в нашей стране за последние годы выявил ряд существенных изменений в этиологической структуре всего комплекса ОРВИ. На протяжении последних лет отмечается тенденция роста ОРВИ при отсутствии роста заболеваемости гриппом. В целом в настоящее время менее трети респираторных заболеваний приходится на грипп, а основную часть ОРВИ (до 90%) составляют респираторные вирусные инфекции негриппозной этиологии.
Эпидемиология острых респираторных инфекций имеет много общих черт независимо от возбудителя. Основным фактором, определяющим сходство эпидемического процесса при этих инфекциях, является локализация возбудителя в эпителии верхних дыхательных путей и соответственно аэрогенный механизм передачи. Он реализуется воздушно–капельным, воздушно–пылевым путями передачи. Вместе с тем при некоторых инфекциях, например, риновирусной, аденовирусной, также возможен контактный путь передачи — через воду и предметы обихода. Практически единственным источником инфекции является человек, переносящий клинически выраженную (реже — бессимптомную) форму инфекции, что дает основание отнести острые респираторные заболевания к антропонозам. Наибольшую эпидемиологическую опасность представляют человек со стертыми формами заболевания и вирусоноситель.
При лабораторной верификации возбудителей у значительного числа больных с острыми заболеваниями дыхательных путей определяются одновременно несколько вирусов — микст-инфекции, но в ряде случаев этиология, несмотря на выраженную клиническую картину респираторного вирусного заболевания, остается так и не выясненной. Клинический диагноз, подтвержденный данными лабораторных анализов, и определяет выбор терапии.
Круг препаратов, используемых при профилактике и лечении ОРВИ и гриппа, широк и разнообразен. Он включает живые и инактивированные вакцины, химиопрепараты этиотропного действия, а также средства, применяющиеся для иммунокорригирующей и патогенетической терапии.
Тем не менее, течение гриппа и других ОРВИ по-прежнему плохо поддается контролю. Это связано не только с полиэтиологичностью данных заболеваний, но и с уникальной изменчивостью вирусов и глобальным характером эпидемий. Распространение ОРВИ в значительной степени зависит от экологической, социально-экономической ситуации, наличия у пациентов аллергических заболеваний и ряда других факторов.
В настоящее время основным методом профилактики гриппа обоснованно считается вакцинация широких слоев населения. Однако следует отметить, что высокую эффективность вакцинация приобретает при условии охвата не менее 60% популяции. Поствакцинальный иммунитет, развивающийся после применения противогриппозных вакцин, не является пожизненным и не может обеспечить долгосрочной (многолетней) защиты от гриппа. Кроме того, вакцинация не обеспечивает защиты против других респираторных вирусов.
В последние годы большой интерес вызывают препараты, влияющие на иммунную систему, повышающие неспецифическую резистентность организма, а также обладающие широким спектром действия на многочисленных возбудителей ОРВИ. Известно, что наряду с реализацией специфического иммунного ответа при гриппе и других ОРВИ, то есть выработкой специфических антител к конкретному возбудителю (на чем, собственно, основана современная практика вакцинации против гриппа), большое значение в обеспечении иммунного ответа приобретают так называемые неспецифические факторы.
Среди факторов неспецифической противовирусной защиты ведущая роль принадлежит интерферонам. Интерфероны — естественные цитокины, обладающие универсальными антивирусными свойствами — способностью к подавлению репликации многих РНК- и ДНК-содержащих вирусов благодаря ингибированию процессов транскрипции и трансляции вирусных матриц. Кроме того, интерфероны повышают эффективность неспецифических защитных реакций: усиливают цитотоксичность сенсибилизированных лимфоцитов и NK–клеток, активность макрофагов, а также способствуют восстановлению нарушенного гомеостаза и оказывают иммуномодулирующее действие.
С учетом вышеизложенного перспективным для лечения ОРВИ считается применение препаратов нового класса — индукторов синтеза интерферонов. Среди появившихся в последнее время на фармацевтическом рынке препаратов — индукторов интерфероногенеза для лечения и профилактики гриппа и ОРВИ представляет интерес препарат «Кагоцел». Это оригинальное противовирусное лекарственное средство представляет собой высокомолекулярное соединение, синтезированное на основе натриевой соли карбоксиметилцеллюлозы и низкомолекулярного полифенольного альдегида природного происхождения из семян хлопчатника. Препарат вызывает образование в организме так называемого позднего интерферона, являющегося смесью альфа- и бета-интерферонов, обладающих высокой противовирусной активностью. «Кагоцел» вызывает продукцию интерферона практически во всех популяциях клеток, принимающих участие в противовирусном ответе организма: Т- и В-лимфоцитах, макрофагах, гранулоцитах, фибробластах, эндотелиальных клетках. При приеме внутрь одной дозы препарата «Кагоцел» титр интерферона в сыворотке крови достигает максимальных значений через 48 часов.
Международное общество внутренней медицины при взаимодействии в Восточной Европе с Лигой содействия клиническим исследованиям и Евроазиатским обществом инфекционистов в ноябре 2013 года инициировали самое крупное по количеству (более 20000 пациентов) неинтервенционное наблюдательное исследование FLU-EE «Лечение ОРВИ и гриппа в рутинной клинической практике». Последний включенный в исследование пациент завершил его в январе 2015 года, в настоящее время проводится обработка полученных данных.
Проведение исследования FLU-EE «Лечение ОРВИ и гриппа в рутинной клинической практике» на территории Российской Федерации было одобрено Независимым междисциплинарным комитетом по этической экспертизе клинических исследований; на территории Армении, Молдовы и Грузии — «Международным Фрайбургским этическим комитетом». Во всех странах мира диагностика и лечение больных с гриппом и ОРВИ проводится главным образом в первичных амбулаторно-поликлинических учреждениях по месту обращения и жительства пациентов. Поэтому врачами-исследователями в FLU-EE стали специалисты первичного звена здравоохранения: терапевты, семейные врачи и врачи общей практики из 262 медицинских центров России, Армении, Молдовы, Грузии.
Целью исследования было получение информации о существующих схемах лечения ОРВИ, гриппа и гриппоподобных заболеваний, назначаемых врачами в рутинной клинической практике, а также получение новой информации об эффективности и безопасности применения индукторов интерферона на большой популяции пациентов, получающих терапию в медицинских учреждениях различного типа. Это может содействовать развитию современной стратегии лечения гриппа и ОРВИ, в частности, назначению противовирусных препаратов и индукторов интерферонов. В исследование включались пациенты старше 18 лет, подписавшие информированное согласие на участие и обработку персональных данных, с установленным диагнозом гриппа или ОРВИ и назначенной врачом, на момент получения согласия, терапией. Согласно протоколу исключалось одновременное участие в других клинических исследованиях, других критериев исключения предусмотрено не было.
Лечение пациентов проводилось в соответствии со стандартами, принятыми в медицинском учреждении, и назначалось вне зависимости от данного исследования. Врачи с согласия пациента осуществляли регистрацию, систематический сбор проспективных данных в индивидуальную регистрационную карту (ИРК) для оценки развития и исхода заболевания за пациентами из медицинских записей первичной документации.
Согласно протоколу, врачу было рекомендовано проведение 3-х визитов.
В данной работе представлены результаты промежуточного отчета.
В анализ были включены следующие параметры: социально-демографические; симптомы гриппа и ОРВИ (озноб, слабость, боли в мышцах и суставах, ринит, першение в горле, кашель, склерит/конъюнктивит, головная боль), температура тела. Регистрировалась также назначенная терапия, в том числе антибактериальная. Оценка назначаемой противовирусной терапии ранжировалась в зависимости от времени обращения пациента к врачу: «раннее назначение» с 1-го по 3-й день с момента появления первых симптомов ОРВИ и гриппа и «позднее назначение» на 4-й день с момента появления первых симптомов и позже. Проводилась регистрация безопасности применения лекарственных препаратов разных групп.
В анализируемую группу из 14431 пациента вошли данные, полученные от врачей из 202 медицинских центров перечисленных выше стран. Для статистической обработки результатов исследования был использован статистический пакет SPSS 16.0.
По полу пациенты распределились следующим образом: мужчины — 6609 человек (42,06%), женщины — 8276 человек (57,35%), у 86 пациентов (0,60%) информация о поле не была указана. Средний возраст больных составил 42,5±15,0 (медиана 40,5) лет, максимальный — 96 лет, пожилые лица (согласно критериям ВОЗ старше 65 лет) — 8,52%. Преобладающее число 14236 пациентов (98,65%) принадлежали к европеоидной расе.
Все пациенты, включенные в исследование, завершили его согласно протоколу. Данные 83 (0,58%) человек, совершивших всего два визита из рекомендованных по протоколу врачу трех, вошли в анализ, так как на втором визите у них отсутствовали все анализируемые симптомы ОРВИ и гриппа, т.е. не было необходимости в проведении 3-го визита. Среднее время между визитами: первым (В1) и вторым (В2), составило 2,7±1,0 (медиана 2) дня, а среднее время между визитами В1 и третьим (В3) — 5,4±1,5 (5) дней.
На первый день появления симптомов ОРВИ и гриппа к врачу обратилось 4737 человек (32,83%), на второй — 6036 (41,83%), на третий день после появления первых симптомов заболевания и позднее — 3607 пациентов (24,99%). У 51 пациента (0,35%) время появления первых симптомов респираторного заболевания врачами указано не было или было указано некорректно. Всем пациентам лечение было назначено в день обращения к врачу на первом визите. Таким образом, можно отметить, что лечение в первые 24–48 часов от начала заболевания стали получать около двух третей больных (74,66%). Стоит также подчеркнуть, что каждый четвертый заболевший обращался за медицинской помощью к врачу на 3-й день болезни и позднее. В рассматриваемой популяции всем 14431 (100%) пациентам врачи на первом визите назначали противовирусный препарат «Кагоцел». Одновременно 38 больным (0,26%) были прописаны и другие лекарственные средства из группы J05 (противовирусные препараты для системного применения), к которой относится и «Кагоцел». Из них 33 человека (0,23%) принимали «Ингавирин», 2 (0,01%) — «Арбидол», а также «Валацикловир», «Осельтамивир» и «Эргоферон» (по одному больному соответственно).
Одновременно с противовирусной терапией «Кагоцелом» 10839 человек (75,11%) получали медикаментозные средства других групп. Противовоспалительные препараты принимали 14,5% пациентов, анальгетики — 25,48%, средства для лечения заболеваний носа — 22,72%, заболеваний горла — 24,4%, препараты, применяемые при кашле и простудных заболеваниях — 29,24% человек.
Противомикробные препараты для системного применения (J) получали 1363 пациента (9,44%), из них препараты подгруппы J01 — 1306 пациента (9,05%). Наличие каких-либо осложнений гриппа или ОРВИ, являющихся показанием к назначению антибактериальных препаратов врачи отметили только у 1163 пациентов (8,06%). Таким образом, 143 пациентам антибактериальные средства были назначены врачами без показаний, что подтверждает давнюю практику необоснованного назначения противомикробных препаратов для лечения вирусных инфекций.
Наиболее часто использовались: макролиды (азитромицин, кларитромицин) — у 3,37% больных, амоксициллин — у 2,32%, амоксициллин+клавулановая кислота — у 1,5%. Частота назначений антибактериальных препаратов при обращении к врачу на 4-й день и позже от начала болезни, выше более чем в 2 раза, чем в первые 1–3 дня от начала заболевания, что, вероятно, объяснимо присоединением бактериальных осложнений. Чем тяжелее было исходное состояние больных, тем чаще врачи назначали антибиотики, тем меньше процент пациентов, у которых полное купирование симптомов было отмечено на визите В2.
В ходе терапии «Кагоцелом» происходит достаточно быстрое купирование всех рассматриваемых в настоящем исследовании симптомов ОРВИ (озноб, слабость, боль в мышцах и суставах, ринит, першение в горле, кашель, склерит или конъюктивит, головная боль, повышенная температура тела).
На визите В2 не было отмечено симптомов заболевания у 1270 человек (8,80%), несмотря на это пациенты пришли на третий визит. На третьем визите врачами зарегистрировано отсутствие всех анализируемых симптомов ОРВИ и гриппа у 11422 пациентов (79,15%). Показательно, что с увеличением возраста замедляется положительная динамика заболеваний
Из вошедших в промежуточный анализ карт информация о нежелательных реакциях была внесена в ИРК врачами только у 3 пациентов (0,02%). В одном случае зарегистрирована тошнота, в другом — сыпь, в третьем — боли в желудке. Тошнота отмечалась у пациента, который не принимал, помимо «Кагоцела», никаких других препаратов. Сыпь наблюдалась у больного, который, помимо «Кагоцела», получал еще парацетамол и ксилометазолин. Боли в желудке отмечалась у пациента, который принимал помимо «Кагоцела» парацетамол.
У одного пациента врач зафиксировал неэффективность применения препарата «Кагоцел», и назначил антибактериальный препарат. Последнее обстоятельство может быть связано с наличием бактериальной, а не вирусной респираторной инфекции. Более подробные сведения будут представлены в следующей публикации, содержащей финальный анализ всех собранных ИРК.
В заключение хочется отметить, что впервые в условиях амбулаторной практики проанализировано лечение ОРВИ и гриппа такого количества пациентов (14431) из 202 медицинских центров нескольких стран (России, Армении, Молдовы, Грузии). Показана в динамике эффективность препарата «Кагоцел» вне зависимости от времени назначения терапии, в том числе у пожилых.
Представленные данные являются промежуточными. На основании анализа всех собранных ИРК в финальном отчете будут опубликованы окончательные результаты, за весь период проведения исследования с участием всех включенных в исследование пациентов.
Ситников И.Г.1, Еганян Г.А.2, Гроппа Л.Г.3, Фазылов В.Х.4, Корсантия Б.М.5, Можина Л.Н.6
1 Ярославский государственный медицинский университет, Российская Федерация
2 Ереванский государственный медицинский университет им. Мхитара Гераци, Республика Армения
3 Государственный университет медицины и фармации им. Николае Тестемициану, Республика Молдова
4 Казанский государственный медицинский университет, Российская Федерация
5 Институт Медицинской Биотехнологии Тбилисского Государственного медицинского университета, Грузия
6 Сибирский Государственный Медицинский Университет, Российская Федерация
По материалам Доктор Питер и Лечаший врач
Лечение и профилактика орви и гриппа у беременных
Грипп и другие острые респираторные вирусные инфекции (ОРВИ) занимают особое место среди инфекционных заболеваний беременных. Эти заболевания не являются такими безобидными, как многие думают.
Особенно это касается беременных женщин. Актуальность проблемы острых респираторных заболеваний вирусной природы определяется их распространенностью, неуправляемостью, высокой заразностью.
Современные условия урбанизации создают основу для частой встречи женщин с различными респираторными вирусами в течение всего срока беременности. Среди патологии беременных ОРВИ занимают первое место по распространенности — более 2/3 от общей заболеваемости острыми инфекциями. Это связано с высокой восприимчивостью беременных к вирусным инфекциям, что обусловлено особенностями иммунитета беременных.
Влияние вирусной инфекции на течение беременности и состояние плода характеризуется возможным инфицированием плаценты, околоплодных оболочек, а также самого плода, косвенным влиянием в результате развития у беременной лихорадки, нарушения равновесия, постоянства в организме и др. Многообразие клинических эффектов объясняется временем инфицирования к сроку беременности, свойствами и вирулентностью вируса, состоянием плацентарного барьера и защитных сил, как матери, так и плода.
Для беременных характерно затяжное течение ОРВИ при отсутствии тяжелых клинических проявлений. Это объясняется способностью вирусов респираторной группы к репродукции в плаценте, а также особенностью иммунной системы беременной (состояние физиологического иммунодефицита).
Основные клинические симптомы ОРВИ: недомогание, слабость, повышенная утомляемость на фоне субфебрильной или нормальной температуры, заложенность носа, насморк, першение в горле, переходящее в поверхностный кашель.
Наиболее характерная для беременных стертая клиника ОРВИ часто является причиной недостаточного внимания к самому факту заболевания, полагая, что «банальная простуда совершенно безвредна».
Но это не так. Вирусная инфекция может оказать на течение беременности негативное воздействие, вплоть до преждевременного отхождения околоплодных вод. Кроме того, вирус, проникая через плаценту к плоду, может вызвать инфицирование плода.
ЧТО ТАКОЕ ГРИПП?
Симптомы гриппа известны всем — это высокая температура, общая слабость, головная боль, боль в мышцах рук, ног, пояснице, боль в глазах, заложенность носа, першение в горле, сухой кашель. Могут беспокоить головокружение, тошнота, рвота, понос. Гриппом нельзя заразиться, просто промочив ноги — эта инфекция проникает в организм воздушно-капельным путем от зараженного человека.
Вирус гриппа, попав в организм, поражает эпителий респираторного тракта, особенно трахеи, начинает быстро размножаться. Повышение проницаемости сосудистой стенки приводит к появлению петехиальной сыпи на коже и слизистой оболочке щек и мягкого неба, кровоизлиянию в склеры глаз, реже — к кровохарканью, носовым кровотечениям. Грипп снижает иммунитет и тем самым способствует обострению хронических заболеваний, таких как бронхиальная астма и хронический бронхит, сердечно-сосудистые заболевания, нарушения обмена веществ, заболевания почек и др.
Кроме пневмонии грипп вызывает и такие осложнения, как воспаление мышцы сердца, которое может привести к развитию сердечной недостаточности, синусит, отит и др. Кроме этого, на ослабленный гриппом организм нередко присоединятся бактериальная инфекция — пневмококковая, гемофильная, стафилококковая. Своими осложнениями и опасен грипп во время беременности, так как он может вызвать нарушение функций всех систем организма беременной.
Самое неприятное — это угроза выкидыша или преждевременных родов. Вирус гриппа вызывает кислородное голодание плода вследствие развития комплекса нарушений со стороны плода и плаценты (фетоплацетарная недостаточность), внутриутробное инфицирование (септическое состояние, врожденная пневмония и др.) и гибель плода, отклонения в физическом и психическом развитии малыша.
ЛЕЧЕНИЕ ОРВИ И ГРИППА ВО ВРЕМЯ БЕРЕМЕННОСТИ
При появлении первых признаков ОРВИ (общая слабость, утомляемость, потеря аппетита, головная боль, подъем температуры, першение и боль в горле, кашель, насморк) необходимо обратиться за консультацией к врачу-терапевту, врачу общей практики или вызвать врача на дом, а не заниматься самолечением. Врач оценит состояние и назначит обследование и лечение.
При легком течении простудных заболеваний лечение можно начинать с использования народных средств. Рекомендуется теплое обильное питье (зеленый чай с лимоном, малиновым вареньем, медом, клюквенный и брусничный морсы, настой из цветков ромашки, липы, ягод и листьев черной смородины). Полезен напиток из шиповника, который готовят из пропорции 5 столовых ложек измельченных сухих плодов на 1 л кипятка. Смесь настаивают в термосе 8-12 часов. Теплый настой употребляют по 1 стакану 3-4 раза в день. Шиповник и черная смородина являются богатыми источниками аскорбиновой кислоты (витамина С). Необходимо помнить, что на поздних сроках беременности обильное питье может спровоцировать появление отеков.
При заболевании ОРВИ и гриппом питание должно быть калорийным и легкоусвояемым (предпочтение отдается углеводам). В рацион необходимо включать каши (манную, овсяную, гречневую и др.), картофельное и овощное пюре, мед, варенье, джем, фрукты (киви, апельсины, бананы и др.). Исключаются острые, жареные, соленые продукты. Полезным дополнением к блюдам может стать свежий лук и чеснок.
Лук и чеснок необходимо использовать при первых признаках болезни. Если по каким-то причинам нельзя употреблять эти овощи внутрь, достаточно разложить в помещении мелко нарезанные на кусочки эти ароматные продукты и вдыхать пары, в которых содержатся фитонциды, губительно действующие на вирусы и бактерии.
Если нет аллергии, рекомендуется проводить ароматерапию с использованием эфирных масел, пары которых убивают болезнетворные микроорганизмы, освежают дыхание, уменьшают отечность слизистой.
В качестве растительного иммуностимулятора можно использовать хрен. Корень хрена натереть на мелкой терке, смешать в равных пропорциях с сахаром, смесь поставить в теплое место на 12 часов, отжать выделившийся сок и принимать в первые 2 дня болезни по 1 столовой ложке через каждый час.
При ОРВИ помогает теплая ванна для рук, воздействуя на рецепторы ладоней. При использовании ванны происходит вдыхание паров воды, которые увлажняют дыхательные пути. Для усиления эффекта в воду можно добавить морскую соль, настои лекарственных трав. После приема ванны необходимо надеть варежки и теплые шерстяные носки.
При першении в горле, заложенности носа и кашле полезно назначение ингаляций с Боржоми, содовым раствором, с настоем из цветков ромашки, календулы, листьев шалфея, эвкалипта, и др. с использованием небулайзера или широких емкостей. Ингаляции рекомендуется делать 2-3 раза в день в течение 7-10 минут.
При першении и боли в горле рекомендуется полоскание горла настоем травы (ромашка, эвкалипт, календула, кора дуба), раствором соли и йода (на стакан теплой воды 1 чайная ложка соли и 2-3 капли йода). Полоскание горла необходимо до улучшения самочувствия.
При насморке обязательно регулярное проветривание и увлажнение помещения, промывание носа физиологическим раствором хлорида натрия, который можно приготовить самостоятельно (в стакане теплой кипяченой воды растворить ½ чайной ложки кухонной или морской соли) или купить физиологический раствор в аптеке. Можно использовать медицинские препараты из морской соли и воды, такие как Салин, Аква Марис, Хьюмер, Долфин и др. Промывание необходимо повторять 4-6 раз в сутки.
При подъеме температуры выше 38° помогут прохладные водные компрессы на лоб, растирание областей подмышечных и подколенных впадин, запястья, локтевых сгибов раствором уксуса (на одну часть уксуса берется три части воды).
При назначении народных средств необходимо учитывать наличие аллергических реакций на лекарственные травы, мед, лимон и др.
Во время беременности запрещается парить ноги, накладывать горчичники, посещать бани и сауны, принимать горячие ванны, использовать корень солодки при кашле, так как солодка (лакрица) вызывает отеки и подъем артериального давления. Не приветствуется активное лечение медом и малиной, так как это может привести к повышению тонуса матки, спровоцировать развитие аллергии у ребенка.
При неэффективности лечения народными средствами, но только по рекомендации врача, при ОРВИ и гриппе можно применять ряд медикаментозных препаратов, разрешенных во время беременности.
Для снижения температуры тела показан парацетомол, противопоказаны аспирин, комплексные препараты (колдрекс, фервекс, терафлю и др.), ибупрофен, нестероидные противовоспалительные препараты.
Сосудосуживающие капли в нос беременным противопоказаны, так как они вызывают сужение сосудов плаценты, повышают артериальное давление. Для лечения насморка у беременных можно использовать пиносол, если у пациентки отсутствует аллергия на эфирные масла, а также синупрет в форме драже и таблеток.
При кашле разрешается использовать мукалтин, со 2-го и 3-го триместров беременности допускается амброксол.
При боли в горле безопасны для беременных женщин спреи для горла и растворы для полоскания: Хлоргексидин, Мирамистин, Ингалипт, Аргенто Септ, Люголь, Стрепсилс Плюс, Тантум Верде, Стопангин (разрешен со 2-го триместра беременности).
Не все лекарственные средства с противовирусным действием могут быть назначены беременным, так как некоторые из них обладают токсическим действием на плод, а о безопасности применения других недостаточно информации. Для лечения и профилактики ОРВИ в течение всей беременности можно принимать Оциллококцинум, Инфлюцид. Начинать прием данных препаратов необходимо при первых симптомах заболевания.
Показаны препараты группы интерферона и индукторы интерферонов, обладающие противовирусным и иммуномодулирующим действием. Из этих препаратов допускаются к применению во время беременности следующие: со 2-го триместра беременности можно использовать свечи Виферон, на протяжении беременности допускается прием Гриппферона и Генферона (спрей назальный и капли назальные).
Умифеновир (арпетол, арбидол) обладает широким спектром противовирусного действия, кроме того, он обладает низкой токсичностью, что позволяет использовать его в качестве противовирусного средства для лечения гриппа у беременных.
Назначаемая доза умифеновира по 200 мг 4 раза в день (каждые 6 часов) 5 дней.
Вопрос о назначении антибиотиков при ОРВИ и гриппе решает врач. Во время беременности разрешены для приема антибактериальные средства пенициллинового и цефалоспоринового ряда, а также макролиды. При беременности противопоказаны тетрациклины (доксициклин), фторхинолоны (ципрофлоксацин, левофлоксацин), ко-тримоксазол и другие сульфаниламиды, аминогликозиды (канамицин, гентамицин, амикацин).
СПОСОБЫ ПРОФИЛАКТИКИ ОРВИ И ГРИППА ВО ВРЕМЯ БЕРЕМЕННОСТИ:
А. Неспецифическая профилактика
1.Соблюдение правил личной гигиены:
- «Этикет кашля» — прикрывать нос и рот салфеткой во время кашля или чихания. После использования выбрасывать салфетку в мусор. Если салфетка отсутствует чихать и кашлять в локтевой изгиб.
- Частое мытье рук с мылом и водой, особенно после кашля и чихания.
- Использование спиртсодержащих средств для мытья рук.
- Избегать близкого контакта с заболевшими (расстояние не менее 1 метра), объятий, поцелуев и рукопожатий.
- Избегать касаний руками глаз, носа, рта.
- Обязательное промывание носа и полоскание рта после возвращения домой.
2.Предупреждение инфицирования и распространения инфекций:
- Изоляция заболевших, использование отдельной посуды.
- Влажная уборка и частое проветривание помещений.
- Частые прогулки на свежем воздухе.
- Избегать пребывания в людных местах и контакта с заболевшими.
- Отмена массовых мероприятий.
- Использование средств защиты (марлевые повязки, респираторные маски).
- Смазывание слизистой носа оксолиновой мазью перед выходом на улицу во время эпидемий ОРВИ.
3.Повышение устойчивости организма:
- Прием витаминных препаратов, настоев трав, богатых витамином С (настои из шиповника и черной смородины), лимона, клюквенного и брусничного морсов).
- Рациональное питание с включением свежих овощей и фруктов, прием растительных фитонцидов (лук, чеснок, хрен).
- Лекарственная профилактика после контакта с заболевшим лицом (Гриппферон, Виферон, Оциллококцинум).
В. Специфическая профилактика гриппа.
Наиболее эффективным методом профилактики гриппа является иммунизация беременных женщин и их близких родственников.
Прививку лучше сделать на стадии планирования беременности. Если этого не произошло, прививаться можно, начиная со 2-го триместра беременности. Современные вакцины второго поколения – Флюваксин (Китай), Бегривак (Германия), Ваксигрип (Франция), Флюарикс (Бельгия) и третьего поколения – Гриппол и Гриппол плюс (РФ), Агриппал SI (Италия), Инфлювак (Нидерланды) разрешены к применению у беременных, начиная со 2-го триместра беременности, в период лактации и у детей с 6-месячного возраста.
Сделать выбор в пользу профилактической прививки – это шаг к сохранению здоровья в эпидемию гриппа.
Микша Ядвига Станиславовна, доцент кафедры поликлинической терапии БГМУ, канд. мед. наук
ЭТИОПАТОГЕНЕТИЧЕСКОЕ ЛЕЧЕНИЕ ГРИППА И ОРВИ У ДЕТЕЙ: НОВЫЙ ВЗГЛЯД НА СТАРУЮ ПРОБЛЕМУ | Шамшева
1. Шамшева О.В., Зарубаев В.В. Этиопатогенетическое лечение гриппа у детей младшего возраста. ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Эпидемиология и инфекции. 2016, 2(44). [Shamsheva O.V., Zarubayev V.V. Etiopathogenetic treatment of influenza in young children. EFFECTIVE PHARMACOTHERAPY. Epidemiology and infections. 2016, 2(44). (In Russ.)].
2. http://www.pravda.ru/accidents/factor/14-04-2011/ 1073624-remantadin-0/
3. Отчет о результатах клинического изучения лечебной эффективности препарата «АЛЬГИРЕМ» у детей с гриппом и ОРВИ. СПб.: Всесоюзный НИИ гриппа, 2003:9. [Report on the results of the clinical study of the therapeutic effectiveness of the drug ALGIREM in children with influenza and acute respiratory viral infection. St. Petersburg: All-Union Research Institute of Influenza, 2003: 9. (In Russ.)].
4. Отчет о результатах клинического изучения лечебной эффективности препарата «АЛЬГИРЕМ» у детей с гриппом и ОРВИ. СПб.: Всесоюзный НИИ гриппа, 2004:17. [Report on the results of the clinical study of the therapeutic effectiveness of the drug ALGIREM in children with influenza and acute respiratory viral infection. St. Petersburg: All-Union Research Institute of Influenza, 2004:17. (In Russ.)].
5. Бойцов В.П., Шамшева О.В., Фомичева Е.А., Зверева Н.Н., Зоненшайн Т.П., Ртищев А.Ю., Коновалов И.В. Опыт применения препарата Орвирем при острых респираторных вирусных инфекциях у детей. Детские инфекции. 2009; 3: 44—48. [Boytsov V.P., Shamsheva O.V., Fomicheva E.A., Zvereva N.N., Zonenshain T.P., Rtishchev A.Yu., Konovalov I.V. Experience of application of the drug by Orvirem in acute respiratory viral infections in children. Detskie Infektsii=Children’s infections. 2009; 3: 44—48. (In Russ.)]
6. Мазанкова Л.Н., Чебуркин А.А. Тактика и стратегия этиотропной терапии ОРВИ и гриппа у детей. Вопросы современной педиатрии. 2009; 8(16):126—130. [Mazankova L.N., Cheburkin A.A. Tactics and strategy of etiotropic therapy for acute respiratory viral infection and influenza in children. Questions of Modern Pediatrics. 2009; 8(16): 26—130. (In Russ.)]
7. Овсянников Д.Ю. Бронхолегочная дисплазия: естественное развитие, исходы и контроль. Педиатрия. 2011, 90(1):141— 150. [Ovsyannikov D.Yu. Bronchopulmonary dysplasia: natural development, outcomes and control. Pediatrics. 2011, 90 (1): 141—150. (In Russ.)]
8. Дегтярева Е.А., Овсянников Д.Ю., Жданова О.И., Лазарева С.И. Клиническая эффективность противовирусного препарата у детей «групп риска» тяжелого течения гриппа и острых респираторных заболеваний. Лечащий врач. 2010; 2. www.lvrach.ru [Degtyareva E.A., Ovsyannikov D.Yu., Zhdanova O.I., Lazareva S.I. Clinical efficacy of antiviral drug in children of «risk groups» of severe influenza and acute respiratory diseases. The Attending Physician. 2010; 2. www.lvrach.ru (In Russ.)]
9. Мурадян А.Я. Роль коронавирусной инфекции в острой патологии респираторного тракта: Автореф. … к.м.н. СПб., 2005. [Muradyan A.Ya. The role of coronavirus infection in the acute pathology of the respiratory tract: Abstract of PhD Thesis (Medicine). St.-P., 2005. (In Russ.)]
10. Афанасьева О.И., Суховецкая В.Ф., Осидак Л.В., Милькинт К.К. и др. Клинико-лабораторная характеристика и терапия ОРВИ со стенозирующим ларинготрахеитом у детей. Детские инфекции. 2005; 4(1): 32—36. [Afanasieva O.I., Suhovetskaya V.F., Osidak L.V., Milkint K.K. et al. Clinical and laboratory characteristics and therapy of acute respiratory viral infections with stenosing laryngotracheitis in children. Detskie Infektsii=Children’s infections. 2005; 4 (1): 32—36. (In Russ.)].
Лечение гриппа и ОРВИ у детей препаратом Кагоцел ® — Просмотр полного текста
Это неинтервенционное обсервационное исследование включало 80 пациентов в возрасте от 3 до 11 лет, которые были госпитализированы с симптомами гриппа и ОРВИ в любое время из начало заболевания (до 15 дней) и кому был назначен индуктор интерферона Кагоцел в качестве противовирусного препарата.
Диагноз гриппа и ОРВИ был подтвержден в соответствии с руководящими принципами Всемирной организации здравоохранения (ВОЗ) по фармакологическому лечению пандемического гриппа A (h2N1) 2009 и других вирусов гриппа.
Все обследования пациентов проводятся в соответствии с местной повседневной клинической практикой и местными и международными стандартами лечения.
После окончания лечения были собраны и проанализированы следующие данные:
- демография
- степень тяжести заболевания
- данные анамнеза (данные о вакцинации против гриппа в текущем сезоне; посещение дошкольных учреждений; предыдущие контакты с больным гриппом / ОРВИ; предыдущая противовирусная терапия при текущем эпизоде заболевания; сопутствующие заболевания)
- Температура тела (утро / вечер)
- озноб и лихорадка (совокупный балл по всем симптомам: 0 — нет симптомов, 1 — легкая, 2 — умеренная, 3 — тяжелая)
- Симптом интоксикации (совокупный балл по всем симптомам: 0 — нет симптомов, 1 — легкая, 2 — умеренная, 3 — тяжелая)
- катаральные симптомы (совокупный балл по всем симптомам: 0 — нет симптомов, 1 — легкие, 2 — умеренные, 3 — тяжелые)
- сроки: начало заболевания, первый визит к врачу, начало лечения, продолжительность заболевания
- Определение возбудителя методом ПЦР (при поступлении больных и их выписке через 5-6 дней от начала терапии)
- Противовирусная терапия (доза Кагоцела в зависимости от возраста)
- Симптоматическое лечение текущего эпизода гриппа или ОРВИ до и во время госпитализации пациента
- Бактериальные обострения (да / нет)
- Лечение бактериальных обострений (название препарата)
- нежелательные явления
грипп | Определение, симптомы, лечение и профилактика
Грипп , также называемый грипп или грипп , острая вирусная инфекция верхних или нижних дыхательных путей, которая характеризуется лихорадкой, ознобом и общим ощущением слабости и боли в мышцах, а также различной степени болезненности в голове и животе.
вирус гриппаЦветная трансмиссионная электронная микрофотография, показывающая вирусы гриппа (красный цвет) на внешней поверхности клетки-хозяина.
Библиотека научных фотографий / SuperStockБританская викторина
44 вопроса из самых популярных викторин «Британника» о здоровье и медицине
Что вы знаете об анатомии человека? Как насчет медицинских условий? Мозг? Вам нужно будет много знать, чтобы ответить на 44 самых сложных вопроса из самых популярных викторин Britannica о здоровье и медицине.
Классификация вирусов гриппа
Грипп вызывается одним из нескольких близкородственных вирусов семейства Orthomyxoviridae (группа РНК-вирусов). Вирусы гриппа подразделяются на типы A, B, C и D. Эти основные типы обычно вызывают схожие симптомы, но совершенно не связаны антигенно, так что инфицирование одним типом не дает иммунитета против других. Вирусы A вызывают большие эпидемии гриппа, а вирусы B вызывают небольшие локальные вспышки.Вирусы C вызывают у людей только легкие респираторные заболевания. Вирусы гриппа D не заражают людей и наблюдались только у свиней и крупного рогатого скота.
Вирусы гриппа A подразделяются на подтипы, а вирусы гриппа B и подтипы гриппа A далее делятся на штаммы. Подтипы гриппа A дифференцируются в основном на основе двух поверхностных антигенов (чужеродных белков) — гемагглютинина (H) и нейраминидазы (N). Примеры подтипов гриппа A включают h2N1, H5N1 и h4N2.Вирусы гриппа B подразделяются на две основные линии: B / Yamagata и B / Victoria. Штаммы гриппа B и штаммы подтипов гриппа A, кроме того, различаются вариациями в генетической последовательности.
Эволюция и вирулентность вирусов гриппа
Между всемирными вспышками, известными как пандемии, вирусы гриппа претерпевают постоянную быструю эволюцию (процесс, называемый антигенным дрейфом), который обусловлен мутациями в генах, кодирующих антигенные белки. Периодически вирусы претерпевают серьезные эволюционные изменения, приобретая новый сегмент генома у другого вируса гриппа (антигенный сдвиг), фактически становясь новым подтипом.Эволюции вирусов способствуют такие животные, как свиньи и птицы, которые служат резервуарами вирусов гриппа. Когда свинья одновременно заражена разными вирусами гриппа А, такими как человеческие, свиньи и птичьи штаммы, может произойти генетическая перегруппировка. Этот процесс приводит к появлению новых штаммов гриппа A.
Получите подписку Britannica Premium и получите доступ к эксклюзивному контенту. Подпишись сейчасНедавно появившиеся вирусы гриппа имеют тенденцию быть изначально высоко инфекционными и вирулентными для людей, поскольку они обладают новыми антигенами, против которых человеческий организм не имеет подготовленной иммунной защиты (т.е., существующие антитела). Как только значительная часть населения вырабатывает иммунитет за счет выработки антител, способных нейтрализовать новый вирус, заразность и вирулентность вируса снижается. Хотя вспышки вирусов гриппа обычно наиболее смертельны для маленьких детей и пожилых людей, уровень смертности среди людей в возрасте от 20 до 40 лет иногда бывает неожиданно высоким, даже если пациенты получают лечение. Считается, что это явление связано с гиперреакцией иммунной системы на новые штаммы вируса гриппа.Такая реакция возникает в результате перепроизводства воспалительных веществ, называемых цитокинами. Высвобождение чрезмерного количества этих молекул вызывает сильное воспаление, особенно в эпителиальных клетках легких. Люди, чья иммунная система не полностью развита (например, младенцы) или ослаблены (например, пожилые люди), не могут вызвать такой смертельный иммунный ответ.
Пандемии и эпидемии
Пандемии гриппа, по оценкам, происходят в среднем один раз в 50 лет.Эпидемии случаются гораздо чаще, и сезонный грипп появляется ежегодно в большинстве регионов мира, иногда в масштабах эпидемии. Вирус гриппа типа А является наиболее частой причиной сезонного гриппа. Когда вирус гриппа А претерпевает антигенный сдвиг, пандемия, затрагивающая большую часть мира, может произойти в течение нескольких месяцев. Пандемия гриппа 1918–1919 годов, самая разрушительная вспышка гриппа в истории и одна из самых тяжелых пандемий, когда-либо встречавшихся, была вызвана подтипом гриппа A, известным как h2N1.Во время этой пандемии около 25 миллионов человек во всем мире умерли от так называемого испанского гриппа, который впервые был широко зарегистрирован в Испании, но возник в американском штате Канзас.
Последующие пандемии гриппа были менее серьезными. Например, грипп A подтипа h3N2, или пандемия гриппа 1957 года, по-видимому, начался в Восточной Азии в начале 1957 года и к середине года охватил весь земной шар. Вспышка продолжалась на уровне пандемии примерно до середины 1958 года и вызвала, по оценкам, от одного до двух миллионов смертей во всем мире.После 10 лет эволюции, которая привела к ежегодным эпидемиям, грипп 1957 года исчез в 1968 году только для того, чтобы быть замененным новым подтипом гриппа A, h4N2. Этот вирус все еще находится в обращении. Вспышка гриппа 1968 года стала третьей пандемией гриппа в 20-м веке, в результате которой, по оценкам, погибло от одного до четырех миллионов человек.
В 1997 году вирус птичьего гриппа, или вирус птичьего гриппа, распространился среди домашних птиц в Гонконге, а затем заразил небольшое количество людей, убив некоторых из них.Тот же самый вирус, H5N1, снова появился среди кур в Юго-Восточной Азии зимой 2003–04 годов, снова заразив некоторых людей со смертельным исходом, и с тех пор он периодически появлялся снова, в основном у диких птиц, домашних птиц и людей. Известно несколько других подтипов вирусов птичьего гриппа, включая H7N2, H7N3 и H9N2. Хотя эти подтипы редко вызывают инфекцию у людей, считается, что они обладают эпидемическим и пандемическим потенциалом.
Вспышка ранее неизвестного штамма h2N1 произошла в 2009 году.Первоначально заболевание называлось свиным гриппом, поскольку предполагалось, что вирус передается людям от свиней, болезнь сначала разразилась в Мексике, а затем распространилась на Соединенные Штаты. Было обнаружено, что вирус h2N1, вызвавший вспышку, обладает генетическим материалом от вирусов гриппа человека, птиц и двух разных вирусов свиного гриппа. Вспышка h2N1 в 2009 г. была не столь смертоносной, как пандемия 1918–1919 годов. Однако вирус был очень заразным и быстро распространялся. Пандемический потенциал нового вируса h2N1 был разъяснен международному сообществу Всемирной организацией здравоохранения (ВОЗ), которая объявила 29 апреля 2009 года предупреждение о пандемии пятого уровня.Это побудило к быстрому внедрению процедур смягчения последствий, включая распределение лекарств по лечебным учреждениям в странах по всему миру. Несмотря на эти меры, вирус продолжал распространяться по всему миру. 11 июня 2009 г., после увеличения числа случаев заболевания в Чили, Австралии и Соединенном Королевстве, ВОЗ повысила уровень опасности вируса h2N1 с 5 до 6, что означает, что вспышка была официально объявлена пандемией. К середине января 2010 года вспышка охватила людей более чем в 209 странах мира.Это была первая пандемия гриппа 21 века. В Соединенных Штатах высокие уровни гриппоподобных заболеваний, наблюдавшиеся во время пандемии h2N1 в 2009 г., не наблюдались до 2018 г.
Исследования показали, что каждой из четырех исторических пандемий гриппа предшествовало событие Ла-Нинья — изменение глобального погодные условия, связанные с прохладной температурой морской поверхности в Тихом океане, что, как предполагают некоторые ученые, могло изменить характер миграции птиц, возможно, увеличив их взаимодействие с домашними животными и сделав возможной генетическую перегруппировку и появление новых пандемических штаммов вирусов гриппа.
Лечение ОРВИ в Киеве
ОРВИ (ОРВИ) — инфекционные вирусные заболевания, которыми легко заразиться в местах массового скопления людей — общественном транспорте, офисах, магазинах и т. Д. влияет на человека, когда его организм по каким-то причинам ослаблен. Например, люди часто простужаются в период резких перепадов температур весной и осенью, а также в период зимних заморозков.
СИМПТОМЫ ОРВИОРВИ проявляются через:
- кашель;
- насморк;
- высокая температура;
- головные боли;
- ревматическая боль.
Иногда могут появиться такие осложнения, как отит (воспаление уха) или гайморит (воспаление носовых пазух). При некоторых осложнениях голос мужчины может искажаться — он может стать хриплым.
Симптомы ОРВИ могут быть похожи на симптомы других заболеваний, например, бронхита и гриппа; поэтому лучше проконсультироваться с квалифицированными специалистами по лечению ОРВИ.
ЛЕЧЕНИЕ И ПРОФИЛАКТИКА ОРВИДля лечения ОРВИ используются жаропонижающие, противовирусные препараты, капли и спреи, облегчающие насморк. В некоторых случаях врачи могут порекомендовать противовоспалительные или противовирусные препараты. При кашле врачи назначают отхаркивающие средства или курсы ингаляций.
ОРВИ очень заразны; поэтому рекомендуется максимально ограничить контакт с больным и обязательно носить марлевые маски для лица больному и контактирующим с ним.Также всегда важно соблюдать правила личной гигиены, пользоваться индивидуальной посудой, посудой и при необходимости избегать контакта с больными людьми.
Врачи Oxford Medical помогут вылечить ОРВИ, избежать возможных осложнений и укрепить иммунитет. В дневном стационаре возможно полноценное лечение, не отвлекаясь от повседневной жизни.
В Российской Федерации продолжается эпидемический сезон по заболеваемости гриппом и ОРВИ, характерный для этого времени года
Возбудители гриппа и ОРВИ передаются от человека к человеку воздушно-капельным путем и весьма заразны (заразны).
При ОРВИ — ОРВИ
негриппозной этиологии заболевание развивается постепенно, чаще всего начинается с переутомления и насморка, сухого кашля, который затем становится влажным.
Когда грипп поражает сосуды, возможно кровотечение десен и слизистой оболочки носа. После перенесенного гриппа организм становится чрезвычайно восприимчивым к различным инфекциям, что приводит к тяжелым инфекционным осложнениям.
Особо тяжелые ОРВИ и грипп возникают у детей раннего возраста, пожилых людей, людей с хроническими патологиями и заболеваниями иммунной системы.
Лучшая защита от гриппа — это иммунизация. Однако вакцинация не защищает от других ОРВИ.
Укреплению организма способствует правильное питание. Включите в рацион продукты, содержащие витамины А, С, цинк и кальций: цитрусовые, киви, сладкий перец, молочные и молочные продукты, твердые сыры, отварную рыбу, говяжью морковь со сметаной, изюм или курагу и др.
Планируя посещение общественных мест, возьмите с собой медицинскую маску: если вы чихаете и кашляете в общественном месте, закройте рот и нос медицинской маской или носовым платком — это поможет предотвратить заражение.
Любое вирусное заболевание, перенесенное «на ногах», в дальнейшем может привести к нежелательным последствиям и осложнениям.
Кроме того, больной заражает других.
Грипп — инфекционное заболевание, которым может заразиться каждый. Возбудитель гриппа — вирус, попадающий от инфицированных людей в носоглотку других людей.
Большинство людей болеют гриппом всего несколько дней
, но некоторые люди заболевают более серьезно, возможно, имеют тяжелую болезнь, даже смерть.
С гриппом обострились существующие хронические заболевания; Кроме того, у гриппа есть обширный список возможных осложнений:
Легочные осложнения (пневмония, бронхит). Пневмония — причина большинства смертей от гриппа.
Осложнения со стороны ЛОР-органов и ЛОР-органов (отиты, синуситы, риниты, трахеиты).
Осложнения сердечно-сосудистой системы (миокардит, перикардит).
Осложнения нервной системы (менингит, менингоэнцефалит, энцефалит, невралгия, полирадикулоневрит).
Чтобы избежать возможных осложнений, важно своевременно проводить профилактику гриппа и правильно лечить само заболевание.
Обычно грипп начинается внезапно. Возбудители гриппа, вирусы типов A и B, отличаются агрессивностью и исключительно высокой скоростью размножения, поэтому в течение нескольких часов после заражения вирус приводит к глубоким поражениям слизистой оболочки дыхательных путей, открывая возможности для проникновения в нее бактерий.
Симптомы гриппа включают лихорадку, температуру 37.5–39 ° C, головная боль, боль в мышцах или суставах, озноб, усталость, кашель, насморк или заложенность носа, боль и першение в горле.
Что делать, если у вас грипп?
При первых симптомах самому пациенту нужно оставаться дома, чтобы не только не заразить окружающих, но и вовремя начать лечение, для чего немедленно обратиться к врачу. Чтобы предотвратить дальнейшее распространение инфекции, пациента необходимо изолировать.
от здоровых людей, желательно выделить отдельную комнату.
Важно!
При гриппе крайне важно соблюдать постельный режим, так как болезнь увеличивает нагрузку на сердечно-сосудистую, иммунную
и другие системы организма.
Самолечение гриппа недопустимо, и врач должен поставить диагноз и назначить необходимое лечение в зависимости от состояния и возраста пациента.
Для правильного лечения необходимо строго соблюдать все рекомендации лечащего врача и своевременно принимать лекарства.Кроме того, рекомендуется обильное питье — это может быть горячий чай, клюквенный или брусничный сок, щелочная минеральная вода. Пить нужно чаще и как можно больше.
Важно!
При температуре 38 — 39 ° C вызвать на дом участкового врача или бригаду скорой помощи.
При кашле и чихании больной должен прикрывать рот и нос платком или салфеткой.
Помещение, в котором находится больной, следует регулярно проветривать и проводить там влажную уборку как можно чаще, желательно с использованием дезинфицирующих средств, действующих на вирусы.
Общение с заболевшим гриппом следует ограничить, а при уходе за ним использовать медицинскую маску или марлевую повязку.
Как уберечься от гриппа?
Согласно позиции Всемирной организации здравоохранения, наиболее эффективным средством против гриппа является вакцинация, поскольку именно вакцина обеспечивает защиту от тех видов вируса гриппа, которые наиболее актуальны в данный эпидемиологический сезон и входят в его состав.
Введение вакцины в организм не может вызвать заболевания, но за счет выработки защитных антител стимулирует иммунную систему к выздоровлению.
ПРАЙМ PubMed | [ИСПОЛЬЗОВАНИЕ ЦИКЛОФЕРОНА ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ГРИППА И ОСТРЫХ ДЫХАТЕЛЬНЫХ ВИРУСНЫХ ИНФЕКЦИЙ]
Abstract
Результаты применения циклоферона, низкомолекулярного индуктора выработки интерферона, для лечения и профилактики гриппа и острых респираторных вирусов представлены инфекции (ОРВИ) у взрослых и детей. Показано, что уменьшает симптомы этих заболеваний и их продолжительность, корректирует дисбаланс активности иммунной системы, предотвращает осложнения, снижает частоту гриппа и ОРВИ.Эффективность циклоферона не зависела от этиологии заболевания.
Цитата
Алимбарова, Л. «[ИСПОЛЬЗОВАНИЕ ЦИКЛОФЕРОНА ДЛЯ ЛЕЧЕНИЯ и ПРОФИЛАКТИКИ ГРИППА и ОСТРЫХ ДЫХАТЕЛЬНЫХ ВИРУСНЫХ ИНФЕКЦИЙ]». Клиническая Медицина, т. 93, нет. 3, 2015, с. 57-63.
Алимбарова Л. [ПРИМЕНЕНИЕ ЦИКЛОФЕРОНА ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ГРИППА И ОСТРЫХ ДЫХАТЕЛЬНЫХ ВИРУСНЫХ ИНФЕКЦИЙ]. Клин Мед (Моск) . 2015; 93 (3): 57-63.
Алимбарова, Л.(2015). [ИСПОЛЬЗОВАНИЕ ЦИКЛОФЕРОНА ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ГРИППА И ОСТРЫХ ДЫХАТЕЛЬНЫХ ВИРУСНЫХ ИНФЕКЦИЙ]. Клиническая Медицина , 93 (3), 57-63.
Алимбарова Л. [ПРИМЕНЕНИЕ ЦИКЛОФЕРОНА для ЛЕЧЕНИЯ и ПРОФИЛАКТИКИ ГРИППА и ОСТРЫХ ДЫХАТЕЛЬНЫХ ВИРУСНЫХ ИНФЕКЦИЙ]. Клин Мед (Москва). 2015; 93 (3): 57-63. PubMed PMID: 26168605.
TY — JOUR T1 — [ИСПОЛЬЗОВАНИЕ ЦИКЛОФЕРОНА ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ГРИППА И ОСТРЫХ ДЫХАТЕЛЬНЫХ ВИРУСНЫХ ИНФЕКЦИЙ].А1 — Алимбарова, Л, PY — 2015/7/15 / entrez PY — 2015/7/15 / pubmed PY — 2015/8/13 / medline СП — 57 EP — 63 JF — Клиническая медицина JO — Клин Мед (Москва) ВЛ — 93 ИС — 3 N2 — Представлены результаты использования циклоферона, низкомолекулярного индуктора выработки интерферона, для лечения и профилактики гриппа и ОРВИ у взрослых и детей. Было показано, что он снижает симптомы этих заболеваний и их продолжительность, коррекция дисбаланса деятельности иммунной системы, предотвращение осложнений, снижение частоты гриппа и ОРВИ.Эффективность циклоферона не зависела от этиологии заболевания. SN — 0023-2149 UR — https://www.unboundmedicine.com/medline/citation/26168605/[the_use_of_cycloferon_for_the_treatment_and_prevention_of_influenza_and_acute_respiratory_viral_infections]. L2 — https://medlineplus.gov/flu.html БД — ПРЕМЬЕР DP — Unbound Medicine ER —
Оценка эффективности схемы лечения ОРВИ, включая этиотропное (йодид енизама) и симптоматическое лечение
Оценка эффективности схемы лечения ОРВИ, включая этиотропное (йодид енизама) и симптоматическое лечение | МетаТерапевтический архив
Д А ЛиозновЕ В Шахланская
Реферат
Оценить эффективность применения противовирусного препарата енизамия йодид в комплексном лечении острых респираторных вирусных инфекций (ОРВИ), вызванных различными возбудителями, в рутинной клинической практике.В проспективное рандомизированное исследование вошли 134 пациента, которые лечились в сезон эпидемии гриппа и ОРВИ в 2018–2019 годах. Все пациенты были обследованы на наличие вирусов гриппа A и B, респираторно-синцитиального вируса, метапневмовируса человека, вируса парагриппа, коронавирусов, риновирусов, аденовирусов. в мазках из носоглотки методом ПЦР. Пациенты основной группы получали йодид энисамиума на фоне симптоматической терапии, контрольная группа — только симптоматическая терапия. Первичный параметр эффективности терапии оценивался по шкале общей тяжести проявлений ОРВИ (Total Symptom Score TSS) со 2-го по 4-й день и по вторичным критериям эффективности: оценка длительности ОРВИ, степень тяжести лихорадки, доля пациентов с нормальной температурой тела, длительность основных клинических симптомов ОРВИ, доля пациентов, у которых отмечены осложнения, требующие применения антибиотиков, динамика интерферонового статуса…Продолжить чтение
Связанные концепции
Амизон
Противовирусные агенты
Homo sapiens
Иодиды
Перспективные исследования
Пиридины
0002000 Антивирус
000000000
000
000000 Инфекции, связанные с респираторными путями Корма
Аллергия и инфекционные заболевания (ASM)
Аллергия возникает в результате гиперреактивности иммунной системы к некоторым веществам окружающей среды и может быть опасной для жизни.Инфекционные заболевания вызываются организмами, включая бактерии, вирусы, грибки и паразиты. Они могут передаваться разными путями, например от человека к человеку. Вот последние исследования по аллергии и инфекционным заболеваниям.
Противовирусные препараты (ASM)
Противовирусные препараты — это лекарства, которые используются специально для лечения вирусных инфекций. Ознакомьтесь с последними исследованиями в области противовирусных препаратов здесь.
Противовирусные препараты
Противовирусные препараты — это лекарства, которые используются специально для лечения вирусных инфекций.Ознакомьтесь с последними исследованиями в области противовирусных препаратов здесь.
Аллергия и инфекционные заболевания
Аллергия возникает в результате гиперреактивности иммунной системы к некоторым веществам окружающей среды и может быть опасной для жизни. Инфекционные заболевания вызываются организмами, включая бактерии, вирусы, грибки и паразиты. Они могут передаваться разными путями, например от человека к человеку. Вот последние исследования по аллергии и инфекционным заболеваниям.
Статьи по теме
Scientia Pharmaceutica
Элеонора Халтнер-Укомадув И Маргитич
Терапевтический архив
Е.В. СилинаГ А Еганян
Э.В.
Терапевтический архив
В.К. ФазыловБ М Корсантия
/ статьи / оценка-эффективности-лечения-арви / 32598793
Проблема бактериальных осложнений после респираторных вирусных инфекций
Каждый человек в течение своей жизни неоднократно заражается различными респираторными вирусами, которые представляют собой факторы риска развития бактериальных осложнений.Среди этиологических факторов ОРВИ наиболее опасным является вирус гриппа А. Этот вирус способен вызывать катастрофические пандемии с высокой смертностью, в основном из-за вторичной бактериальной пневмонии. Как показали многочисленные недавние исследования, основным механизмом провоцирования бактериальных инфекций независимо от типа респираторного вируса является несбалансированный ответ противовирусного врожденного иммунитета — чрезмерный ответ интерферона и неконтролируемое воспаление. Вероятность тяжелых бактериальных осложнений в течении ОРВИ определяется как вирулентностью самого вируса, так и составом респираторной микробиоты на момент вирусной инфекции, а также генетическими характеристиками организма.На возникновение серьезных бактериальных осложнений также влияют хронические заболевания, которые влияют на регуляцию врожденного иммунного ответа. В этом обзоре суммируется текущая концепция механизмов развития поствирусных бактериальных осложнений, а также возможные стратегии профилактики этих осложнений.
По оценкам Всемирной организации здравоохранения (ВОЗ), от острых респираторных вирусных инфекций (ОРВИ) ежегодно умирает 3,9 миллиона человек [1].Эти инфекции поражают все возрастные группы, но сильнее всего влияют на здоровье детей, пожилых людей и людей с хроническими заболеваниями. Риск ОРВИ определяется их способностью спровоцировать вирусную пневмонию и вторичные бактериальные инфекции, например бактериальная пневмония, отит, менингит, а также хронические заболевания легких. Таким образом, респираторные вирусы вызывают примерно половину всех случаев внебольничной пневмонии (ВП) у детей. Кроме того, они вызывают более 90% случаев бронхиолита у младенцев и 85-95% случаев обострения астмы у детей.Вне периода пандемии гриппа ОРВИ являются причиной 30-50% случаев ВП, 80% обострений астмы и 20-60% обострений хронической обструктивной болезни легких (ХОБЛ) у взрослых. В целом эти инфекции являются одной из пяти основных причин смертности населения в мире, а во многих развивающихся странах они являются ведущими причинами смертности детей в возрасте до пяти лет.
В отличие от других респираторных вирусов, вирус гриппа A представляет наибольшую опасность из-за его циркуляции у разных видов животных и способности реассортировать геномные фрагменты, что приводит к быстрой модификации основных поверхностных антигенов вируса — гемагглютинина (НА) и нейраминидазы ( NA) (антигенный сдвиг).Этот механизм определяет возможность появления новых антигенных вариантов вирусов гриппа А, таких как h2N1, h3N2, h4N2, h2N1pdm09, которые стали причиной четырех известных пандемий [2, 3].
В периоды между пандемиями вирусы гриппа также претерпевают антигенные изменения, вызванные постепенным накоплением мутаций в HA и NA (антигенный дрейф), что приводит к возникновению сезонных эпидемий.
Даже сейчас, в 21 веке, когда доступны противогриппозные препараты и антибиотики широкого спектра действия, у людей с сезонным гриппом есть вероятность развития осложнений.Таким образом, как вирус-индуцированный острый респираторный дистресс-синдром (ОРДС), так и вторичная бактериальная пневмония могут развиться в течение первой недели после вирусной инфекции. По данным ВОЗ, грипп вызывает до 650 000 смертей во всем мире ежегодно [1]. По данным Центров по контролю и профилактике заболеваний (CDC, Атланта, Джорджия, США), в США с населением около 300 миллионов человек уровень смертности от гриппа колеблется от 16 000 до 56 000 случаев в год. В Российской Федерации с населением около 140 миллионов человек смертность от сезонного гриппа оценивается на уровне нескольких сотен в год, хотя официальных данных в открытом доступе нет.Различие в статистике смертности от гриппа в разных странах можно определить по разнице в методах расчета. Например, статистика смертности от бактериальной пневмонии может не учитывать роль вирусного этиологического фактора как провокатора вторичной инфекции. Таким образом, лица, умершие от бактериальной пневмонии, могут не учитываться при расчете уровня смертности от гриппа, даже если бактериальные осложнения были спровоцированы первичной инфекцией гриппа.
Пандемия вируса гриппа A (h2N1) (испанский грипп) 1918 года была самой смертельной из когда-либо зарегистрированных эпидемий гриппа. В ходе этой пандемии, случившейся во время Первой мировой войны, было инфицировано 50% населения мира, в результате чего погибло около 40-50 миллионов человек [4]. От пандемии больше всего страдали люди в возрасте от 20 до 40 лет, служившие в армии. Поскольку вирус гриппа был открыт в 1933 году, во время пандемии в Испании этиологический агент болезни еще не был идентифицирован.В то время микробиологи пытались связать испанский грипп с различными бактериальными возбудителями, в частности с Haemophilus influenzae (H.influenzae) [5]. Теперь, благодаря доступности метода ПЦР, стало возможным идентифицировать гены вируса гриппа в вскрытых и гистологических образцах того времени и реконструировать испанский вирус h2N1 с помощью обратной генетики. Удивительно, но реконструированный вирус не имел радикальных отличий по генетической структуре от циркулирующих в настоящее время вирусов [6].Последующее исследование вскрытых образцов показало, что более 90% проанализированных образцов легочной ткани умерших во время пандемии гриппа в Испании имели признаки бактериальной инфекции [7-9]. Оказалось, что 95% смертей были вызваны не самим вирусом гриппа, а последующей бактериальной пневмонией. В частности, было доказано, что Streptococcus pneumoniae (S. pneumoniae) был основным инфекционным агентом, вызвавшим диагностированную пневмонию [10]. Вскрытие показало наличие S.pneumoniae в легких 44% и в крови 33% больных, умерших от испанского гриппа [10, 11]. Хотя S. pneumoniae была основной причиной смертности, другие инфекционные агенты, такие как Staphylococcus aureus (S. aureus) , H. influenzae и ряд других Streptococcus spp . были также идентифицированы при вскрытии образца легкого [5, 7]. Следовательно, катастрофический исход пандемии гриппа 1918 года мог быть определен нехваткой вакцин и противовирусных препаратов против вируса гриппа, а также отсутствием антибиотиков, которые могли бы подавить вторичные бактериальные осложнения.
Пандемия гриппа в эпоху антибиотиков при отсутствии вакцинации и противовирусных препаратов
В 1957 году пандемия азиатского гриппа поразила 40-50% людей во всем мире с оценками общей смертности от 1,5 до 4 миллионов человек [13], а число погибших в Соединенных Штатах достигло около 69 800 человек [13-15]. Причиной пандемии стал штамм вируса гриппа A (h3N2) [12]. Анализ вскрытых образцов показал наличие бактериальной инфекции в 80% всех тяжелых и смертельных случаев [8, 16, 17].Следует отметить, что к этому времени такие антибиотики, как пенициллин и стрептомицин, уже были доступны и использовались в медицинской практике в развитых странах. Однако во время этой пандемии в США и ряде других стран произошло заметное увеличение количества госпитализаций, связанных с пневмонией, вызванной в основном S. pneumoniae , H. influenzae и S. aureus [18 ]. Аналогичные данные были получены в Нидерландах, где из 148 смертей, предположительно вызванных азиатской пандемией гриппа, 75% были связаны с бактериальной пневмонией, спровоцированной в 15% случаев S.pneumoniae и в 59% случаев — S. aureus [16]. Следует отметить, что приведенные данные бактериологического исследования могли быть сильно искажены, так как в то время многие пациенты уже лечились антибиотиками [19].
Общее число погибших от пандемии в Гонконге 1968-1969 гг., Вызванной штаммом вируса гриппа A (h4N2), составило около 2 миллионов человек [20, 21]. Увеличение смертности от респираторных инфекций на 55%, в большинстве случаев сопровождающееся вторичной бактериальной пневмонией, было зарегистрировано в Великобритании в 1969 г. [22].Стафилококковая пневмония оказалась основным осложнением гонконгского гриппа h4N2. Например, из 129 взрослых, у которых был диагностирован пандемический грипп, пневмония была обнаружена в 16% случаев, из которых 40% (6% из всех 129 случаев гриппа) закончились летальным исходом. S. aureus или Pseudomonas aeruginosa (P. aeruginosa) были обнаружены в 75% вскрытых образцов умершего [23]. Следует отметить, что в ходе пандемии в Испании большинство летальных случаев вторичной бактериальной пневмонии было вызвано S.pneumonia , но во время пандемий 1957 и 1968 годов преобладающим этиологическим агентом вторичной бактериальной пневмонии стал S. aureus . Это можно объяснить повышенной устойчивостью к антибиотикам S. aureus из-за широкого использования антибиотиков населением в то время.
Пандемия гриппа в присутствии противогриппозных вакцин, противовирусных препаратов и антибиотиков
Вспышка вируса гриппа A (h2N1) pdm09 в 2009 г. распространилась на 41 страну в течение четырех недель и переросла в пандемию [20, 24 ].Компонент h2N1 вакцин против сезонного гриппа, произведенных в 2009 г., не соответствовал антигенным свойствам недавно появившемуся пандемическому штамму A (h2N1) pdm09. Считается, что общее число погибших от этой пандемии составило около 284 000 человек во всем мире [25]. Частыми причинами смерти в ходе этой пандемии в США были вторичные бактериальные инфекции, вызванные в основном S. pneumoniae и S. pyogenes [26, 27]. Другие исследования в США показали, что почти в 30% из 77 летальных случаев инфекция гриппа сопровождалась бактериальными инфекциями, 46% из которых были вызваны S.pneumoniae , 9% — S. aureus и 1% — H. influenzae . Palacios et al. исследовал мазки из носоглотки почти 200 пациентов с пандемическим гриппом и обнаружил H. influenzae в 52% образцов, S. pneumoniae в 31% и S. aureus в 18% образцов соответственно [28 ]. Тяжесть заболевания чаще всего была связана с вторичной инфекцией, вызванной S. pneumoniae .
В другом исследовании 838 тяжелобольных детей в США было показано, что через 72 часа после госпитализации в отделение интенсивной терапии бактериальная суперинфекция развилась у 33% пациентов, 48% из которых были вызваны метициллин-резистентными. С.aureus (MRSA), в 5,5% случаев — S. pneumoniae и 5% — H. influenzae [29].
Таким образом, несмотря на повсеместное внедрение сезонных противогриппозных вакцин, противовирусных препаратов и антибиотиков, проблема бактериальных осложнений течения гриппа не перестает быть актуальной. Более того, из-за развития устойчивости бактериальной флоры к современным антибиотикам эта проблема может обостриться в случае новой пандемии гриппа [30].
Респираторные вирусные инфекции не гриппозной этиологии как провокаторы вторичной бактериальной пневмонии
Современная диагностика позволяет ученым анализировать бактериальные осложнения при различных респираторных инфекциях, не связанных с гриппом. В таблице 1 обобщены многочисленные исследования, показывающие взаимосвязь респираторных вирусных патогенов с некоторыми бактериями, которые могут вызывать пневмонию, средний отит, синусит и менингит в качестве осложнений. Несмотря на то, что другие респираторные вирусы не способны вызывать пандемии, эти вирусы оказались столь же опасными, как и грипп, в провоцировании вторичных бактериальных осложнений.Например, представитель семейства Paramyxoviridae , метапневмовирус человека (hMPV), может вызывать серьезные осложнения, такие как вирус гриппа, включая как вирусную пневмонию с развитием ОРДС, так и бактериальную пневмонию [31]. Другой представитель этого семейства — респираторно-синцитиальный вирус (РСВ) — оказался даже более опасным, чем грипп, по уровню смертности среди госпитализированных пациентов с диагнозом пневмония. Таким образом, смертность от всех причин через 20 дней после госпитализации была выше у пациентов с RSV-инфекцией (18.4%), чем у больных гриппом (6,7%) [32]. К сожалению, не существует вакцин и эффективных противовирусных препаратов для профилактики и лечения пневмовирусов, а также большинства респираторных вирусов не гриппозной этиологии.
Хотя обсервационные исследования взаимосвязи вирусных и бактериальных инфекций, проведенные в разных регионах мира, приводят к согласованным выводам, они могут различаться в оценке роли различных патогенов в развитии бактериальной ВП.Это можно объяснить значительным влиянием климатических условий и генетических характеристик населения на распространенность отдельных вирусных и бактериальных патогенов.
В США обследовали 1024 пациента с ВП и сравнили с группой из 759 контрольных пациентов без симптомов [48]. Оказалось, что вирусы гриппа, RSV, hMPV и, в меньшей степени, вирусы парагриппа и коронавирусы значительно чаще выделялись из группы пациентов с диагнозом пневмония, независимо от возраста пациента.В то же время риновирусы были частой причиной ВП у взрослых, но практически не диагностировались у детей с пневмонией. Напротив, аденовирусы были связаны с ВП только у детей младше 2 лет.
В исследовании, проведенном в Японии с участием 2617 пожилых (≥65 лет) пациентов с диагнозом хронические респираторные или другие сопутствующие заболевания, вирусные патогены были изолированы в 23,1% случаев [49]. Риновирусы были наиболее частой причиной пневмонии (9.8%), тогда как и грипп, и RSV были обнаружены в 3,9% случаев. RSV чаще всего диагностировался у людей с хроническими респираторными заболеваниями, тогда как другие вирусы были связаны с пневмонией, независимо от наличия респираторных и других хронических заболеваний. В целом вирусные инфекции не предопределяли повышенного риска смертности пациентов с пневмонией, но грипп привел к трехкратному увеличению смертности пациентов с хроническими респираторными заболеваниями. Следовательно, вклад вирусной инфекции в смертность от пневмонии зависит от типа вирусного агента и наличия сопутствующих заболеваний.
Южнокорейское метааналитическое исследование, проведенное с участием 5 298 пациентов разных возрастных групп, показало, что провокация бактериальной суперинфекции характерна для всех вирусных респираторных инфекций [50]. Однако тип бактериального патогена, вызывающего вторичную инфекцию, может зависеть как от типа вирусной инфекции, так и от возраста пациента. Например, вирусные инфекции гриппа A и B, риновирус и hMPV вызвали пневмонию у взрослых пациентов, которая была связана с S.aureus , тогда как коронавирус, вирус парагриппа и RSV привели к пневмонии, связанной с грамотрицательными бактериями Klebsiella spp . и Acinetobacter spp. Инфекция микоплазмы ( M. pneumonia ) была наиболее частой причиной бактериальной пневмонии у детей независимо от типа предыдущей вирусной инфекции. Эти исследования подчеркивают важность вирусной диагностики у пациентов с вторичной бактериальной пневмонией с точки зрения выбора правильной антибактериальной терапии.Например, поствирусная пневмония у младенцев и детей должна лечиться антибиотиками, активными против M. pneumoniae (макролиды). Взрослых с гриппом, hMPV или риновирусной инфекцией следует лечить антибиотиками, которые эффективно убивают стафилококковые бактерии, тогда как антибиотики, активные против широкого спектра грамотрицательных бактерий, следует назначать в случаях заражения коронавирусом и вирусом парагриппа.
Однако, как отмечалось выше, взаимосвязь между генотипом популяции и климатическими условиями, с одной стороны, и спектром колонизирующей микробной флоры, с другой стороны, требует дальнейшего изучения с целью разработки адекватных медицинских стандартов для лечения респираторные инфекции у пациентов в разных странах.
Человеческое тело является переносчиком различных видов бактерий, которые вместе называются микробиотой [51]. Обычно эти бактерии, которые называются комменсальными штаммами, живут во взаимовыгодном симбиозе с хозяином и обеспечивают множество полезных функций для хозяина, такие как защита организма хозяина посредством конкуренции с патогенными бактериями. Обычно небольшое количество болезнетворных бактерий, в том числе S. pneumoniae , S. aureus , H.influenzae , S. pyogenes , Moraxella catarrhalis и MRSA присутствуют в микробиоте верхних дыхательных путей человека без серьезных последствий для организма [52]. Сдвиг микробиоты в сторону увеличения патогенных штаммов может происходить при вирусных респираторных инфекциях из-за подавления факторов антибактериальной защиты. В результате вторичные бактериальные инфекции дыхательных путей, спровоцированные вирусной инфекцией, чаще всего вызываются резидентными патогенными бактериями, а не внешней инфекцией [53, 54].
На сегодняшний день известно множество факторов, способствующих бактериальной колонизации в ходе вирусных инфекций:
Действие большинства из этих факторов зависит не только от природы вирусного патогена, но и от типа колонизирующих бактерий. . Например, известно, что S. aureus может усиливать репродукцию вируса в результате подавления передачи сигнала IFN типа I, ингибируя димеризацию STAT-1 – STAT-2 [68]. При течении RSV-инфекции у детей степень тяжести заболевания можно определить по распространенности S.pneumoniae и H. influenzae в микробиоте до начала вирусного заболевания [69].
Тем не менее, результаты экспериментов на животных и клинических наблюдений показывают, что колонизация дыхательных путей патогенными бактериальными штаммами чаще всего вызывается вирусными инфекциями. Первичное инфицирование мышей сублетальной дозой бактерий с последующим заражением сублетальной дозой вируса гриппа не приводило к вторичной бактериальной пневмонии, тогда как обратная последовательность инфекций вызывала пневмонию с летальным исходом [70–72].В случае вирусной инфекции бактериальное осложнение чаще всего возникало на 4-й день у животных после вирусной инфекции или на 7-й день у человека после клинического проявления вирусной инфекции [42, 73]. В этом случае, независимо от типа вирусного патогена, ответ IFN типа I играет основную роль, фокусируя действие системы врожденного иммунитета на борьбу с вирусной инфекцией, но в то же время снижая активность факторов антибактериальной защиты, таких как как фагоцитоз или производство антибактериальных пептидов.
Роль IFN-ответа в патогенезе вторичных бактериальных инфекций
Несмотря на различия в структурной и генетической организации вирусов разных семейств, они имеют общее свойство — все они являются внутриклеточными патогенами, вызывающими IFN-ответ типа I. Система врожденного иммунитета распознает вирусную инфекцию с помощью Toll-подобных рецепторов, расположенных в клеточной мембране или цитоплазматических рецепторов распознавания образов RIG-1 и MDA5 (PRR).Эти рецепторы обнаруживают компоненты патогенов, такие как двухцепочечная РНК (дцРНК) или липосахариды (ЛПС), которые нетипичны для нормальных клеток, но присутствуют в очаге инфекции. Распознавание вирусной инфекции приводит к индукции цитокинового ответа, прежде всего ИФН I, II и III типов. Система врожденного противовирусного иммунитета подробно описана в обзорах [74, 75]. Защитные эффекты IFN обусловлены их способностью индуцировать синтез противовирусных белков в инфицированных и окружающих клетках, а также регулированием активации и миграции клеток врожденного иммунитета, которые определяют развитие специфических B- и T- клеточный иммунный ответ [76–78].
С другой стороны, большая часть недавних экспериментальных данных показывает, что влияние IFN-ответа на течение ОРВИ может быть пагубным. В случае прогрессирующего развития инфекции непрерывная и избыточная продукция IFN может привести к развитию воспаления из-за гиперпродукции хемокинов, таких как CCL2 и CXCL10, и инфильтрации альвеол провоспалительными моноцитами / макрофагами и плазмацитоидами. дендритные клетки. В этом случае попадание вирусных и бактериальных лигандов Toll-подобных рецепторов, таких как LPS или dsRNA, в зону воспаления может привести к усиленной продукции провоспалительных цитокинов этими клетками с возможностью развития так называемого цитокинового шторма [79]. .Тогда неконтролируемая продукция провоспалительных цитокинов и чрезмерная инфильтрация тканей легких клетками врожденного иммунитета могут стать ведущей причиной повреждения легких [80, 81].
Экспрессия проапоптотического лиганда TRIAL, индуцированная IFN типа I, также приводит к массивному апоптозу эпителиальных клеток, которые вносят вклад в развитие ARDS [82].
Важным фактором риска развития неконтролируемого воспаления является генетическая предрасположенность организма к регуляции ответа IFN.Например, мыши DBA, которые продуцируют высокие уровни IFN типа I в ответ на инфекцию гриппа, демонстрируют высокую смертность при инфицировании дозами, безопасными для мышей C57BL / 6 с умеренным продуцированием INF [83, 84]. Люди с синдромом Дауна имеют повышенную чувствительность к респираторным инфекциям и высокую вероятность серьезных осложнений, связанных с генетически обусловленной гиперпродукцией IFN α / γ в ответ на вирусную инфекцию [85].
Помимо стимуляции цитокинового шторма, IFN типа I могут участвовать в патогенезе вторичной бактериальной инфекции [86, 87].Развитие IFN-ответа в ходе вирусной инфекции приводит к снижению как миграции, так и фагоцитарной функции нейтрофилов и макрофагов за счет проапоптотических механизмов или за счет эпигенетической регуляции их функций [61, 88, 89].
IFN типа I также способны подавлять антибактериальную защиту, подавляя продукцию IL-17 Т-клетками [63, 90]. Отсутствие ответа на IL-17 приводит к снижению продукции антибактериальных пептидов, таких как липокалин 2 и BPIFA1, что, в свою очередь, приводит к увеличению бактериального роста в очаге вирусной инфекции [87].
Тот факт, что генетически модифицированные мыши с дефицитом рецепторов IFN типа I (IFNAR) были более устойчивы к развитию ARDS, бактериальной пневмонии или сепсиса по сравнению с мышами с нормальной передачей сигналов IFN, доказывает отрицательный эффект сверхэкспрессии IFN [61, 62, 84, 91, 92]. Использование индуктора поли (I: C) IFN перед заражением мышей пневмококком привело к 100-кратному увеличению колонизации легких введенными бактериями [64].
Следовательно, развитие тяжелых осложнений после ОРВИ может зависеть не только от вирулентности самого вируса или от состава респираторной микробиоты во время вирусной инфекции, но и от способности организма регулировать выраженность реакций врожденного иммунитета, особенно ответа на ИФН.
Роль противовирусной вакцинации и противовирусной терапии в профилактике вторичных бактериальных осложнений
В настоящее время существует множество доказательств того, что противовирусная вакцинация может снизить риск бактериальных осложнений после ОРВИ. Было показано, что иммунизация инактивированной противогриппозной вакциной значительно снижает тяжесть бактериальной суперинфекции у мышей, инфицированных гриппом [93]. В другом исследовании было показано, что иммунизация мышей инактивированной или живой вакциной против гриппа может в равной степени снизить летальность вирусной и последующей бактериальной инфекции, но в то же время она не может ограничить рост S.pyogenes в легких. В этом случае было показано, что вакцинация против гриппа, приводящая к снижению вирусной нагрузки, приводит к снижению провоспалительных цитокинов и индукции IFNγ в легких во время бактериальной суперинфекции [94]. К сожалению, информации о влиянии вакцинации против гриппа на вторичные бактериальные осложнения мало. Это объясняется сложностью подобных исследований, поскольку потребовалась бы параллельная оценка противовирусного и антибактериального иммунитета к большому количеству потенциальных патогенов.Однако в ограниченном исследовании, проведенном в США среди военнослужащих, вакцина против гриппа снижает уровень заболеваемости, вызываемой S. pyogenes [95]. Аналогичным образом вакцинация детей живой вакциной, адаптированной к холоду, показала снижение заболеваемости средним отитом [96].
Таким образом, вакцинация против респираторных вирусов может помочь предотвратить вторичные бактериальные осложнения из-за различных механизмов неспецифической защиты путем модуляции врожденного иммунитета.Разумно предположить, что снижение репродукции вируса из-за эффективной вакцинации может привести к снижению противовирусного ответа IFN и, как следствие, ограничению негативного действия IFN на эффекторы антибактериальной защиты. Кроме того, снижение концентрации вируса может помочь сохранить респираторный эпителий и уменьшить адгезию бактериальных клеток [56].
Действие противовирусных препаратов, таких как ингибиторы NA, на предотвращение вторичных бактериальных инфекций также может быть связано со снижением ответа IFN из-за ингибирования репликации вируса.Исследования на животных моделях показали, что ингибиторы NA могут снижать восприимчивость животных, инфицированных гриппом, к вторичной бактериальной пневмонии [97]. Клинические испытания у взрослых и детей показали, что прием ингибиторов НА (занамивир и осельтамивир) приводит к снижению частоты бронхита и, как следствие, к меньшему количеству назначений антибиотиков [98-101].
Открытие антибиотиков и разработка противогриппозных и бактериальных вакцин значительно снизили шансы повторения катастрофических пандемий, таких как испанский грипп 1918 года [102].Однако грипп и другие респираторные вирусы остаются одной из основных причин бактериальных осложнений и ВП. С другой стороны, растущая устойчивость бактериальных патогенов к современным антибиотикам из-за их широкого использования становится все более тревожной.
К сожалению, в настоящее время практически отсутствуют вакцины или противовирусные препараты для профилактики и лечения респираторных вирусов, кроме гриппа. Несмотря на прогресс, достигнутый в разработке пневмококковых и других антибактериальных вакцин и обширные усилия по разработке вакцин против респираторных вирусов, маловероятно, что в обозримом будущем будет доступна эффективная комплексная система вакцинации против распространенных вирусных и бактериальных респираторных патогенов.Создание специфических противовирусных препаратов против различных групп респираторных вирусов, эффективных на поздней стадии инфекции, имеет низкую вероятность успеха. Поэтому существует острая необходимость в разработке патогенетических препаратов, снижающих реакции врожденного иммунитета, ослабляющие факторы антибактериальной защиты при вирусной инфекции. Одним из возможных подходов может быть поиск лекарств, предотвращающих чрезмерную продукцию IFN на пике вирусной инфекции.Подавление избыточной передачи сигналов IFN может стать важным терапевтическим подходом к предотвращению как эффектов цитокинового шторма, так и развития вторичных бактериальных осложнений в областях, прилегающих к дыхательным путям [79, 82, 103-105].
Эта работа была поддержана грантом RSF-FWF № 18-45-05002 (подход VLP к борьбе с бактериальными инфекциями после гриппа).
Автор не преследует коммерческих или финансовых интересов.
Егоров А. Проблема бактериальных осложнений после респираторных вирусных инфекций.МИР Ж, 2018; 5 (1), 12-21, DOI: 10.18527 / 2500-2236-2018-5-1-12-21.
© Егоров, 2018. Это статья в открытом доступе, распространяемая в соответствии с условиями Международной общественной лицензии Creative Commons AttributionNonCommercial-ShareAlike 4.0 (CC-BY-NC-SA), которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе, при условии, что материал не используется в коммерческих целях при условии ссылки на автора и источник.
1. Инициатива «Битва с респираторными вирусами» (BRaVe).Всемирная организация здоровья. Доступно: http://www.who.int/influenza/patient_care/clinical/brave/en/#; http://www.who.int/mediacentre/factsheets/fs211/en/
2. Kilbourne ED. Пандемии гриппа ХХ века. Emerg Infect Dis 2006; 12 (1), 9-14. DOI: 10.3201 / eid1201.051254.
3. Cheng VC, To KK, Tse H, Hung IF, Yuen KY. Через два года после пандемии гриппа A / 2009 / h2N1: что мы узнали? Clin Microbiol Rev 2012; 25 (2), 223-63. DOI: 10.1128 / CMR.05012-11.
4. Оксфорд Дж. С., Сефтон А., Джексон Р., Иннес В., Дэниэлс Р. С., Джонсон Н. П.. Первая мировая война, возможно, привела к появлению «испанского» гриппа. Lancet Infect Dis 2002; 2 (2), 111-4. PubMed PMID: 11
2.5. Брем В.В., Боллинг Г.Е., Каспер Э.Дж. Пандемия гриппа и вторичная пневмония в Кэмп-Фремонт, Калифорния. J Am Med Assoc, 1918; 71, 2138-44. DOI: 10.1001 / jama.1918.26020520007010b.
6. Таубенбергер Дж. К., Балтимор Д., Доэрти П. К., Маркель Х., Моренс Д. М., Вебстер Р. Г. и др.Реконструкция вируса гриппа 1918 года: неожиданные награды из прошлого. MBio 2012; 3 (5). DOI: 10.1128 / mBio.00201-12.
7. Моррис Д.Е., Клири Д.В., Кларк СК. Вторичные бактериальные инфекции, связанные с пандемиями гриппа. Front Microbiol 2017; 8, 1041. DOI: 10.3389 / fmicb.2017.01041.
8. Morens DM, Taubenberger JK, Fauci AS. Преобладающая роль бактериальной пневмонии как причины смерти при пандемическом гриппе: последствия для готовности к пандемическому гриппу.J Infect Dis 2008; 198 (7), 962-70. DOI: 10,1086 / 591708.
9. Чиен Ю.В., Клугман К.П., Моренс Д.М. Бактериальные патогены и смерть во время пандемии гриппа 1918 г. N Engl J Med 2009; 361 (26), 2582-3. DOI: 10.1056 / NEJMc0908216.
10. Brundage JF, Shanks GD. Смертность от бактериальной пневмонии во время пандемии гриппа 1918-19 гг. Emerg Infect Dis 2008; 14 (8), 1193-9. DOI: 10.3201 / eid1408.071313.
11. Вин М.К., Чен М.И., Баркхэм Т., Лин С, Тан А., Лин Р. и др.Бремя заболевания гриппом среди взрослых по подтипам после начальной эпидемии пандемии h2N1 в Сингапуре. Другие респирные вирусы гриппа 2011; 5 (6), е563-7. DOI: 10.1111 / j.1750-2659.2011.00282.x.
12. Поттер CW. История гриппа. J Appl Microbiol 2001; 91 (4), 572-9. PubMed PMID: 11576290.
13. Вибуд К., Симонсен Л., Фуэнтес Р., Флорес Дж., Миллер М.А., Човелл Г. Глобальное влияние пандемии гриппа 1957-1959 гг. На смертность. J Infect Dis 2016; 213 (5), 738-45.DOI: 10.1093 / infdis / jiv534.
14. Eickhoff TC, Sherman IL, Serfling RE. Наблюдения за повышенной смертностью, связанной с эпидемическим гриппом. JAMA 1961; 176, 776-82. PubMed PMID: 13726091.
15. Хиллеман MR. Реалии и загадки вирусного гриппа человека: патогенез, эпидемиология и борьба. Вакцина 2002; 20 (25-26), 3068-87. PubMed PMID: 12163258.
16. Херс Дж. Ф., Мазурел Н., Малдер Дж. Бактериология и гистопатология дыхательных путей и легких при фатальном азиатском гриппе.Lancet 1958; 2 (7057), 1141-3. PubMed PMID: 13612141.
17. Гилл Дж. Р., Шенг З. М., Эли С.Ф., Гине Д.Г., Бисли М.Б., Су Дж. И др. Легочные патологические находки фатальных вирусных инфекций пандемического гриппа A / h2N1 2009 г. Arch Pathol Lab Med 2010; 134 (2), 235-43. DOI: 10.1043 / 1543-2165-134.2.235.
18. Петерсдорф Р.Г., Фуско Дж. Дж., Хартер Д.Х., Олбринк В.С. Легочные инфекции, осложняющие азиатский грипп. AMA Arch Intern Med 1959; 103 (2), 262-72. PubMed PMID: 13616762.
19.Робертсон Л., Кейли Дж. П., Мур Дж. Важность золотистого стафилококка при пневмонии во время эпидемии гриппа 1957 г. A. Lancet 1958; 2 (7040), 233-6. PubMed PMID: 13564806.
20. Михаэлис М., Дорр Х.В., Цинатл Дж. Младший. Новый вирус гриппа А свиного происхождения у людей: еще одна пандемия, стучащаяся в дверь. Med Microbiol Immunol 2009; 198 (3), 175-83. DOI: 10.1007 / s00430-009-0118-5.
21. Климов А., Симонсен Л., Фукуда К., Кокс Н. Эпиднадзор и влияние гриппа в США.Vaccine 1999; 17 Дополнение 1, S42-6. PubMed PMID: 10471179.
22. Тиллетт Х.Э., Смит Дж. В., Гуч CD. Чрезмерное количество смертей от гриппа в Англии и Уэльсе: возраст на момент смерти и подтвержденная причина. Int J Epidemiol 1983; 12 (3), 344-52. PubMed PMID: 6629624.
23. Линдсей М.И., мл., Херрманн Е.К., мл., Морроу Г.В., мл., Браун А.Л., мл. Гонконгский грипп: клинические, микробиологические и патологические особенности в 127 случаях. JAMA 1970; 214 (10), 1825-32. PubMed PMID: 5537337.
24.Ван Т.Т., Палезе П. Раскрытие тайны вируса свиного гриппа. Cell 2009; 137 (6), 983-5. DOI: 10.1016 / j.cell.2009.05.032.
25. Chertow DS, Memoli MJ. Бактериальная коинфекция при гриппе: обзор большого количества раундов. JAMA 2013; 309 (3), 275-82. DOI: 10.1001 / jama.2012.194139.
26. Ли Э. Х., Ву С., Ли ЕС, Стаут А., Хэнсон Х., Кук Х. А. и др. Смертельные случаи, связанные с вирусом гриппа A 2009 h2N1 в Нью-Йорке. Clin Infect Dis 2010; 50 (11), 1498-504.DOI: 10,1086 / 652446.
27. Лукас С. Прогностические клинико-патологические особенности, полученные на основе систематического вскрытия трупов пациентов, умерших от инфекции гриппа A / h2N1 во время пандемии 2009-10 в Великобритании. Оценка медицинских технологий 2010; 14 (55), 83-114. DOI: 10.3310 / hta14550-02.
28. Паласиос Г., Хорниг М., Цистерна Д., Савджи Н., Буссетти А.В., Капур В. и др. Коинфекция Streptococcus pneumoniae коррелирует с тяжестью пандемического гриппа h2N1. PLoS One 2009; 4 (12), е8540.DOI: 10.1371 / journal.pone.0008540.
29. Рэндольф А.Г., Вон Ф., Салливан Р., Рубинсон Л., Томпсон Б.Т., Юн Г. и др. Дети в критическом состоянии во время пандемии гриппа 2009-2010 гг. В США. Педиатрия 2011; 128 (6), е1450-8. DOI: 10.1542 / peds.2011-0774.
30. Живич А. Борьба с бактериальной устойчивостью: подходы, проблемы и возможности в поисках новых антибиотиков. Часть 1. Антибиотики, применяемые в клинической практике: механизмы действия и развитие резистентности бактерий.МИР Ж 2017; 4 (1), 31-51. DOI: 10.18527 / 2500-2236-2017-4-1-31-51.
31. Хасволд Дж., Сджодинг М., Поль К., Кук С., Хизи Р.С. Роль метапневмовируса человека у взрослого пациента в критическом состоянии. J Crit Care 2016; 31 (1), 233-7. DOI: 10.1016 / j.jcrc.2015.09.035.
32. Квон Ю.С., Пак С.Х., Ким М.А., Ким Х.Дж., Пак Дж.С., Ли М.И. и др. Риск смерти, связанный с респираторно-синцитиальным вирусом и инфекцией гриппа у взрослых. BMC Infect Dis 2017; 17 (1), 785. DOI: 10.1186 / s12879-017-2897-4.
33. Prasso JE, Deng JC. Поствирусные осложнения: бактериальная пневмония. Clin Chest Med 2017; 38 (1), 127-38. DOI: 10.1016 / j.ccm.2016.11.006.
34. Метерский М.Л., Мастертон Р.Г., Лоде Х., Файл TM, мл., Бабинчак Т. Эпидемиология, микробиология и рекомендации по лечению бактериальной пневмонии, осложняющей грипп. Int J Infect Dis 2012; 16 (5), е321-31. DOI: 10.1016 / j.ijid.2012.01.003.
35. Mulcahy ME, McLoughlin RM. Золотистый стафилококк и вирус гриппа А: партнеры в коинфекции.MBio 2016; 7 (6). DOI: 10.1128 / mBio.02068-16.
36. Сафеян Ф., Нахаи М.Р., Сейфи С.Дж., Кафил Х.С., Садеги Дж. Количественное определение Staphylococcus aureus, Streptococcus pneumoniae и Haemophilus influenzae у пациентов с новым вирусом гриппа A (h2N1) / 2009 и гриппом A / 2010. GMS Hyg Infect Control 2015; 10, Doc06. DOI: 10.3205 / dgkh000249.
37. Дженнингс Л.С., Андерсон Т.П., Бейнон К.А., Чуа А., Лэйнг Р.Т., Верно А.М. и др. Заболеваемость и характеристики вирусной внебольничной пневмонии у взрослых.Thorax 2008; 63 (1), 42-8. DOI: 10.1136 / thx.2006.075077.
38. Лидерот К., Ахл М., Озенци В. Вторичные бактериальные инфекции у пациентов с сезонным гриппом A и пандемией h2N1. Biomed Res Int 2013; 2013, 376219. DOI: 10.1155 / 2013/376219.
39. Чонмайтри Т., Дженнингс К., Головко Г., Ханипов К., Пименова М., Патель Дж. А. и др. Микробиота носоглотки у младенцев и изменения во время вирусной инфекции верхних дыхательных путей и острого среднего отита. PLoS One 2017; 12 (7), e0180630.DOI: 10.1371 / journal.pone.0180630.
40. Jacobs JH, Viboud C, Tchetgen ET, Schwartz J, Steiner C, Simonsen L, et al. Связь менингококковой инфекции с гриппом в США, 1989-2009 гг. PLoS One 2014; 9 (9), e107486. DOI: 10.1371 / journal.pone.0107486.
41. Брили Дж. К., Чаппелл К. Дж., Гэлбрейт С., Фантино Е., Гайдон Дж., Тозер С. и др. Колонизация носоглотки Streptococcus pneumoniae связана с усилением тяжести респираторно-синцитиальной вирусной инфекции у детей раннего возраста.Респирология 2018; 23 (2), 220-7. DOI: 10.1111 / resp.13179.
42. Hendaus MA, Jomha FA, Alhammadi AH. Вторичная бактериальная инфекция, индуцированная вирусами: краткий обзор. Ther Clin Risk Manag 2015; 11, 1265-71. DOI: 10.2147 / TCRM.S87789.
43. Луи Дж. К., Рой-Берман А., Гуардиа-Лабар Л., Бостон Е. Дж., Кианг Д., Падилла Т. и др. Риновирус, связанный с тяжелыми инфекциями нижних дыхательных путей у детей. Pediatr Infect Dis J 2009; 28 (4), 337-9. DOI: 10.1097 / INF.0b013e31818ffc1b.
44. Маллиа П., Футитт Дж., Сотеро Р., Джепсон А., Контоли М., Трухильо-Торральбо МБ и др. Риновирусная инфекция вызывает деградацию антимикробных пептидов и вторичную бактериальную инфекцию при хронической обструктивной болезни легких. Am J Respir Crit Care Med 2012; 186 (11), 1117-24. DOI: 10.1164 / rccm.201205-0806OC.
45. Kloepfer KM, Lee WM, Pappas TE, Kang TJ, Vrtis RF, Evans MD, et al. Обнаружение патогенных бактерий при риновирусной инфекции связано с усилением респираторных симптомов и обострениями астмы.J Allergy Clin Immunol 2014; 133 (5), 1301-7, 7 е1-3. DOI: 10.1016 / j.jaci.2014.02.030.
46. Корппи М., Лейнонен М., Макела PH, Лауниала К. Участие бактерий в вирусной инфекции парагриппа у детей. Scand J Infect Dis 1990; 22 (3), 307-12. PubMed PMID: 2164707.
47. Verkaik NJ, Nguyen DT, de Vogel CP, Moll HA, Verbrugh HA, Jaddoe VW, et al. Воздействие Streptococcus pneumoniae связано с сероконверсией метапневмовируса человека и повышенной восприимчивостью к инфекции HMPV in vitro.Clin Microbiol Infect 2011; 17 (12), 1840-4. DOI: 10.1111 / j.1469-0691.2011.03480.x.
48. Self WH, Williams DJ, Zhu Y, Ampofo K, Pavia AT, Chappell JD, et al. Выявление респираторных вирусов у детей и взрослых: сравнение бессимптомных контрольных групп и пациентов с внебольничной пневмонией. J Infect Dis 2016; 213 (4), 584-91. DOI: 10.1093 / infdis / jiv323.
49. Кацурада Н., Сузуки М., Аошима М., Яэгаши М., Ишифудзи Т., Асо Н. и др. Влияние вирусных инфекций на смертность от пневмонии у взрослых сложное: проспективное многоцентровое обсервационное исследование.BMC Infect Dis 2017; 17 (1), 755. DOI: 10.1186 / s12879-017-2858-у.
50. Юнг Х.С., Кан Б.Дж., Ра С.В., Со К.В., Джегал Й., Джун Дж. Б. и др. Выявление возбудителей бактериальной пневмонии у пациентов с респираторной вирусной инфекцией. Tuberc Respir Dis (Сеул) 2017; 80 (4), 358-67. DOI: 10.4046 / trd.2017.0044.
51. Хупер Л.В., Литтман Д.Р., Макферсон А.Дж. Взаимодействие между микробиотой и иммунной системой. Наука 2012; 336 (6086), 1268-73. DOI: 10.1126 / наука.1223490.
52. Чарлсон Е.С., Биттингер К., Хаас А.Р., Фицджеральд А.С., Франк И., Ядав А. и др. Топографическая преемственность бактериальных популяций в дыхательных путях здорового человека. Am J Respir Crit Care Med 2011; 184 (8), 957-63. DOI: 10.1164 / rccm.201104-0655OC.
53. Богерт Д., Де Гроот Р., Херманс П.В. Колонизация Streptococcus pneumoniae: ключ к пневмококковой инфекции. Lancet Infect Dis 2004; 4 (3), 144-54. DOI: 10.1016 / S1473-3099 (04) 00938-7.
54.Bosch AA, Biesbroek G, Trzcinski K, Sanders EA, Bogaert D. Взаимодействие вирусов и бактерий в верхних дыхательных путях. PLoS Pathog 2013; 9 (1), e1003057. DOI: 10.1371 / journal.ppat.1003057.
55. Ян Х, Стойкерс Л., Фориер К., Сюн Р., Брекманс К., Ван Рит К. и др. Благоприятная роль нейраминидазы в проникновении вируса гриппа через дыхательную слизь. PLoS One 2014; 9 (10), e110026. DOI: 10.1371 / journal.pone.0110026.
56. Avadhanula V, Rodriguez CA, Devincenzo JP, Wang Y, Webby RJ, Ulett GC, et al.Респираторные вирусы усиливают адгезию бактериальных патогенов к респираторному эпителию в зависимости от вида вируса и типа клеток. J Virol 2006; 80 (4), 1629-36. DOI: 10.1128 / JVI.80.4.1629-1636.2006.
57. Ли Н, Рен А., Ван Х, Фан Х, Чжао И, Гао Г.Ф. и др. Вирусная нейраминидаза гриппа вызывает бактериальную коинфекцию через TGF-бета-опосредованную экспрессию рецепторов клетки-хозяина. Proc Natl Acad Sci U S A 2015; 112 (1), 238-43. DOI: 10.1073 / pnas.1414422112.
58.Карсон Дж. Л., Кольер А. М., Ху СС. Приобретенные пороки ресничек носового эпителия у детей с острыми вирусными инфекциями верхних дыхательных путей. N Engl J Med 1985; 312 (8), 463-8. DOI: 10.1056 / NEJM198502213120802.
59. Питтет Л.А., Холл-Стодли Л., Рутковски М.Р., Хармсен АГ. Инфекция вируса гриппа снижает мукоцилиарную скорость в трахее и клиренс Streptococcus pneumoniae. Am J Respir Cell Mol Biol 2010; 42 (4), 450-60. DOI: 10.1165 / rcmb.2007-0417OC.
60. Sun K, Metzger DW.Подавление антибактериальной защиты легких интерфероном-гамма во время выздоровления от инфекции гриппа. Nat Med 2008; 14 (5), 558-64. DOI: 10,1038 / нм1765.
61. Shahangian A, Chow EK, Tian X, Kang JR, Ghaffari A, Liu SY, et al. IFN типа I опосредуют развитие бактериальной пневмонии после гриппа у мышей. J Clin Invest 2009; 119 (7), 1910-20. DOI: 10.1172 / JCI35412.
62. Nakamura S, Davis KM, Weiser JN. Синергетическая стимуляция интерферонов типа I во время коинфекции вирусом гриппа способствует колонизации Streptococcus pneumoniae у мышей.J Clin Invest 2011; 121 (9), 3657-65. DOI: 10,1172 / JCI57762.
63. Кудва А., Шеллер Э.В., Робинсон К.М., Кроу С.Р., Чой С.М., Слайт С.Р. и др. Грипп A подавляет Th27-опосредованную защиту хозяина от бактериальной пневмонии у мышей. J Immunol 2011; 186 (3), 1666-74. DOI: 10.4049 / jimmunol.1002194.
64. Тиан X, Сюй Ф., Лунг В.Й., Мейерсон С., Гаффари А.А., Ченг Дж. И др. Поли I: C повышает восприимчивость к вторичным легочным инфекциям, вызываемым грамположительными бактериями. PLoS One 2012; 7 (9), e41879.DOI: 10.1371 / journal.pone.0041879.
65. Astry CL, Jakab GJ. Иммунные комплексы, индуцированные вирусом гриппа, подавляют фагоцитоз альвеолярных макрофагов. J Virol 1984; 50 (2), 287-92. PubMed PMID: 6708169.
66. Franke-Ullmann G, Pfortner C, Walter P, Steinmuller C., Lohmann-Matthes ML, Kobzik L, et al. Изменение функции легочных макрофагов инфекцией респираторно-синцитиального вируса in vitro. J Immunol 1995; 154 (1), 268-80. PubMed PMID: 7995946.
67.Jakab GJ. Иммунное нарушение фагоцитоза альвеолярных макрофагов при пневмонии, вызванной вирусом гриппа. Am Rev Respir Dis 1982; 126 (5), 778-82. DOI: 10.1164 / arrd.1982.126.5.778.
68. Warnking K, Klemm C, Loffler B, Niemann S, van Kruchten A, Peters G, et al. Суперинфекция Staphylococcus aureus подавляет индуцированную вирусом гриппа передачу сигналов IFN типа I за счет нарушения димеризации STAT1-STAT2. Cell Microbiol 2015; 17 (3), 303-17. DOI: 10,1111 / cmi.12375.
69.de Steenhuijsen Piters WA, Heinonen S, Hasrat R, Bunsow E, Smith B, Suarez-Arrabal MC и др. Микробиота носоглотки, транскриптом хозяина и тяжесть заболевания у детей с респираторно-синцитиальной вирусной инфекцией. Am J Respir Crit Care Med 2016; 194 (9), 1104-15. DOI: 10.1164 / rccm.201602-0220OC.
70. Jia L, Xie J, Zhao J, Cao D, Liang Y, Hou X и др. Механизмы сопутствующих бактериальных инфекций, связанных с тяжелой смертностью, после инфицирования вирусом гриппа. Front Cell Infect Microbiol 2017; 7, 338.DOI: 10.3389 / fcimb.2017.00338.
71. Джеймисон А.М., Пашман Л., Ю. С., Гамрад П., Гомер Р. Дж., Деккер Т. и др. Роль защиты тканей при летальной респираторной вирусно-бактериальной коинфекции. Наука 2013; 340 (6137), 1230-4. DOI: 10.1126 / science.1233632.
72. Ли Л.Н., Диас П., Хан Д., Юн С., Ши А., Захаров В. и др. Мышиная модель летального синергизма между вирусом гриппа и Haemophilus influenzae. Am J Pathol 2010; 176 (2), 800-11. DOI: 10.2353 / ajpath.2010.0
.
73. McCullers JA. Совместное патогенез вирусов гриппа с бактериями в легких. Nat Rev Microbiol 2014; 12 (4), 252-62. DOI: 10,1038 / nrmicro3231.
74. Трипати С., Гарсия-Састре А. Противовирусный врожденный иммунитет через призму системной биологии. Virus Res 2016; 218, 10-7. DOI: 10.1016 / j.virusres.2015.11.024.
75. Бреннан К., Боуи АГ. Активация вирусами рецепторов распознавания образов хозяина. Curr Opin Microbiol 2010; 13 (4), 503-7.DOI: 10.1016 / j.mib.2010.05.007.
76. Чен X, Лю С., Горая М.Ю., Мааруф М., Хуанг С., Чен Дж.Л. Иммунный ответ хозяина на инфекцию вирусом гриппа А. Фронт Иммунол 2018; 9, 320. DOI: 10.3389 / fimmu.2018.00320.
77. Шим Дж. М., Ким Дж., Тенсон Т., Мин Дж. Я., Кайнов Д.Е. Инфекция вирусом гриппа, ответ интерферона, ответный вирусный ответ и апоптоз. Вирусы 2017; 9 (8), 223. DOI: 10.3390 / v9080223.
78. Андреакос Э., Салагянни М, Галани ИП, Кольцида О.Интерферон-лямбды: передовые стражи иммунитета и гомеостаза в дыхательных путях. Фронт Иммунол 2017; 8, 1232. DOI: 10.3389 / fimmu.2017.01232.
79. Горицка М., Дюрант Л.Р., Перейра С., Салек-Ардакани С., Опеншоу П.Дж., Йоханссон С. Передача сигналов рецептора альфа / бета-интерферона усиливает раннюю продукцию провоспалительных цитокинов в легких во время респираторно-синцитиальной вирусной инфекции. J Virol 2014; 88 (11), 6128-36. DOI: 10.1128 / JVI.00333-14.
80. Доэрти П.С., Тернер С.Дж., Уэбби Р.Г., Томас П.Г.Грипп и вызов иммунологии. Нат Иммунол 2006; 7 (5), 449-55. DOI: 10,1038 / NI1343.
81. Пейрис Дж. С., Ю. В. К., Люнг К. В., Чунг С. Ю., Нг В. Ф., Николлс Дж. М. и др. Повторное появление смертельного человеческого гриппа A подтипа H5N1. Lancet 2004; 363 (9409), 617-9. DOI: 10.1016 / S0140-6736 (04) 15595-5.
82. Макрис С., Полсен М., Йоханссон С. Интерфероны типа I как регуляторы воспаления легких. Фронт Иммунол 2017; 8, 259. DOI: 10.3389 / fimmu.2017.00259.
83.Шривастава Б., Блажеевска П., Хессманн М., Брудер Д., Гефферс Р., Мауэль С. и др. Генетический фон хозяина сильно влияет на реакцию на вирусную инфекцию гриппа. PLoS One 2009; 4 (3), е4857. DOI: 10.1371 / journal.pone.0004857.
84. Дэвидсон С., Кротта С., МакКейб TM, Вак А. Патогенный потенциал интерферона алфавита при острой гриппозной инфекции. Nat Commun 2014; 5, 3864. DOI: 10.1038 / ncomms4864.
85. Broers CJ, Gemke RJ, Weijerman ME, van der Sluijs KF, van Furth AM.Повышенная выработка провоспалительных цитокинов у детей с синдромом Дауна при стимуляции живым вирусом гриппа А. J Clin Immunol 2012; 32 (2), 323-9. DOI: 10.1007 / s10875-011-9625-4.
86. Рында-Эппл А., Робинсон К.М., Алкорн Дж. Ф. Грипп и бактериальная суперинфекция: освещение иммунологических механизмов заболевания. Infect Immun 2015; 83 (10), 3764-70. DOI: 10.1128 / IAI.00298-15.
87. Ли Б., Робинсон К.М., МакХью К.Дж., Шеллер Е.В., Мандалапу С., Чен С. и др.Интерферон I типа, индуцированный гриппом, увеличивает восприимчивость к грамотрицательной и грамположительной бактериальной пневмонии у мышей. Am J Physiol Lung Cell Mol Physiol 2015; 309 (2), Л158-67. DOI: 10.1152 / ajplung.00338.2014.
88. Шлихе С., Флинн Е.К., Вилагос Б., Ричсон Ю., Сваминантан С., Босняк Б. и др. Метилтрансфераза Setdb2 опосредует вирус-индуцированную чувствительность к бактериальной суперинфекции. Нат Иммунол 2015; 16 (1), 67-74. DOI: 10.1038 / NI.3046.
89. Кроец Д. Н., Аллен Р. М., Шаллер М. А., Кавалларо К., Ито Т., Кункель С. Л..Эпигенетическая регуляция макрофагов, индуцированная интерфероном I типа, подавляет врожденный и адаптивный иммунитет при острой респираторной вирусной инфекции. PLoS Pathog 2015; 11 (12), e1005338. DOI: 10.1371 / journal.ppat.1005338.
90. Цао Дж., Ван Д., Сюй Ф., Гун Й., Ван Х., Сун З. и др. Активация передачи сигналов IL-27 способствует развитию постгриппозной пневмококковой пневмонии. EMBO Mol Med 2014; 6 (1), 120-40. DOI: 10.1002 / emmm.201302890.
91. Ли В., Мольтедо Б., Моран TM. Индукция интерферона I типа во время инфицирования вирусом гриппа увеличивает восприимчивость к вторичной инфекции Streptococcus pneumoniae за счет отрицательной регуляции гаммадельта-Т-клеток.J Virol 2012; 86 (22), 12304-12. DOI: 10.1128 / JVI.01269-12.
92. Dejager L, Vandevyver S, Ballegeer M, Van Wonterghem E, An LL, Riggs J, et al. Фармакологическое подавление передачи сигналов интерферона типа I защищает мышей от летального сепсиса. J Infect Dis 2014; 209 (6), 960-70. DOI: 10,1093 / infdis / jit600.
93. Хубер В.К., Пелтола В., Айверсон А.Р., Маккаллерс Дж.А. Вклад индуцированного вакциной иммунитета к HA или NA компоненту вирусов гриппа ограничивает вторичные бактериальные осложнения.J Virol 2010; 84 (8), 4105-8. DOI: 10.1128 / JVI.02621-09.
94. Chaussee MS, Sandbulte HR, Schuneman MJ, Depaula FP, Addengast LA, Schlenker EH, et al. Инактивированные и живые, аттенуированные вакцины против гриппа защищают мышей от гриппа: суперинфекций Streptococcus pyogenes. Вакцина 2011; 29 (21), 3773-81. DOI: 10.1016 / j.vaccine.2011.03.031.
95. Ли С.Е., Эйк А., Блум М.С., Брандейдж Дж.Ф. Иммунизация против гриппа и последующая диагностика стрептококковой болезни группы А среди U.С. Стажеры армии, 2002-2006 гг. Вакцина 2008; 26 (27-28), 3383-6. DOI: 10.1016 / j.vaccine.2008.04.041.
96. Белше РБ, Грубер WC. Профилактика среднего отита у детей с помощью живой аттенуированной вакцины против гриппа, вводимой интраназально. Pediatr Infect Dis J 2000; 19 (5 доп.), С66-71. PubMed PMID: 10821474.
97. McCullers JA. Влияние противовирусного лечения на исход вторичной бактериальной пневмонии после гриппа. J Infect Dis 2004; 190 (3), 519-26. DOI: 10,1086 / 421525.
98. Hayden FG, Osterhaus AD, Treanor JJ, Fleming DM, Aoki FY, Nicholson KG, et al. Эффективность и безопасность занамивира, ингибитора нейраминидазы, при лечении инфекций, вызванных вирусом гриппа. GG167 Исследовательская группа по гриппу. N Engl J Med 1997; 337 (13), 874-80. DOI: 10.1056 / NEJM199709253371302.
99. Кайзер Л., Кин О.Н., Хаммонд Дж. М., Эллиотт М., Хайден Ф. Г.. Влияние занамивира на использование антибиотиков при респираторных осложнениях после острого гриппа у подростков и взрослых.Arch Intern Med 2000; 160 (21), 3234-40. PubMed PMID: 11088083.
100. Кайзер Л., Уот С., Миллс Т., Махони П., Уорд П., Хайден Ф. Влияние лечения осельтамивиром на связанные с гриппом осложнения со стороны нижних дыхательных путей и госпитализации. Arch Intern Med 2003; 163 (14), 1667-72. DOI: 10.1001 / archinte.163.14.1667.
101. Николсон К.Г., Аоки Ф.Й., Остерхаус А.Д., Троттье С., Каревич О., Мерсье С.Х. и др. Эффективность и безопасность осельтамивира при лечении острого гриппа: рандомизированное контролируемое исследование.Группа исследователей лечения гриппа с ингибиторами нейраминидазы. Lancet 2000; 355 (9218), 1845-50. PubMed PMID: 10866439.
102. Смит AM, Huber VC. Неожиданное влияние вакцин на вторичные бактериальные инфекции после гриппа. Вирусный Иммунол 2018; 31 (2), 159-73. DOI: 10.1089 / vim.2017.0138.
103. Zang N, Xie X, Deng Y, Wu S, Wang L, Peng C и др. Опосредованное ресвератролом уменьшение гамма-интерферона предотвращает воспаление дыхательных путей и гиперчувствительность дыхательных путей у мышей с иммунодефицитом, инфицированных респираторно-синцитиальным вирусом.J Virol 2011; 85 (24), 13061-8. DOI: 10.1128 / JVI.05869-11.
104. Баумгарт Н., Келсо А. Блокада гамма-интерферона in vivo влияет на гуморальный и местный клеточный иммунный ответ в ткани легких, вызванный вирусом гриппа. J Virol 1996; 70 (7), 4411-8. PubMed PMID: 8676464.
105. Вольф С., Джонсон С., Первитасари О., Махалингам С., Трипп Р.А. Нацеленность на провоспалительный фактор CCL2 (MCP-1) с помощью Биндарита для лечения гриппа A (H7N9).


