ИСТОРИЯ РАЗВИТИЯ ОНКОЛОГИИ
Опухоли (новообразования) человека известны с древнейших времен. Еще Гиппократ описал отдельные формы опухолей. Новообразования костей были обнаружены у мумий древнего Египта. Хирургические методы лечения опухолей использовали в медицинских школах древнего Египта, Китая, Индии, у инков Перу и др. Однако, несмотря на значительный интерес к вопросу возникновения и роста опухолей, несмотря на многообразные попытки их лечения, в продолжение ряда веков уровень медицинской науки не позволял глубоко изучить данные процессы. Это стало возможным только с изобретением во второй половине XIX века микроскопа и развитием патологической анатомии, особенная роль отводится работам Вирхова по целлюлярной патологии. Чрезвычайно важными для развития онкологии стали экспериментальные исследования на животных.
Наблюдение так называемого профессионального рака сыграло выдающуюся роль в изучении причин появления опухолей.
Отдельные наблюдения профессиональных заболеваний человека и многочисленные опыты на животных показали, что канцерогенным действием могут обладать рентгеновские и ультрафиолетовые лучи, радий и радиоактивные вещества.
Важным этапом в истории онкологии явилось открытие Раусом в 1910-1911 гг. вирусной природы некоторых сарком кур. Эти работы легли в основу вирусной концепции рака и послужили поводом для многих исследований, которые открыли ряд вирусов, вызывающих опухоли у животных (вирус папилломы кроликов Шоупа, 1933; вирус рака молочных желез мышей Битнера, 1936; вирусы лейкозов мышей Гросса, 1951;
Для изучения этиологии и патогенеза опухолей человека большое значение имеют исследования по эпидемиологии рака, подтверждающие несомненное влияние климатических, бытовых, профессиональных и других экзогенных и эндогенных факторов на возникновение и рост определенных форм злокачественных опухолей. Установлены значительные различия в частоте распространения разных форм рака в различных местах земного шара. Так, например, во вторую половину XX века резко увеличилась заболеваемость раком легкого в странах Западной Европы, особенно в Англии и США, что связывают с загрязнением атмосферы городов и распространением курения. Известно преобладание рака печени в развивающихся странах Африки, что может быть обусловлено недостаточностью белкового питания и наличием паразитарных заболеваний печени.
Установлены значительные различия в частоте распространения разных форм рака в различных местах земного шара. Так, например, во вторую половину XX века резко увеличилась заболеваемость раком легкого в странах Западной Европы, особенно в Англии и США, что связывают с загрязнением атмосферы городов и распространением курения. Известно преобладание рака печени в развивающихся странах Африки, что может быть обусловлено недостаточностью белкового питания и наличием паразитарных заболеваний печени.
В 1910 г. в России было издано первое руководство Н.Н. Петрова «Общее учение об опухолях». В начале XX века о вирусной природе злокачественных опухолей высказывались И.И. Мечников и Н.Ф. Гамалея. Культивированием опухолевой ткани занимались А.А. Кронтовский, Н.Г. Хлопин, А.Д. Тимофеевский и их сотрудники.
Первые в России работы по экспериментальной индукции опухолей
 Н. Петровым и Г.В. Шором с сотрудниками. Работы по изучению патогенеза опухолей, особенно по выяснению роли нарушений функций нервной системы в опухолевом процессе, проводили в СССР М.К. Петрова, А.А. Соловьев, С.И. Лебединский и др. В середине ХХ века все больший интерес вызывают иммунология опухолей и существование специфических опухолевых антигенов [Зильбер Л.А., 1948]. Выяснению роли мезенхимы и взаимоотношениям опухоли и организма были посвящены работы А.А. Богомольца, Р.Е. Кавецкого и их сотрудников.
Н. Петровым и Г.В. Шором с сотрудниками. Работы по изучению патогенеза опухолей, особенно по выяснению роли нарушений функций нервной системы в опухолевом процессе, проводили в СССР М.К. Петрова, А.А. Соловьев, С.И. Лебединский и др. В середине ХХ века все больший интерес вызывают иммунология опухолей и существование специфических опухолевых антигенов [Зильбер Л.А., 1948]. Выяснению роли мезенхимы и взаимоотношениям опухоли и организма были посвящены работы А.А. Богомольца, Р.Е. Кавецкого и их сотрудников.Изучение морфологии различных опухолей нашло отражение в трудах М.Ф. Глазунова, Н.А. Краевского и других советских патологоанатомов. Современные гистологические и цитологические исследования на молекулярном уровне (Ю.М. Васильев) углубили наши представления о свойствах опухолевых клеток.
Много усилий было направлено на изучение этиологии опухолей. Л.А. Зильбером разработана вирусогенетическая концепция опухолей. Его работы по иммунологии опухолей привели к исследованию опухолевых антигенов и, как результат, к открытию специфического печеночного альфа-фетопротеина, который стал диагностическим маркером рака печени.
Его работы по иммунологии опухолей привели к исследованию опухолевых антигенов и, как результат, к открытию специфического печеночного альфа-фетопротеина, который стал диагностическим маркером рака печени.
С помощью радиоактивных веществ и канцерогенных углеводородов впервые в мире были получены экспериментальные злокачественные опухоли у обезьян.
Изучение химических канцерогенных веществ привело к целому ряду достижений. В 1937 г. впервые в мире была доказана возможность получения опухолей у животных при введении экстрактов из тканей умерших от рака людей, так были заложены основы представлений об эндогенных бластомогенных веществах (Л.М. Шабад). Эта концепция была в дальнейшем развита как в СССР (Л.М. Шабад и др., М.О. Раушенбах), так и за рубежом (Лакассань, Бойланд).
Изучение канцерогенных углеводородов побудило к разработке точных количественных методов их обнаружения в различных компонентах внешней среды. На основании результатов этих исследований был разработан ряд рекомендаций по профилактике рака.
Наибольший размах приобрела экспериментальная и клиническая работа по химиотерапии опухолей. К традиционным методам лечения опухолей – хирургическому и лучевому – прибавилось лекарственное лечение. Эта новая отрасль онкологии бурно развивается и уже дает существенные результаты. Синтез и экспериментальное изучение новых противоопухолевых препаратов при правильно организованной системе кооперативного их испытания (во многих клиниках одновременно) и в контролируемых условиях сулят новые успехи химиотерапии опухолей.
В России первым онкологическим учреждением для лечения опухолей стал Институт им. Морозовых, основанный на частные средства в 1903 г. в Москве. В советские годы он был полностью реорганизован в существующий уже 75 лет Московский онкологический институт, получивший имя П.А. Герцена – одного из создателей московской школы онкологов. В 1926 г. по инициативе Н.Н. Петрова был создан Ленинградский институт онкологии, ныне носящий его имя.
В России разработана четкая система организации онкологической помощи. Это комплекс мероприятий, направленных на профилактику опухолей, их раннее выявление и разработку наиболее эффективных методов лечения. Система, возглавляемая онкологическими институтами, опирается на большое количество (около 250) онкологических диспансеров. Научно-исследовательские онкологические институты, а также институты рентгенорадиологии ведут подготовку специалистов-онкологов в аспирантуре и ординатуре. Усовершенствование врачей проводится кафедрами онкологии в институтах усовершенствования врачей (ныне – Академии последипломного образования).
В 1954 г. организовано Всесоюзное (теперь Российское) научное общество онкологов. Отделения этого общества работают во многих регионах, хотя ныне в силу определенных экономических обстоятельств, многие из них приобрели самостоятельность и организовали областные ассоциации онкологов. С участием онкологических институтов проводятся межобластные, республиканские конференции. Общество онкологов России организует съезды и конференции, а также входит в состав Международного противоракового союза, объединяющего онкологов большинства стран мира.
организовано Всесоюзное (теперь Российское) научное общество онкологов. Отделения этого общества работают во многих регионах, хотя ныне в силу определенных экономических обстоятельств, многие из них приобрели самостоятельность и организовали областные ассоциации онкологов. С участием онкологических институтов проводятся межобластные, республиканские конференции. Общество онкологов России организует съезды и конференции, а также входит в состав Международного противоракового союза, объединяющего онкологов большинства стран мира.
Во Всемирной организации здравоохранения (ВОЗ) существует специальный Отдел рака, основанный и в течение многих лет возглавляемый российскими онкологами. Специалисты России активно участвуют в международных конгрессах, работают в постоянно действующих комиссиях и комитетах Международного противоракового союза, ВОЗ и МАИР, принимают активное участие в симпозиумах по различным проблемам онкологии.
Несмотря на то, что злокачественные опухоли известны с древних времен, онкология (от греческого oncos – опухоль, logos – слово, наука) является молодой наукой – ей не более 100 лет, а полноценное развитие ее началось лишь в XX веке. Основные ее задачи: выяснение причин новообразований, разработка методов профилактики, способов раннего распознавания и успешного лечения.
Основные ее задачи: выяснение причин новообразований, разработка методов профилактики, способов раннего распознавания и успешного лечения.
Первоначально лечение опухолей целиком сосредоточилось в руках хирургов. В дальнейшем все шире стали применять методы лучевого лечения, которые для некоторых локализаций злокачественных опухолей и по сей день остаются методом выбора. Наконец, начиная с 40-х годов XX века стали применять и лекарственное лечение опухолей. В настоящее время все чаще прибегают к сочетанию всех этих методов лечения, подключая и иммунотерапию.
В последние годы достижения онкоиммунологии, онкогенетики (а правильнее, видимо, будет сказать в целом – биотерапии рака) вдохнули в науку «второе» дыхание, новые надежды на победу над этим недугом. Разрабатываются новые вакцины, новые методы генной терапии рака. Сообщения из разных стран, институтов и центров онкологии столь многочисленны, что порой уже трудно уследить за всеми новостями. Остается надеяться, что решение экономических проблем России существенно поможет делу борьбы с онкологическими заболеваниями.
Остается надеяться, что решение экономических проблем России существенно поможет делу борьбы с онкологическими заболеваниями.
рак. История лечения / Блог компании «Атлас» / Хабр
Злокачественная опухоль отличается от других видов опухолей и заболеваний тем, что её клетки схожи со здоровыми клетками организма. Поэтому перед учеными стоит непростая задача: различить клетки и уничтожить только зараженные. На протяжении истории у врачей были разные идеи о том, как это сделать. Сегодня Атлас расскажет о том, как развивалась онкология и чем лечат рак в наши дни.
Иллюстрации: Майкл Ковальски
Гуморальная теория Гиппократа
До 18 века онкологические заболевания было трудно изучать: подходящее оборудование еще не изобрели, церковь запрещала вскрытия, а чума и оспа уносили больше жизней и притягивали к себе внимание. Поэтому с древних времен до нас дошло мало записей о злокачественных опухолях, но все же они есть.
Первые упоминания рака встречаются в папирусе Эдвина Смита — медицинском тексте Древнего Египта, который датируется 16 веком до нашей эры. Этот папирус можно полистать и почитать. Случай № 45 как раз описывает злокачественные опухоли. Там же отмечается, что метода лечения нет.
Этот папирус можно полистать и почитать. Случай № 45 как раз описывает злокачественные опухоли. Там же отмечается, что метода лечения нет.
Гиппократ (400 лет до нашей эры) первым начал различать доброкачественные и злокачественные опухоли. Он считал, что тело человека содержит четыре гумора, или жидкости — кровь, слизь, желтую и черную желчь, — а любой дисбаланс приводит к заболеваниям. Считалось, что причина злокачественных опухолей — скопление черной желчи в определенном месте. Гиппократ отмечал, что без лечения больные могут прожить дольше: черная желчь уже распространилась по организму и удалить ее нельзя.
Конечно, никакой черной желчи в организме человека нет, но идея о распространении опухоли по организму оказалась верной. Злокачественные клетки со временем отделяются от опухоли и дают метастазы.
Врачи и знахари пользовались гуморальной теорией более 1300 лет. В течение этого периода вскрытия были запрещены по религиозным соображениям, что ограничивало изучение опухолей. Доступными методами лечения в древние времена и Средневековье были хирургия, прижигание, кровопускание и обряды.
Доступными методами лечения в древние времена и Средневековье были хирургия, прижигание, кровопускание и обряды.
Первые хирургические вмешательства
Хирургия — одна из самых древних отраслей медицины. Однако в средневековые времена вмешательства не всегда приводили к нужным результатам из-за большой потери крови, высокого риска заражения после операции, отсутствия антисептиков.
Гален
Римский врач Гален (130-200 годы нашей эры) писал о хирургическом лечении рака молочной железы на ранней стадии, но не считал этот метод эффективным для лечения крупных и «скрытых» опухолей. Он придерживался гуморальной теории и предполагал, что черную желчь удалить из организма полностью нельзя. Такой подход спас жизнь многим людям: в Средневековье пациенты часто умирали во время операции или из-за осложнений после нее.
Отмена гуморальной теории
После отмены запрета на вскрытия в 16 веке Андреас Везалий составил первый анатомический справочник тела человека, а веком позже Метью Бейли описал строение различных патологий. Гуморальную теорию пришлось пересмотреть, так как никакой черной желчи ученые не нашли.
Гуморальную теорию пришлось пересмотреть, так как никакой черной желчи ученые не нашли.
В 17 веке начали развиваться хирургические методы удаления опухолей. Немецкий хирург Вильгельм Фабри во время операции по удалению рака молочной железы вырезал опухоль вместе с увеличенными лимфоузлами, а голландский хирург Адриан Гельвеций проводил мастэктомию, полное удаление молочной железы. Несколько лет спустя, он писал про один из случаев: «С тех пор пациентка полностью выздоровела. Боли совершенно прекратились, рубцы зажили, и она наслаждается тем же состоянием здоровья, которое у нее было до рака».
В 1850–х немецкий ученый Рудольф Вирхов обнаружил в опухолях бесконтрольное деление клеток. Он назвал это явление неоплазией, а его главный труд «Клеточная патология» стал основой для понимания причин развития онкологических заболеваний.
Обезболивание и антисептик
В 1846 году был изобретен наркоз. Это решило проблему с болью, так как до этого людям приходилось переживать операцию в сознании. А в 1867 году французский врач Джозеф Листер открыл, что мазь на основе карболовой кислоты действует как антисептик и способствует заживлению раны после операции.
А в 1867 году французский врач Джозеф Листер открыл, что мазь на основе карболовой кислоты действует как антисептик и способствует заживлению раны после операции.
Анестезия и первый антисептик расширили возможности хирургии, и операции стали проводиться повсеместно. Однако в некоторых случаях опухоли появлялись вновь. Тогда хирурги начали расширять объемы вмешательств, что в итоге привело к возникновению метода радикальной хирургии.
Радикальная хирургия
Хирург Уильям Холстед думал, что чем больше тканей удалить во время операции, тем меньше будет вероятность рецидивов. Вывод не совсем верный, так как злокачественные клетки еще до операции могли распространиться по организму и метастазировать в другие ткани.
Только в 1970–х годах в ходе клинических испытаний было доказано, что менее обширные операции эффективны так же, как и радикальные. К сожалению, к этому времени радикальная мастэктомия набрала большую популярность и считалась практически единственным верным методом лечения рака молочной железы.
Современность
В 1990-е годы хирурги минимизировали вмешательства в здоровые ткани человека. Сегодня операции делятся на два вида: открытые и малоинвазивные. Для открытой операции врач делает большой разрез, чтобы удалить опухоль, нездоровые ткани и, возможно, лимфоузлы.
Для проведения малоинвазивной операции врач делает несколько небольших разрезов, находит опухоль с помощью тонкой трубки с камерой (лапароскопа) и через другой разрез удаляет опухоль инструментами. После этой операции пациент восстанавливается быстрее.
Лучевая терапия
В конце 19 века ученых обратили внимание на способность рентгеновских лучей убивать злокачественные клетки. Тогда никто еще не догадывался, насколько губительно излучение действует и на здоровые ткани.
Рентгеновские трубки
Рентгеновские лучи были открыты в 1895 году, одновременно с развитием радикальной хирургии. Через год после этого молодой врач Эмиль Груббе заметил, как разрушаются кожа и ногти у людей, которые работали с источниками излучения. Он предположил, что лучи убивают и клетки опухоли, и был первым, кто использовал лучевую терапию для лечения онкологии.
Он предположил, что лучи убивают и клетки опухоли, и был первым, кто использовал лучевую терапию для лечения онкологии.
Метод быстро набрал популярность: в Европе и США открывались новые клиники, предлагающие лучевую терапию. Она была эффективной в тех случаях, когда опухоль не успела распространиться на другие органы.
Идея использовать излучение была отличной, но она не учитывала два существенных минуса рентгеновской трубки: неоднородный поток излучения и недостаточную проникающую способность. Большая часть дозы поглощается другими тканями или рассеивается. Таким образом рентгеновские лучи увеличивают количество мутаций в здоровых клетках, что приводит к формированию новых опухолей. Такой вариант нельзя считать подходящим лечением.
Радий
В 1902 году ученые Пьер и Мария Кюри открыли радиоактивные свойства радия. На первый взгляд, это вещество проникало глубже рентгеновских лучей и давало больше возможностей для лечения. На протяжении 10 лет после открытия радия у многих врачей и ученых, не знающих об опасности облучения, развивались различные злокачественные заболевания. Так продолжалось до тех пор, пока не появились первые дозиметры и стандарты измерений радиоактивного излучения.
Так продолжалось до тех пор, пока не появились первые дозиметры и стандарты измерений радиоактивного излучения.
Ускоритель электронов и радиоактивный кобальт
В 1940 Дональд Керст собрал бетатрон — циклический ускоритель электронов. Устройство испускает частицы, обладающие высокой энергией и проникающей способностью, поэтому при его использовании возникает мало рассеянных лучей. В 1951 шведский нейрохирург Ларс Лекселл разработал аппарат «Гамма-нож». Он имеет несколько источников излучения радиоактивного кобальта и дает однородный пучок большой энергии. Бетатрон и гамма-нож успешно применяются для лечения опухолей и сегодня.
Излучение разрушает ДНК клеток прямо или косвенно. Во втором случае вода, которая содержится в клетках, превращается в свободные радикалы — заряженные частицы, повреждающие ДНК. Излучение не разбирает, какие клетки разрушать, здоровые или злокачественные, поэтому аппараты требуют внимательной настройки, чтобы пик дозы приходился на нужную глубину.
Современность
Сегодня в онкологии используют рентгеновское излучение, гамма-лучи и заряженные частицы. Они могут поступать в тело и воздействовать на злокачественные клетки через специальное устройство либо исходить от радиоактивного материала, помещенного в тело пациента рядом с опухолью (брахитерапия).
Существует также третий вид лучевой терапии — системный. Пациенту вводят радиоактивную жидкость, например йод, который находит и убивает клетки опухоли. Но в этом случае трудно учесть точное количество изотопа, которое поглощает организм, и доза может нанести вред.
Химиотерапия
Хирургия и лучевая терапия применялись для лечения солидных опухолей, которые развиваются не из клеток кроветворной системы. Как лечить лимфомы и лейкемию никто не знал.
Горчичный газ
Идея использовать токсичные вещества для лечения этих заболеваний возникла после Первой мировой войны. В это время в качестве химического оружия применялся иприт — горчичный газ. Он обжигал кожу и слизистые оболочки, а также убивал лейкоциты: у раненых они практически отсутствовали.
Он обжигал кожу и слизистые оболочки, а также убивал лейкоциты: у раненых они практически отсутствовали.
Ученые задались вопросом, может ли иприт вылечить лимфому — опухоль лимфатической ткани. При этом заболевании лимфоциты бесконтрольно делятся и нарушают работу лимфатических узлов и других органов, поэтому сокращение лимфоцитов казалось верным решением. В 1942 году после исследований на животных больному лимфомой ввели внутривенно 10 доз иприта. Количество лимфоцитов быстро упало, а опухоль уменьшилась, но позже начала расти вновь. Это означало, что терапия подействовала, но дозы было недостаточно для полного выздоровления.
Ремиссия наступала потому, что горчичный газ входит в группу алкилирующих агентов, которые разрушают ДНК клеток и не дают им делиться. Но тогда об этом еще ничего не знали.
Предшественник метотрексата
В 1947 году врач Сидни Фарбер показал, что производное фолиевой кислоты, аметоптерин, подавляет у детей развитие острого лейкоза, который характеризуется бесконтрольным делением белых клеток крови. Этот препарат был предшественником метотрексата, который применяют и сейчас.
Этот препарат был предшественником метотрексата, который применяют и сейчас.
Результаты биопсии костного мозга пациентов после курса лечения аметоптерина были в норме. Химиотерапия продлевала жизнь детей до 6 месяцев, но затем болезнь возвращалась. Фарбер бросил все силы на то, чтобы найти лекарство, которое смогло бы вылечить лейкемию полностью. Тогда трудно было предположить, что нужно использовать сразу несколько токсичных веществ, а не одно.
В 1950 году Гертруда Элион разработала препарат 6-меркаптопурин (6-МП), который быстро получил разрешение к применению у детей с лейкозом. После него врачи снова наблюдали недолгую ремиссию.
Комбинированная химиотерапия
Позже были проведены рандомизированные клинические испытания, в ходе которых стало ясно, что использование двух препаратов вместо одного продлевает ремиссию и улучшает прогноз.
В 1956 году доктор Мин Чиу Ли клинически подтвердил, что комбинация из четырех препаратов вылечила метастатическую хориокарциному у беременных. Национальный институт онкологии сначала расценил эти действия как агрессивное и лишнее лечение пациентов, и ученого отстранили от работы. Только потом стало понятно, что выжили только те женщины, которые прошли полный курс лечения Ли. Это был первый случай полного излечения методом химиотерапии.
Национальный институт онкологии сначала расценил эти действия как агрессивное и лишнее лечение пациентов, и ученого отстранили от работы. Только потом стало понятно, что выжили только те женщины, которые прошли полный курс лечения Ли. Это был первый случай полного излечения методом химиотерапии.
Адъювантная химиотерапия
В 60 и 70–е годы ученые пробовали использовать химиотерапию как дополнительный метод лечения рака молочной железы после операции. Хирурги неохотно шли на клинические исследования: никто не хотел иметь дело с дополнительными побочными эффектами у пациентов. Но они были неправы.
На деле, любая опухоль — системное заболевание. Злокачественные клетки распространяются по организму даже на ранних стадиях в виде микрометастазов. Они остаются в организме даже после удаления опухоли, поэтому локальных методов лечения недостаточно. Нужно системно воздействовать на заболевание с помощью лекарственного лечения. Например, адъювантная терапия (курс химиотерапии после операции) позволяет снизить риск рецидива и смерти.
Несколько исследований доказали положительный результат адъювантной химиотерапии для лечения рака молочной железы и колоректального рака. Также в 1974 году был доказан положительный эффект в случае метастатического рака яичек, и химиотерапию стали применять для лечения солидных опухолей.
Препараты для химиотерапии останавливают и замедляет деление клеток. Во время курса лечения гибнут те клетки, которые быстро делятся. Это не только злокачественные клетки, но и здоровые, что приводит к побочным эффектам: выпадению волос, тошноте, подверженности инфекциям.
Иммунотерапия
Иммунотерапия — относительно новый вид лечения рака. В его основе лежит использование препаратов, тренирующих клетки иммунитета пациента. Это стало возможным благодаря открытию структуры ДНК, изучению особенностей злокачественных клеток и клеток иммунной системы.
Вакцина Коли
В 1891 году Вильям Коли заметил, что у онкобольных, перенесших скарлатину или рожистую болезнь, наступала ремиссия.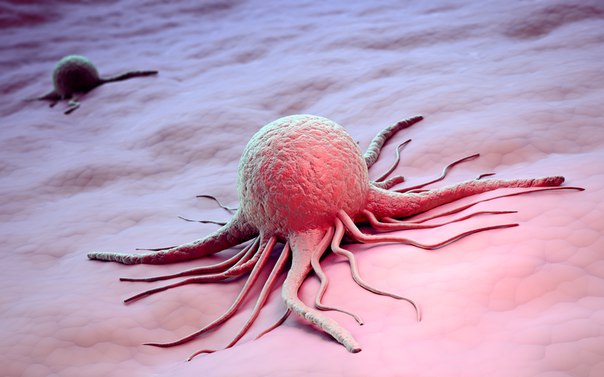 После этого он начал вводить пациентам с последней стадией рака бактерии стрептококков. Опухоль уменьшалась, но больные умирали от инфекции. Тогда Коли нагревал вакцину и вводил пациентам мертвые стрептококки.
После этого он начал вводить пациентам с последней стадией рака бактерии стрептококков. Опухоль уменьшалась, но больные умирали от инфекции. Тогда Коли нагревал вакцину и вводил пациентам мертвые стрептококки.
Результат для того времени был впечатляющим: больные выздоравливали и жили несколько лет. Однако вакцина Коли не получила широкого распространения. Ученые не могли объяснить механизм, как бактерии действуют на опухоль, а риск инфицирования был высоким. Всех гораздо больше интересовала химио- и лучевая терапия.
В 1976 году для лечения рака мочевого пузыря успешно применили вакцину BCG, которая использовалась для предупреждения туберкулеза. Она активизирует иммунную систему и помогает организму бороться с этим видом рака.
Моноклональные антитела
В 1975 году Жорж Кёллер и Сезар Мильштейн опубликовали статью о методе получения клеточного гибрида опухолевой клетки и лимфоцита. Гибридомная технология позволяет обнаружить антигены, характерные для опухолей определенных тканей, получить к ним антитела и использовать их для диагностики и типирования опухолей. Такие антитела называются моноклональными: они вырабатываются иммунными клетками-клонами, которые происходят из одной родительской клетки.
Такие антитела называются моноклональными: они вырабатываются иммунными клетками-клонами, которые происходят из одной родительской клетки.
Другие типы антител маркируют раковые клетки, чтобы иммунной системе было легче найти и уничтожить их.
В конце 1990 годов FDA одобрила первые терапевтические моноклональные антитела, ритуксимаб и трастузумаб. Первый для лечения лимфомы, а второй — рака молочной железы.
В 2010 году Стивен Розенберг объявил об успехе терапии химерными антигенными рецепторами. В основе нее лежит генетическая модификация Т-клеток пациента для лечения злокачественной опухоли.
Цитокины
Другой метод иммунотерапии — введение в мышцу или вену цитокинов, биологически активных белков, которые регулируют иммунную реакцию. Интерлейкин-2 помогает клеткам иммунной системы быстрее делиться, а интерферон — бороться с вирусными инфекциями и злокачественными опухолями.
Контрольные точки
Еще одно перспективное направление — воздействие на иммунные контрольные точки, которые подавляют ответ иммунной системы. Ученые научились блокировать контрольные точки на Т-клетках, что помогает иммунной системе распознавать и атаковать злокачественные клетки. Этот метод уже одобрен FDA для лечения онкологических заболеваний.
Ученые научились блокировать контрольные точки на Т-клетках, что помогает иммунной системе распознавать и атаковать злокачественные клетки. Этот метод уже одобрен FDA для лечения онкологических заболеваний.
Подобрать оптимальное лечение можно с помощью молекулярной диагностики. Ученые исследуют операционный материал или биопсию пациента, чтобы выявить мутации в протоонкогенах и генах супрессорах. Набор мутаций индивидуален для каждой опухоли, поэтому лечение должно быть персонализированным. В следующий раз Атлас подробно расскажет о молекулярной диагностике.
Рак появился по вине человека
+ A —
Природа не виновата в возникновении онкологических заболеваний
Рак является современным, антропогенным заболеванием, вызванным такими факторами, как загрязнение окружающей среды, современный образ жизни и диета, убеждены исследователи Университета Манчестера (УМ). В древности же им болели редко.
В древности же им болели редко.
Исследование древних останков и литературы Древних Египта и Греции, а также более ранних периодов — выполненное в Центре биомедицинской египтологии при УМ и опубликованное в «Nature» — являет собой первый гистологический диагноз рака у египетской мумии.
Обнаружение лишь одного случая этого заболевания при изучении сотен египетских мумий, наряду с немногочисленными упоминаниями о раке в «литературе», показывает, что в древности рак встречался чрезвычайно редко. Уровень заболеваемости раком стал массово расти со времен Промышленной революции. В частности распространение детского рака доказывает, что распространение заболевания не связано с тем, что люди стали жить дольше.
Профессор Розали Дэвид с факультета Наук о жизни УМ говорит: «В промышленно развитых обществах рак занимает второе место после сердечно-сосудистых заболеваний в качестве причины смертности. В природе нет ничего такого, что могло бы вызывать рак. Мы изучили этот вопрос в глубокой исторической ретроспективе — мы рассмотрели историю многих столетий».
Профессор Майкл Циммерман диагностировал рак прямой кишки у неизвестной мумии «обычного» человека, который жил в Оазисе Дахла во времена правления Птолемеев (200-400 н.э.).
По словам Циммермана, «в древнем обществе, как правило, отсутствует хирургическое вмешательство, поэтому всякое свидетельство о раке должно сохранятся «нетронутым». Фактическое отсутствие злокачественных опухолей у мумий следует интерпретировать как подтверждение их редкой встречаемости в древних временах».
Доказательства рака в окаменелостях животных, нечеловекообразных приматов и ранних людей слишком малочисленны — всего несколько десятков, в основном, спорных примеров среди животных окаменелостей. Конечно, метастатический рак неизвестного происхождения находили у окаменелости Эдмонтозавра (Edmontosaurus). Различные злокачественные новообразования регистрировались у нечеловекообразных приматов, тем не менее среди них не попадались многих из видов рака, обычно идентифицируемых у современных взрослых людей.
Ранние описания операций по удалению рака груди и других видов опухолей появились лишь в 17-м веке. В то время как первые доклады в научной литературе о конкретных видах рака стали появляться в последние 200 лет. Среди примеров — сообщения о раке мошонки у трубочистов в 1775 году, о раке носа у нюхальщиков табака в 1761 году и о болезни Ходжкина (лимфогранулематозе, злокачественной гранулеме) в 1832 году.
Эволюция рака
Рак — причина 12 процентов всех смертей в мире. Ежегодно врачи выявляют более 12 миллионов новых онкологических пациентов, а 7 миллионов людей погибает. Долгое время рак был неизлечимым проклятием человечества — прогресс в его лечении наметился только в XIX веке. При этом рак еще не побежден — борьба с болезнью ведется до сих пор. Вместе с компанией BIOCAD разобрались, как люди болели (и лечились) от рака в прошлые эпохи, и какого прогресса человечество достигло в этом вопросе в наши дни.
Правда ли, что древние люди реже болели раком?
Это утверждение звучит резонно. Особенно если учесть, что среди причин онкологических заболеваний есть употребление табака, воздействие радиации и контакт с промышленными веществами-канцерогенами.
Однако утверждать, что онкологических заболеваний в древности было намного меньше, со всей уверенностью нельзя. Хотя бы потому, что 5-10 процентов всех видов рака связаны с генами, унаследованными от родителей — то есть получить онкологическую болезнь «по наследству» в древности можно было точно так же, как и в наши дни.
Узнать правду о том, насколько были распространены онкологические заболевания в прошедшие эпохи, должны помочь древние захоронения. Однако изучать заболеваемость раком по костям очень сложно.
Однако изучать заболеваемость раком по костям очень сложно.
Во-первых, если речь идет о по-настоящему давних временах, до нас доходит не так уж много костных остатков. Во-вторых — и это самое главное — не все онкологические заболевания оставляют следы на костях.
Исследуя скелеты людей, живших в прошлые эпохи, проще всего найти первичные опухоли костей — а это менее 0,2 процента всех онкозаболеваний
Library of Congress
Еще в костях порой можно обнаружить метастазы некоторых других видов онкологических болезней: рака молочной железы, предстательной железы и легкого. Однако это не так просто, как кажется. В 1996 году английский палеонтолог Тони Вальдрон изучил регистр смертей за 1901–1905 годы и выяснил, что вероятность обнаружения признаков рака в костных останках мужчин составляет 0–2 процента, а у женщин — 4–7 процентов.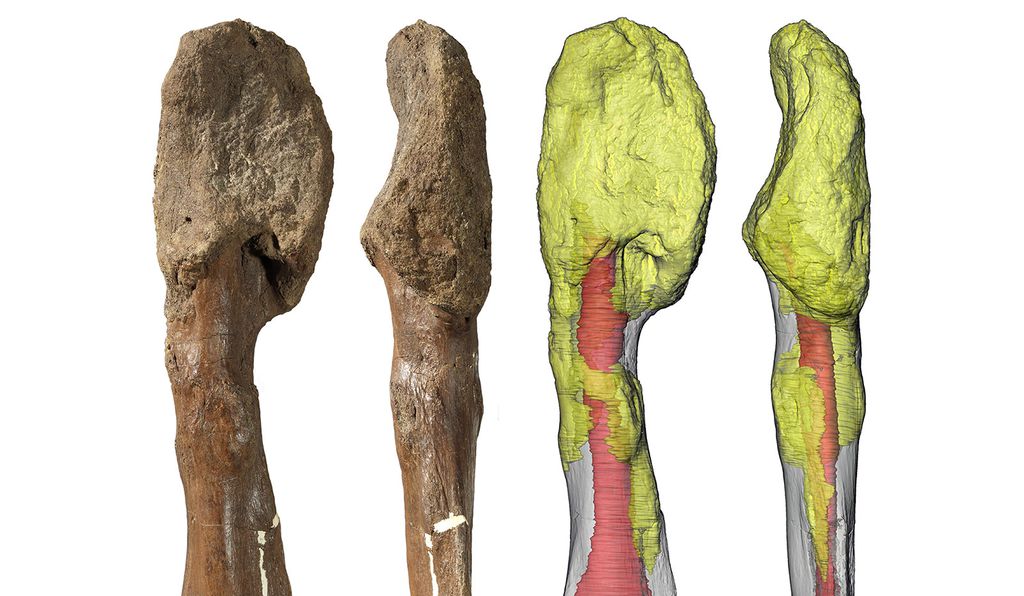
Поэтому с уверенностью мы можем утверждать только одно — раком люди болели всегда: и в каменном веке, и в более поздние эпохи. Например, в 2007 году ученые из Мюнхена обнаружили пять случаев рака среди 905 скелетов в египетских некрополях, и тринадцать случаев — среди 2547 захоронений на средневековом кладбище в Германии.
Другое дело, что характер заболеваемости и частота встречаемости различных онкологических заболеваний в стародавние времена, скорее всего, был совсем иным, чем сейчас. Хотя бы потому, что продолжительность жизни людей все время увеличивается.
По прогнозам, к 2030 году 70 процентов всех случаев рака будет выявляться у людей в возрасте 65 лет и старше. Но всего 200 лет назад (то есть в середине XIX века) средняя ожидаемая продолжительность жизни мужчин составляла 40 лет, а женщин — 42 года. Получается, что до многих видов рака, распространенных в наши дни, предки попросту не доживали.
Как лечили рак до XX века
Самый древний метод лечения рака был описан в медицинском папирусе Эберса — то есть в 1500 году до нашей эры. Египетский фараон Имхотеп рекомендовал «прото-иммунотерапию»: нужно было сделать припарку возле опухоли, а потом надрезать ее. Фараон рассчитывал, что в месте надреза начнется воспаление, которое уничтожит опухоль.
Египетский фараон Имхотеп рекомендовал «прото-иммунотерапию»: нужно было сделать припарку возле опухоли, а потом надрезать ее. Фараон рассчитывал, что в месте надреза начнется воспаление, которое уничтожит опухоль.
Самое интересное, что «фараонский» метод вполне мог сработать. Например, редкая раковая опухоль святого Перегрина способна к спонтанной регрессии — но только в том случае, если в рану попадет инфекция. Однако куда чаще целители из Египта, Греции, Рима и Индии ограничивались тем, что прикладывали к опухоли тепло — в надежде, что нагревание поможет справиться с болезнью.
Рак святого Перегрина: болезнь с чудесным исцелением
Отец Перегрин жил на рубеже XIII-XIV веков, происходил из хорошей семьи и вел праведную жизнь — а прославился благодаря необычной истории своей болезни. В молодости священник заболел раком голени, которая потребовала ампутации ноги. Однако, когда подошел срок операции, врач увидел, что опухоль исчезла — так что удачливый священник ушел из его «кабинета» на обеих ногах.
Сегодня мы знаем, что «самопроизвольное» излечение от рака — вполне возможное, хотя и достаточно редкое явление. Иногда попавшие в рану микробы действительно «модифицируют» иммунный ответ, и организм оказывается в состоянии победить рак. На этом принципе основана современная иммунотерапия. Однако в средние века о работе иммунитета ничего не знали, так что чудесное исцеление приписали не микробам, а божественному вмешательству.
Долгие годы «иммунотерапия» путем загрязнения хирургической раны шла «в комплекте» с хирургическим лечением рака. Поскольку о стерильности хирургических кабинетов и инструментов речь не шла, вырезавшие раковые опухоли хирурги неизбежно заносили в них болезнетворных бактерий (например, Streptococcus pyogenes и Serratia marcescens).
Для многих прооперированных людей это заканчивалось плачевно, поскольку приводило к сепсису (смертельному заражению крови — прим.ред). Однако некоторые пациенты, страдавшие способным к регрессии раком, вытягивали «счастливый билетик» и исцелялись. Подобные случаи описывали и в XVIII, и в XIX, и даже в начале XX века.
Подобные случаи описывали и в XVIII, и в XIX, и даже в начале XX века.
Авторство термина «рак» приписывают греческому врачу Гиппократу (460-370 годы до нашей эры). Считается, что он первым использовал слово «carcinos» для описания не образующих язвы опухолей, а слово «carcinoma» — для описания «язвенных» опухолей.
Оба термина — «carcinos» и «carcinoma» — восходят к греческому слову «краб». Возможно, ученый решил, что силуэт опухоли под кожей напоминает это животное
За второй термин, «онкология», мы должны быть признательны второму греческому врачу, Галену (130-200 годы нашей эры). Для описания опухолей он использовал греческое слово «отек», или «oncos». Оба знаменитых грека придерживались гуморальной теории, в соответствии с которой за здоровье человека отвечают четыре жидкости организма: кровь, мокрота, желтая и черная желчь. Если баланс этих жидкостей нарушается, человек заболевает. В соответствии с этой теорией к раку приводил избыток черной желчи, которая скапливается в некоторых органах и тканях. Их идеи продержались до конца Средних веков.
Если баланс этих жидкостей нарушается, человек заболевает. В соответствии с этой теорией к раку приводил избыток черной желчи, которая скапливается в некоторых органах и тканях. Их идеи продержались до конца Средних веков.
Чтобы вылечить рак «по Галену», нужно было либо нормализовать образ жизни при помощи правильного питания и переезда в «здоровое место» подальше от болот с их тлетворными испарениями — либо попытаться выпустить избыток черной желчи из опухоли хирургическим путем. Однако в отсутствие антибиотиков хирургическое лечение онкологических болезней было крайне болезненным и рискованным делом.
Вплоть до середины XIX века большинство пациентов предпочитало хирургии самое фантастическое якобы «медикаментозное» лечение. Аптекари запаслись зубом кабана, легкими лис, настойкой свинца, молотым белым кораллом и другими сомнительными средствами. Хирургические операции применялись нечасто — лишь изредка хирурги-парикмахеры проводили мастэктомию (удаление опухоли груди). Разумеется, без анестезии и в антисанитарных условиях.
Разумеется, без анестезии и в антисанитарных условиях.
В XVIII веке на смену гуморальной теории пришла теория лимфы. Но это было немногим лучше гуморальной теории. В то время считалось, что рак возникает, если в органах и тканях понемногу накапливается разрушающая и отравляющая организм лимфатическая жидкость.
Истинный прорыв в лечении рака произошел только в XX веке. В это время на помощь хирургам пришли методы, которые до сих пор широко используются в онкологии: лучевая терапия, гормональная терапия, иммунотерапия и химиотерапия
Library of Congress
Прорыв в понимании причин рака случился только в середине XIX века, с появлением микроскопа современного типа. «Отцом онкологии» стал немецкий ученый Рудольф Вирхов — он не только впервые описал раковые клетки, но и установил, что между воспалением и онкологическими заболеваниями есть прямая связь./woman-pointing-to-area-on-mammogram-x-ray--close-up-200410227-001-59c80e7b6f53ba00102734c1.jpg) Теперь удаленные хирургом опухолевые ткани можно было исследовать и уверенно отличать от здоровых.
Теперь удаленные хирургом опухолевые ткани можно было исследовать и уверенно отличать от здоровых.
А поскольку к тому времени уже была изобретена асептическая хирургия (спасибо за нее мы должны сказать английскому доктору Джозефу Листеру) и анестезия (которую изобрел бостонский стоматолог Уильям Мортон), оперативное лечение онкологических заболеваний впервые перестало напоминать гусарскую рулетку.
Лечение рака в XX веке: краткая история
Лучевая терапия. В 1898 году Мари и Пьер Кюри открыли, что радий и полоний могут испускать радиоактивное излучение. Через четыре года после этого немецкий биолог Теодор Бовери пришел к выводу, что раковые опухоли возникают из обычных клеток с поврежденными хромосомами.
Примерно в то же время удалось выяснить, что излучение радия тоже способно повреждать хромосомы в клетках. Еще через год радий впервые использовали, чтобы повредить раковые клетки еще сильнее — и уничтожить их. В эксперименте приняли участие два пациента с базально-клеточным раком — и оба выздоровели.
Долгое время главной проблемой лучевой терапии была ее неуправляемость. Возникали сложности как с расчетами нужной дозы облучения, так и с четким нацеливанием его на раковые клетки. Это очень важно: если перестараться с облучением и промахнуться мимо опухоли, облучение неизбежно повреждало в том числе и здоровые клетки. К счастью, в последней четверти XX века была изобретена конформная лучевая терапия. При этом подходе луч направляют при помощи компьютерной томографии, которая позволяет получить точные трехмерные модели облучаемой ткани.
Затем появилась лучевая терапия с модуляцией интенсивности (IMRT), которая позволяет регулировать интенсивность воздействия, и радиосенсибилизаторы — вещества, которые делают раковые клетки более чувствительными к воздействию радиации. Все это позволило заметно уменьшить побочные эффекты от лечения.
Химиотерапия. В 1909 году немецкий химик Пауль Эрлих предположил, что иммунная система организма способна выслеживать и уничтожать раковые клетки. Впоследствии эта идея превратилась в «гипотезу иммунного надзора», а Эрлих стал «отцом» сразу двух методов лечения онкологических заболеваний — иммунотерапии и химиотерапии.
Впоследствии эта идея превратилась в «гипотезу иммунного надзора», а Эрлих стал «отцом» сразу двух методов лечения онкологических заболеваний — иммунотерапии и химиотерапии.
Однако прорыв в химиотерапии случился только после Второй мировой войны, в 1949 году. В то время ученые активно изучали ядовитый иприт, больше известный как горчичный газ, который применялся в качестве химического оружия. Неожиданно исследователи выяснили, что азотистые соединения иприта помогают бороться с раком лимфатических узлов (лимфомой). «Доработанные» соединения иприта стали первыми в истории химиотерапевтическими лекарствами от рака.
В дальнейшем было открыто множество химиотерапевтических лекарств: от аминоптерина (соединение фолиевой кислоты, или витамина В9), способного обращать вспять острый лейкоз у детей, до адъювантной терапии, которая помогала в борьбе с неуловимыми метастазами. В 1958 году появилась комбинированная химиотерапия, при которой применяется сразу несколько препаратов, и которая действует более эффективно.
Гормонотерапия. В 1941 году американский физиолог Чарльз Хаггинс обнаружил, что снижение уровня тестостерона одновременно с повышением уровня эстрогенов в организме обращает вспять опухоль простаты. Чтобы добиться этой цели, Хиггинс удалял яички и вводил пациентам женские половые гормоны — так появилась гормональная терапия, которая до сих пор лежит в основе лечения рака предстательной и молочных желез.
В наши дни с той же целью применяют более щадящее лечение — используют препараты, блокирующие мужские и женские половые гормоны. Например, ингибиторы ароматазы и лютеинизирующего гормона.
Иммунотерапия. Этот метод лечения рака одновременно и самый передовой, и самый древний — если, конечно, считать первооткрывателем иммунотерапии фараона Имхотепа. На самом деле, осознанное применение этой методики стало возможно только с 1970-х годов, когда ученые наконец научились массово производить моноклональные антитела.
Антитело — особый белок, который белые клетки используют для «маркировки» всего опасного и нежелательного, от микробов до раковых клеток. Ориентируюсь на антитела, как на дорожные знаки, другие белые клетки быстро находят и уничтожают патоген.
Ориентируюсь на антитела, как на дорожные знаки, другие белые клетки быстро находят и уничтожают патоген.
Когда исследователи поняли, что можно создать антитела, которые будут распознавать раковые клетки, это был настоящий прорыв. Дело в том, что наиболее универсальные и эффективные методы лечения онкологических заболеваний — химиотерапия и лучевая терапия — токсичны для организма и дают тяжелые побочные эффекты. Одно из таких осложнений — нейтропения, то есть резкое снижение количества белых клеток в крови.
Химиотерапия, как воздушная гимнастика, требует страховки: чем опасна нейтропения и как ее победить
Химиотерапия (ХТ) – один из базовых методов лечения онкологических пациентов. Лекарства, которые применяют при химиотерапии (цитостатики), нарушают процессы роста, развития, механизмы деления всех клеток организма и обладают высокой пролиферативной активностью. Этим качеством, как правило, характеризуются клетки злокачественных новообразований. Клинические исследования подтверждают, что противоопухолевый эффект зависит от дозы цитостатиков и режима химиотерапии.
Клинические исследования подтверждают, что противоопухолевый эффект зависит от дозы цитостатиков и режима химиотерапии.
Одно из самых частых осложнений цитотоксической терапии — нейтропения, или аномально низкий уровень белых клеток крови (нейтрофилов), которые играют важную роль в формировании иммунного ответа организма. Под воздействием химиотерапии уничтожаются не только нейтрофилы, но и место их продукции – костный мозг. Организм со сниженным числом нейтрофилов практически беззащитен перед инфекцией любой природы и силы. Кроме того, нейтропения сильно снижает эффективность проводимого лечения, так как из-за этого осложнения врачу приходится изменять оптимальный режим терапии и редуцировать дозы цитостатиков.
Однако нейтропения нейтропении рознь. На фоне одних схем химиотерапии количество нейтрофилов снижается не очень сильно, а при применении других у пациентов развивается «нейтропеническая лихорадка», или фебрильная нейтропения (ФН). Это жизнеугрожающее состояние, требующее неотложной медицинской помощи. Высокий риск развития ФН наблюдается при лечении многих онкологических болезней и сопровождает практически все схемы терапии онкогематологических заболеваний. Среди онкологических нозологий можно выделить рак молочной железы, рак легкого, рак шейки матки и яичников, рак яичка, колоректальный рак, саркомы и рак желудка. В группе высокого риска развития ФН находятся пациенты с такими лимфопролиферативными заболеваниями как лимфома Ходжкина и неходжкинские лимфомы, острый лимфобластный лейкоз, множественная миелома, диффузная B-крупноклеточная лимфома, первичная медиастинальная лимфома, лимфома ЦНС и другие.
Высокий риск развития ФН наблюдается при лечении многих онкологических болезней и сопровождает практически все схемы терапии онкогематологических заболеваний. Среди онкологических нозологий можно выделить рак молочной железы, рак легкого, рак шейки матки и яичников, рак яичка, колоректальный рак, саркомы и рак желудка. В группе высокого риска развития ФН находятся пациенты с такими лимфопролиферативными заболеваниями как лимфома Ходжкина и неходжкинские лимфомы, острый лимфобластный лейкоз, множественная миелома, диффузная B-крупноклеточная лимфома, первичная медиастинальная лимфома, лимфома ЦНС и другие.
При ФН число циркулирующих в крови нейтрофилов падает ниже 500/мм³. Это предельно малый уровень, абсолютно недостаточный для защиты организма от инфекций. По этой причине у страдающих ФН людей риск развития тяжелых инфекционных осложнений увеличивается на 30 процентов, а риск гибели — на 15 процентов.
К счастью, своевременная профилактика заметно уменьшает риски, связанные с воздействием химиотерапии, и достоверно снижает вероятность развития нейтропении. Для этого на фоне лечения химиотерапией применяют специальные препараты — гранулоцитарные колониестимулирующие факторы (Г-КСФ). Эти вещества относятся к цитокинам — небольшим сигнальным молекулам, которые синтезируются в организме человека. Цитокины «побуждают» костный мозг создавать больше клеток крови и активно выпускать их в кровь.
Для этого на фоне лечения химиотерапией применяют специальные препараты — гранулоцитарные колониестимулирующие факторы (Г-КСФ). Эти вещества относятся к цитокинам — небольшим сигнальным молекулам, которые синтезируются в организме человека. Цитокины «побуждают» костный мозг создавать больше клеток крови и активно выпускать их в кровь.
На сегодняшний день считается, что применение Г-КСФ сокращает сроки восстановления кроветворения (гемопоэза) в костном мозге, снижает частоту развития инфекционных осложнений и позволяет сохранить дозоинтенсивность терапии (объем дозы и интервал между курсами), необходимую для эффективного лечения онкологических заболеваний. Снижение дозоинтенсивности ХТ приводит к сокращению общей выживаемости больных раком молочной железы и раком яичников на 37 процентов.
Согласно российским и международным исследованиям, первичная профилактика Г-КСФ достоверно уменьшает риски снижения дозоинтенсивности.
Препараты класса Г-КСФ существуют в двух формах: короткого и пролонгированого действия. Г-КСФ пролонгированного действия – это пегилированные (модифицированные в лабораторных условиях) молекулы, которые, по сути, являются усовершенствованной версией коротких Г-КСФ. Пегилированные Г-КСФ работают дольше, и их необходимо вводить всего один раз на курс химиотерапии. Это позволяет минимизировать посещения клиник, поддерживать оптимальные дозы химиотерапевтических лекарств и повышает эффективность лечения в целом.
Г-КСФ пролонгированного действия – это пегилированные (модифицированные в лабораторных условиях) молекулы, которые, по сути, являются усовершенствованной версией коротких Г-КСФ. Пегилированные Г-КСФ работают дольше, и их необходимо вводить всего один раз на курс химиотерапии. Это позволяет минимизировать посещения клиник, поддерживать оптимальные дозы химиотерапевтических лекарств и повышает эффективность лечения в целом.
В России применяются препараты Г-КСФ пролонгированного действия для снижения продолжительности нейтропении и уменьшения риска возникновения фебрильной нейтропении, такие как, например, эмпэгфилграстим.
Сегодня такие препараты входят в перечень жизненно необходимых и важнейших лекарственных препаратов. Это означает, что пациенты вправе получать их бесплатно, за счет бюджетных средств.
Cписок литературы.
Препараты на основе моноклональных антител помогают при лимфоме и раке молочной железы
National Cancer Institute / unsplash
В конце 1990-х годов исследователи создали первые в мире иммунотерапевтические препараты — моноклональные антитела к компонентам раковых клеток на основе химерных (частично мышиных, частично человеческих) антител, которые «не реагируют» на здоровые клетки организма: ритуксимаб и трастузумаб. Эти препараты применяют для лечения лимфомы и рака молочной железы.
Эти препараты применяют для лечения лимфомы и рака молочной железы.
Однако мышиные антитела живут в организме людей недолго, а еще они недостаточно эффективно проникают в опухоль и в целом работают хуже человеческих. Поэтому, чтобы эффективно бороться с человеческим раком, антитела тоже должны быть человеческими.
Проблема в том, что разработка лекарств на основе человеческих моноклональных антител — очень непростая работа. Чтобы получить антитела у мышей, нужно сначала создать «бессмертные» клетки, которые и будут «печатать» лечебный белок. Их делают путем слияния белых В-клеток с опухолевыми клетками (используют клетки миеломы, которые, как известно, не умирают). Однако клетки человеческой миеломы оказалось очень трудно культивировать в лаборатории.
Так что ученым пришлось действовать иначе — брать за основу мышиные антитела, и при помощи методов генной инженерии переделывать их, чтобы они работали в человеческом организме. Именно так создали препарат ритуксимаб. Процесс это дорогой, сложный, долгий и затратный — так что неудивительно, что готовое лекарство стоит порядка 100 долларов за десятимиллилитровую инъекцию.
Процесс это дорогой, сложный, долгий и затратный — так что неудивительно, что готовое лекарство стоит порядка 100 долларов за десятимиллилитровую инъекцию.
Ритуксимаб в России: как в нашей стране научились создавать лекарства на основе моноклональных антител
Современные биотехнологии позволили разработать новые виды лечения. Это открыло путь к таргетной терапии многих заболеваний и способствовало улучшению качества жизни пациентов. Один из ярких примеров биологического препарата направленного действия — ритуксимаб. Это лекарство изменило взгляд мировой общественности на подходы к лечению пациентов с лимфопролиферативными заболеваниями.
Наряду с оригинальными биологическими препаратами существуют биоаналоги. Биоаналогом называют биологический препарат, по параметрам безопасности, качества и эффективности схожий с оригинальным препаратом в такой же лекарственной форме и имеющий идентичный способ введения. Разработка биоаналогов — важная задача современной медицины и фармацевтики, так как позволяет обеспечить более широкое внедрение современных лекарственных препаратов в клиническую практику. И, соответственно, увеличить число успешно пролеченных пациентов.
И, соответственно, увеличить число успешно пролеченных пациентов.
В 2009–2010 годах компания ЗАО «БИОКАД» приступила к разработке и полному циклу исследований отечественного препарата ритуксимаба. Разработку проводили в рамках проекта государственного значения «Организация опытно-промышленного производства субстанций и лекарственных средств на основе моноклональных антител, необходимых для выпуска дорогостоящих импортозамещающих препаратов». Проект был утвержден Комиссией при Президенте Российской Федерации по модернизации и технологическому развитию экономики России.
Полный цикл сравнительных доклинических испытаний in vitro и in vivo завершился к середине 2011 года. В проведенных исследованиях биоаналог ритуксимаба по структуре и специфическому действию оказался идентичен оригинальному препарату «Мабтера» Ф. Хоффманн-Ля Рош, Лтд., Швейцария. Аналогичные данные получены в результате сравнительных физико-химических испытаний, а также доклинического исследования in vivo.
На следующем этапе проводились клинические испытания препарата на пациентах с лимфопролиферативными заболеваниями в сравнении с оригинальным препаратом «Мабтера». Результаты исследования свидетельствуют о том, что оба препарата одинаково воздействовали на В-лимфоциты, и не отличались по профилю безопасности и по эффективности.
На основании полученных данных биоаналог ритуксимаба производства ЗАО «БИОКАД» был зарегистрирован для медицинского применения у больных злокачественными В-клеточными лимфопролиферативными заболеваниями (рег. No ЛП-002420 от 04.04.14, код ATX: L01XC02). Новый отечественный препарат был назван «Ацеллбия». Такое название (A — Сell — B — ia) происходит от нескольких слов: A (от lat. attero) — уничтожать, ослаблять, уменьшать; Cell — клетка; B — вид клетки.
Список онкологических заболеваний, при которых применяют «Ацеллбию», велик: чаще всего препараты применяют при В-клеточных неходжкинских лимфомах, хроническом лимфолейкозе, ревматоидном артрите и гранулёматозе Вегенера.
Как мы лечим рак сегодня: открытия и достижения
За последние десятилетия XXI века ученые и врачи узнали об онкологических заболеваниях едва ли не больше, чем за все предшествующие эпохи. Лечение рака продвинулось очень далеко даже по сравнению с XX веком. Однако онкологические заболевания пока не торопятся сдавать позиции — чтобы их победить или хотя бы уверенно держать под контролем, человечеству предстоит узнать еще очень и очень много.
Все направления исследований в современной онкологии можно условно разделить на два больших направления: совершенствование старых методов и разработка новых. Одно из самых многообещающих «старых» направлений исследовательской онкологии — иммунотерапия. В XXI веке исследователи активно ищут для нее новые цели и мишени.
Современная иммунотерапия: как российские антитела помогают лечить меланому
16 апреля 2020 года Министерство здравоохранения РФ одобрило применение первого российского оригинального PD-1 ингибитора — пролголимаба. Препарат предназначен для лечения метастатической меланомы — одного из наиболее агрессивных видов рака.
Препарат предназначен для лечения метастатической меланомы — одного из наиболее агрессивных видов рака.
По данным ВОЗ, на меланому кожи приходится около 3-4 процентов всех онкологических заболеваний взрослых. Согласно прогнозам, к 2025 году число заболевших меланомой кожи в мире увеличится на 25 процентов. В нашей стране проблема стоит не менее остро, чем во всем мире. По данным справочника «Состояние онкологической помощи населению России в 2018 г.», в 19 процентах случаев у наших соотечественников меланома кожи выявлялась уже на запущенных стадиях, когда лечить ее уже очень сложно. Так что средство для лечения этого опасного заболевания более чем актуально.
У российского препарата есть аналоги за рубежом: пембролизумаб и ниволумаб. До появления отечественного ингибитора на российском рынке терапии меланомы кожи были только эти два лекарства. Пролголимаб — первый PD-1 ингибитор на основе моноклональных антител IgG1 c дополнительными модификациями его эффекторных свойств. Механизм действия ингибиторов PD-1 направлен на восстановление способности Т-лимфоцитов (иммунные клетки) распознавать и уничтожать злокачественные клетки, в результате чего иммунная система человека снова начинает бороться с опухолью.
Механизм действия ингибиторов PD-1 направлен на восстановление способности Т-лимфоцитов (иммунные клетки) распознавать и уничтожать злокачественные клетки, в результате чего иммунная система человека снова начинает бороться с опухолью.
Вакцины от рака — перспективное направление в иммунотерапии
National Cancer Institute / unsplash
Помимо моноклональных антител, в иммунотерапии есть еще одно перспективное направление — вакцины от рака. Первую вакцину от рака простаты, который не отвечает на гормональное лечение, FDA — американский аналог Минздрава и Роспотребнадзора — одобрил уже в XXI веке, в 2010 году. Это был препарат «Provenge». В отличие от привычных вакцин, лекарство не предотвращает болезнь, а помогает белым клеткам уже болеющего человека бороться с раком. К сожалению, вакцинация не излечивает рак простаты — зато помогает жить лучше и дольше.
К сожалению, вакцинация не излечивает рак простаты — зато помогает жить лучше и дольше.
Генная терапия. Новое направление, которое стало активно развиваться уже в XXI веке. Исследователи активно разрабатывают новые классы молекул, способных сражаться с раковыми клетками — например, антисмысловые олигонуклеотиды. Эти молекулы проникают в клетки и связываются с мишенью — матричной РНК (мРНК). В результате клетка прекращает создавать белки, за синтез которых отвечает ген, носители которого имеют предрасположенность к наследственным онкологическим заболеваниям. Если все получится, антисмысловые олигонуклеотиды будут просто «отключать гены рака»! Правда, к сожалению, пока не удалось зарегистрировать ни один такой препарат.
Но кое-что у нас есть и сегодня. Например, мы уже научились лечить онкогематологические заболевания при помощи T-клеток с химерными рецепторами антигена (CAR-T). Если немного упростить, то в ходе этой процедуры у пациента берут его собственные лейкоциты (конкретно — Т-клетки), и модифицируют их, вставляя в клетки ген CAR. В результате Т-клетки выращивают на поверхности специальные рецепторы CD-19, которые помогают им узнавать и уничтожать раковые клетки.
В результате Т-клетки выращивают на поверхности специальные рецепторы CD-19, которые помогают им узнавать и уничтожать раковые клетки.
В 2017-2018 годах в клиники поступило два CAR-T препарата: Kymriah от Novartis и Yescarta от Gilead. В нашей стране CAR-T-препараты разрабатывает группа под руководством Михаила Масчана. Из 46 пациентов с В-клеточным острым лимфобластным лейкозом, получивших российские CAR-T-препараты, выздоровело 40 человек. Это очень много: обычно выживаемость таких пациентов не превышает 10 процентов.
Второе направление генной терапии связано с подбором идеального лекарства. Исследователи активно ищут генные мутации, носители которых будут лучше реагировать на конкретный противораковый препарат. Это поможет сделать терапию по-настоящему индивидуальной — то есть максимально эффективной для конкретного человека, и при этом лишенной большей части побочных эффектов.
Роботизированная хирургия. Предполагается, что точный металлический робот-помощник поможет хирургам-онкологам делать идеально точные операции, которые будут одновременно малоинвазивными (по минимуму повреждающими здоровые ткани — прим. ред.) и высокоэффективными — то есть помогут убрать все до одной раковые клетки.
ред.) и высокоэффективными — то есть помогут убрать все до одной раковые клетки.
Другие направления онкологии касаются скорее диагностики, чем лечения рака. Например, нанотехнологии позволяют создать мельчайшие частицы — метки, которые будут точно показывать местонахождение опухоли.
А протеомика (наука о всех белках, которые есть в организме) поможет больше узнать о том, как ведут себя в организме разные раковые клетки. Протеомика поможет отличать агрессивные опухоли от менее агрессивных — в будущем это может помочь избавить пациента от опасного и ненужного лечения.
А еще протеомические исследования нужны, чтобы разработать новые диагностические тесты. Возможно, когда-нибудь благодаря таким тестам мы сможем «ловить» онкологические заболевания на стадии всего одной клетки. То есть тогда, когда справиться с ними совсем просто.
Даниил Давыдов
Ученые «расшифровали» раковые клетки и обещают революцию в лечении.
 Суть открытия в 100 и 500 словах
Суть открытия в 100 и 500 словах- Николай Воронин
- Корреспондент по вопросам науки
Автор фото, Science Photo Library
Международная команда ученых впервые полностью расшифровала генетическую информацию 38 видов раковых клеток, составив исчерпывающий каталог мутаций ДНК, приводящих к развитию онкологических заболеваний.
Беспрецедентное по масштабу исследование «Анализ полного генома всех видов рака» (PCAWG) заняло более 10 лет. В работе приняли участие около 1300 генетиков из 37 стран, а ее результаты были опубликованы в четверг сразу в двух десятках научных журналов.
По словам самих ученых, причины возникновения рака можно сравнить с пазлом, состоящим из 100 тысяч кусочков. До сегодняшнего дня мы пытались собрать общую картину, имея на руках лишь каждый сотый фрагмент, и лишь теперь можем взглянуть на нее целиком.
«С помощью собранной информации о происхождении и развитии опухолей мы можем разработать новые способы ранней диагностики рака, более направленные методы терапии — и лечить пациентов с большим успехом», — заявил член координационного комитета PCAWG Линкольн Стайн.
Русская служба Би-би-си коротко (в 100 словах) и чуть подробнее (в 500 словах) объясняет, в чем суть этой беспрецедентной работы и как она может произвести революцию в онкологии.
Причина любого рака — мутации в ДНК. Однако ученым мало известно о том, где именно и почему происходит поломка генетического кода, ведущая к возникновению раковой опухоли.
Участники проекта PCAWG полностью расшифровали генетическую информацию раковых клеток почти 2800 пациентов, страдающих от 38 разных видов онкологических заболеваний.
Автор фото, Getty Images
В результате было сделано несколько десятков открытий — от количества и точного расположения так называемых драйверных мутаций (то есть ведущих к развитию опухоли) до неожиданных генетических совпадений у раковых клеток различных тканей.:max_bytes(150000):strip_icc()/sorethroat-567f47103df78ccc158d7275.jpg)
В том числе выяснилось, что предрасположенность к некоторым видам рака может сформироваться за несколько десятилетий до постановки диагноза — иногда в детском возрасте.
Рак — это не одно заболевание, возникающее в разных органах, а общее название для двух сотен различных болезней, протекающих по одной и той же схеме. Одна из клеток ткани мутирует — и начинает быстро и бесконтрольно делиться, формируя опухоль.
Поломка происходит на генном уровне, но до сегодняшнего дня, пытаясь понять ее возможные причины, ученые в основном анализировали лишь «полезную ДНК» — ту часть генома, в которой закодированы белки и которая составляет лишь около 2% всей наследственной информации.
Оставшаяся часть генетического кода, известная как «мусорная ДНК», не вызывала особого интереса, поскольку заключенная в ней информация не отвечает за производство белков — строительных материалов клетки — и вообще долгое время считалась рудиментарной (то есть накопившейся в процессе эволюции, но утратившей полезные функции).
Термин «мусорная ДНК» был введен около 50 лет назад и позже признан не вполне корректным, когда обнаружилось, что некоторые фрагменты «бесполезного» генома выполняют другие важнейшие функции для поддержания жизни клетки.
Было решено расшифровать генетическую информацию раковых клеток целиком, чтобы отследить и изменения в некодирующих генах.
Автор фото, Getty Images
В результате ученые обнаружили тысячи генетических мутаций и описали более 80 процессов, ведущих к поломке генетического кода. Одни из них вызваны возрастными изменениями, другие передаются по наследству, третьи могут быть связаны с вредными привычками или диетой.
Одно из главных открытий состоит в том, что один и тот же вид рака могут вызывать абсолютно разные наборы мутаций. В клетках рака легких было обнаружено до 100 тысяч мутировавших генов, а в некоторых образцах детского рака мутации можно было пересчитать по пальцам.
«Самое удивительное открытие — это то, насколько сильно раковый геном одного пациента отличается от генома раковых клеток другого», — заявил член координационного комитета PCAWG Питер Кэмпбелл.
Однако были выявлены и неожиданные совпадения — например, одна и та же драйверная мутация может привести к развитию рака груди у женщин или рака простаты у мужчин. А значит, методы лечения, разработанные для рака груди, могут оказаться эффективными и в лечении рака простаты.
Некоторые сделанные открытия дают возможность значительно более ранней диагностики заболевания — в частности, выяснилось, что некоторые виды рака начинают формироваться на генетическом уровне задолго до развития опухоли, иногда за несколько лет или даже десятилетий.
«Это показывает, что у нас есть намного больше возможностей раннего вмешательства [в ситуацию], чем мы думали раньше», — уверяет Кэмпбелл.
Кроме того, составленный по итогам исследования каталог мутаций поможет избежать постановки неверного диагноза, что иногда случается из-за совпадения симптомов разных видов заболевания.
Однако в 5% образцов раковых клеток вообще не было выявлено драйверных мутаций — а это значит, что точное место критической поломки генетического кода еще предстоит установить.
«Если мы поймем, что происходит с нашими здоровыми органами по мере старения, что заставляет мутации накапливаться, почему некоторые клоны бесконечно размножаются, а некоторые угасают, как на этот баланс влияет образ жизни — тогда мы сможем придумать способы раннего вмешательства, чтобы предотвратить или замедлить развитие неизлечимых видов рака», — заключает профессор Кэмпбелл.
Ученые обнаружили связь между выхлопными газами и раком мозга
- Николай Воронин
- Корреспондент по вопросам науки
Автор фото, Getty Images
Ученые впервые связали риск развития рака мозга с загрязнением воздуха ультрадисперсными частицами (УДЧ). Основным источником такого загрязнения являются выхлопные газы автомобилей — в особенности работающих на дизельном топливе.
К такому выводу пришли канадские медики по результатам исследования, которое должно быть опубликовано в следующем выпуске журнала Epidemiology.
Ученые подчеркивают, что большая выборка работы (почти 2 млн человек) убедительно доказывает наличие зависимости между концентрацией УДЧ и частотой возникновения рака мозга, однако это первое подобное исследование, так что подтвердить причинно-следственную связь можно будет лишь по итогам аналогичных результатов похожих работ.
Злокачественные опухоли мозга встречаются довольно редко — примерно в 20 раз реже, чем рак груди или простаты, — однако только в России ежегодно диагностируют около 10 тысяч новых случаев.
С 2007 по 2017 год смертность от рака мозга среди россиян (статистика включает и спинной мозг) выросла почти на четверть — это самый быстрый рост среди всех онкологических заболеваний.
В группе риска — горожане
Автор фото, Getty Images
УДЧ — это твердые частицы размером менее 100 нанометров, металлические или углеродосодержащие. Именно из-за своего чрезвычайно малого размера они не просто легко вдыхаются, но и скапливаются в легких, откуда могут быть захвачены кровью и попасть в любые другие органы.
Кроме того, было доказано, что в мозг они могут проникать напрямую через обонятельный нерв и накапливаться там.
Особенно остро проблема стоит в больших городах, где с загрязнением воздуха выхлопными газами сталкивается практически каждый житель.
Канадские ученые проанализировали медицинские истории 1,9 млн жителей двух крупнейших мегаполисов страны, Торонто и Монреаля. За 15 лет (1991-2016 гг.) рак мозга был диагностирован у 1400 пациентов.
Исследовав уровень загрязнения воздуха в разных районах, авторы исследования сравнили их с частотой возникновения злокачественных опухолей у местных жителей. Учитывалась концентрация не только УДЧ, но и более крупных частиц (размером до 2,5 мкм), а также диоксида азота (NO2).
Автор фото, Getty Images
Именно последние два компонента считаются наиболее опасными для здоровья загрязнителями, однако их содержание в воздухе оказалось никак не связано с риском развития в мозгу злокачественной опухоли.
А вот по мере увеличения концентрации УДЧ росли и показатели заболеваемости.
Жители районов со средним уровнем загрязнения (50 тысяч частиц/см3) заболевали раком мозга в полтора раза чаще, чем те, что жили в более чистых от выхлопных газов кварталах (15 тысяч/см3). У обитателей самых загрязненных районов (97 тысяч/см3) заболевание диагностировали почти в 2,3 раза чаще.
Авторы исследования ожидают, что аналогичные результаты будут получены и в других городах с высоким уровнем загрязнения выхлопными газами, поскольку «известно, что УДЧ проникают в человеческий мозг, а в группе риска находятся жители городских регионов по всему миру».
В Москве, например, по данным департамента природопользования и охраны окружающей среды, 90% загрязнений воздуха приходится на автомобили.
Ученые выяснили, когда на Земле появилась самая страшная болезнь
https://ria.ru/20190609/1555363411.html
Ученые выяснили, когда на Земле появилась самая страшная болезнь
Ученые выяснили, когда на Земле появилась самая страшная болезнь
Рак долгое время считали болезнью современности, но в начале XXI века его следы обнаружили у древнеегипетских мумий, неандертальцев и даже на костях динозавров. .. РИА Новости, 09.06.2019
.. РИА Новости, 09.06.2019
2019-06-09T08:00
2019-06-09T08:00
2019-06-09T08:00
неандертальцы
динозавры
рак
москва
германия
наука
/html/head/meta[@name=’og:title’]/@content
/html/head/meta[@name=’og:description’]/@content
https://cdn23.img.ria.ru/images/155537/83/1555378353_0:68:2600:1531_1920x0_80_0_0_7b14d826cc6b69dc4d9b9c837e90c418.jpg
МОСКВА, 9 июн — РИА Новости, Альфия Еникеева. Рак долгое время считали болезнью современности, но в начале XXI века его следы обнаружили у древнеегипетских мумий, неандертальцев и даже на костях динозавров и звероящеров. Похоже, что разного рода опухоли сопровождали многоклеточную жизнь с момента ее возникновения на планете. Болезнь скифского царяВ 2001 году в тувинской «долине царей» российские археологи раскопали скифское захоронение мужчины и женщины возрастом более двух с половиной тысячелетий. Там было более двадцати килограммов золота, что указывает на высокий социальный статус погребенных. Прошло шесть лет, прежде чем специалисты обратили внимание на микроскопические темные точки, покрывающие почти весь мужской скелет. Тщательный анализ костей показал, что это следы метастазов — раковых клеток, оторвавшихся от первичной злокачественной опухоли и образовавших в разных частях организма вторичные очаги болезни. То есть этот скифский царь скончался от какого-то онкологического недуга. Сравнив полученные данные с современными образцами клеток, ученые установили, что это был рак простаты.Опухоль возрастом в 1,7 миллиона летСледы злокачественных опухолей и метастазов находили у египетских мумий, погребенных 2250 лет назад, южноамериканских инков, древних римлян и средневековых англичан. В 2013 году американские палеонтологи выявили рак кости на ребре неандертальца, найденном в хорватской пещере Крапина. Его возраст примерно 120 тысяч лет. По мнению ученых, опухоль возникла в результате редкого заболевания — фиброзной дисплазии, вызванной поломкой в гене ACVR1. Значит, рак носил наследственный характер, и вполне вероятно, что загрязнение окружающей среды — не самая главная причина нынешнего распространения онкологических болезней, отмечают авторы исследования.
Прошло шесть лет, прежде чем специалисты обратили внимание на микроскопические темные точки, покрывающие почти весь мужской скелет. Тщательный анализ костей показал, что это следы метастазов — раковых клеток, оторвавшихся от первичной злокачественной опухоли и образовавших в разных частях организма вторичные очаги болезни. То есть этот скифский царь скончался от какого-то онкологического недуга. Сравнив полученные данные с современными образцами клеток, ученые установили, что это был рак простаты.Опухоль возрастом в 1,7 миллиона летСледы злокачественных опухолей и метастазов находили у египетских мумий, погребенных 2250 лет назад, южноамериканских инков, древних римлян и средневековых англичан. В 2013 году американские палеонтологи выявили рак кости на ребре неандертальца, найденном в хорватской пещере Крапина. Его возраст примерно 120 тысяч лет. По мнению ученых, опухоль возникла в результате редкого заболевания — фиброзной дисплазии, вызванной поломкой в гене ACVR1. Значит, рак носил наследственный характер, и вполне вероятно, что загрязнение окружающей среды — не самая главная причина нынешнего распространения онкологических болезней, отмечают авторы исследования. Такой же точки зрения придерживаются британские и африканские ученые, обнаружившие в 2016 году в пещере Сварткранс (ЮАР) следы самого древнего на данный момент человеческого рака — остеосаркомы. Она поразила стопу и пальцы ног австралопитека седиба — одного из предполагаемых предков Homo sapiens, жившего около 1,7 миллиона лет назад. Неизвестно, что стало причиной гибели этого существа, но опухоль кости, скорее всего, мешала ему нормально передвигаться.Болезни мезозояАмериканские палеонтологи, за несколько лет обследовавшие более десяти тысяч позвонков динозавров из семисот музейных образцов, нашли признаки онкологических заболеваний почти у сотни утконосых динозавров — гадрозавров, живших в меловой период, примерно 70 миллионов лет назад. Следы злокачественной опухоли заметили на костях черепахи Pappochelys rosinae, обитавшей 240 миллионов лет назад. Ее скелет извлекли из отложений раннего триасового периода на юге Германии. Сканирование показало, что страдала остеосаркомой, возникшей из-за «бунта» взрослых стволовых клеток в надкостнице.
Такой же точки зрения придерживаются британские и африканские ученые, обнаружившие в 2016 году в пещере Сварткранс (ЮАР) следы самого древнего на данный момент человеческого рака — остеосаркомы. Она поразила стопу и пальцы ног австралопитека седиба — одного из предполагаемых предков Homo sapiens, жившего около 1,7 миллиона лет назад. Неизвестно, что стало причиной гибели этого существа, но опухоль кости, скорее всего, мешала ему нормально передвигаться.Болезни мезозояАмериканские палеонтологи, за несколько лет обследовавшие более десяти тысяч позвонков динозавров из семисот музейных образцов, нашли признаки онкологических заболеваний почти у сотни утконосых динозавров — гадрозавров, живших в меловой период, примерно 70 миллионов лет назад. Следы злокачественной опухоли заметили на костях черепахи Pappochelys rosinae, обитавшей 240 миллионов лет назад. Ее скелет извлекли из отложений раннего триасового периода на юге Германии. Сканирование показало, что страдала остеосаркомой, возникшей из-за «бунта» взрослых стволовых клеток в надкостнице. Такие опухоли сегодня чаще всего поражают молодых людей — это один из самых распространенных видов рака костей у человека и домашних животных. Самый древний на сегодняшний день рак диагностировали палеонтологи из Университета Вашингтона в Сиэтле (США). Пытаясь понять, как у млекопитающих появились зубы, они исследовали черепа горгонопсов — саблезубых звероящеров, обитавших 255 миллионов лет назад, в самом конце палеозойской эры. Чтобы узнать, каким образом зубы горгонопсов крепились к черепу, исследователи разрезали одну из челюстей на мелкие части и увидели на корнях саблезубых клыков древнего хищника необычные костяные пузырьки неправильной формы. Это были одонтомы — доброкачественные опухоли зубной ткани. Подобные образования нередко возникают в деснах и на зубах человека, обычно безболезненные, они не мешают челюсти нормально работать. Однако их наличие указывает на возможность злокачественных проявлений в дальнейшем. Не исключено, что разного рода опухоли сопровождали многоклеточную жизнь фактически с момента ее возникновения на планете, заключают авторы статьи.
Такие опухоли сегодня чаще всего поражают молодых людей — это один из самых распространенных видов рака костей у человека и домашних животных. Самый древний на сегодняшний день рак диагностировали палеонтологи из Университета Вашингтона в Сиэтле (США). Пытаясь понять, как у млекопитающих появились зубы, они исследовали черепа горгонопсов — саблезубых звероящеров, обитавших 255 миллионов лет назад, в самом конце палеозойской эры. Чтобы узнать, каким образом зубы горгонопсов крепились к черепу, исследователи разрезали одну из челюстей на мелкие части и увидели на корнях саблезубых клыков древнего хищника необычные костяные пузырьки неправильной формы. Это были одонтомы — доброкачественные опухоли зубной ткани. Подобные образования нередко возникают в деснах и на зубах человека, обычно безболезненные, они не мешают челюсти нормально работать. Однако их наличие указывает на возможность злокачественных проявлений в дальнейшем. Не исключено, что разного рода опухоли сопровождали многоклеточную жизнь фактически с момента ее возникновения на планете, заключают авторы статьи.
https://sn.ria.ru/20130606/941716586.html
https://ria.ru/20161208/1483162285.html
москва
германия
РИА Новости
internet-group@rian.ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
2019
РИА Новости
internet-group@rian.ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
Новости
ru-RU
https://ria.ru/docs/about/copyright.html
https://xn--c1acbl2abdlkab1og.xn--p1ai/
РИА Новости
internet-group@rian.ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
https://cdn25.img.ria.ru/images/155537/83/1555378353_149:0:2460:1733_1920x0_80_0_0_bda058e491e43d045edef2f937c8811b.jpgРИА Новости
internet-group@rian.ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og. xn--p1ai/awards/
xn--p1ai/awards/
РИА Новости
internet-group@rian.ru
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
неандертальцы, динозавры, рак, москва, германия
МОСКВА, 9 июн — РИА Новости, Альфия Еникеева. Рак долгое время считали болезнью современности, но в начале XXI века его следы обнаружили у древнеегипетских мумий, неандертальцев и даже на костях динозавров и звероящеров. Похоже, что разного рода опухоли сопровождали многоклеточную жизнь с момента ее возникновения на планете.Болезнь скифского царя
В 2001 году в тувинской «долине царей» российские археологи раскопали скифское захоронение мужчины и женщины возрастом более двух с половиной тысячелетий. Там было более двадцати килограммов золота, что указывает на высокий социальный статус погребенных.
Прошло шесть лет, прежде чем специалисты обратили внимание на микроскопические темные точки, покрывающие почти весь мужской скелет. Тщательный анализ костей показал, что это следы метастазов — раковых клеток, оторвавшихся от первичной злокачественной опухоли и образовавших в разных частях организма вторичные очаги болезни. То есть этот скифский царь скончался от какого-то онкологического недуга. Сравнив полученные данные с современными образцами клеток, ученые установили, что это был рак простаты.6 июня 2013, 09:06НаукаНеандертальцы тоже страдали от раковых опухолей, выяснили ученыеКак полагают ученые, распространение рака сегодня связано не с ухудшением экологии, а со значительным увеличением средней продолжительности жизни.
Тщательный анализ костей показал, что это следы метастазов — раковых клеток, оторвавшихся от первичной злокачественной опухоли и образовавших в разных частях организма вторичные очаги болезни. То есть этот скифский царь скончался от какого-то онкологического недуга. Сравнив полученные данные с современными образцами клеток, ученые установили, что это был рак простаты.6 июня 2013, 09:06НаукаНеандертальцы тоже страдали от раковых опухолей, выяснили ученыеКак полагают ученые, распространение рака сегодня связано не с ухудшением экологии, а со значительным увеличением средней продолжительности жизни.Опухоль возрастом в 1,7 миллиона лет
Следы злокачественных опухолей и метастазов находили у египетских мумий, погребенных 2250 лет назад, южноамериканских инков, древних римлян и средневековых англичан. В 2013 году американские палеонтологи выявили рак кости на ребре неандертальца, найденном в хорватской пещере Крапина. Его возраст примерно 120 тысяч лет. По мнению ученых, опухоль возникла в результате редкого заболевания — фиброзной дисплазии, вызванной поломкой в гене ACVR1. Значит, рак носил наследственный характер, и вполне вероятно, что загрязнение окружающей среды — не самая главная причина нынешнего распространения онкологических болезней, отмечают авторы исследования.Такой же точки зрения придерживаются британские и африканские ученые, обнаружившие в 2016 году в пещере Сварткранс (ЮАР) следы самого древнего на данный момент человеческого рака — остеосаркомы. Она поразила стопу и пальцы ног австралопитека седиба — одного из предполагаемых предков Homo sapiens, жившего около 1,7 миллиона лет назад. Неизвестно, что стало причиной гибели этого существа, но опухоль кости, скорее всего, мешала ему нормально передвигаться.
Значит, рак носил наследственный характер, и вполне вероятно, что загрязнение окружающей среды — не самая главная причина нынешнего распространения онкологических болезней, отмечают авторы исследования.Такой же точки зрения придерживаются британские и африканские ученые, обнаружившие в 2016 году в пещере Сварткранс (ЮАР) следы самого древнего на данный момент человеческого рака — остеосаркомы. Она поразила стопу и пальцы ног австралопитека седиба — одного из предполагаемых предков Homo sapiens, жившего около 1,7 миллиона лет назад. Неизвестно, что стало причиной гибели этого существа, но опухоль кости, скорее всего, мешала ему нормально передвигаться.Болезни мезозоя
Американские палеонтологи, за несколько лет обследовавшие более десяти тысяч позвонков динозавров из семисот музейных образцов, нашли признаки онкологических заболеваний почти у сотни утконосых динозавров — гадрозавров, живших в меловой период, примерно 70 миллионов лет назад. Следы злокачественной опухоли заметили на костях черепахи Pappochelys rosinae, обитавшей 240 миллионов лет назад. Ее скелет извлекли из отложений раннего триасового периода на юге Германии.
Ее скелет извлекли из отложений раннего триасового периода на юге Германии.Сканирование показало, что страдала остеосаркомой, возникшей из-за «бунта» взрослых стволовых клеток в надкостнице. Такие опухоли сегодня чаще всего поражают молодых людей — это один из самых распространенных видов рака костей у человека и домашних животных.
Самый древний на сегодняшний день рак диагностировали палеонтологи из Университета Вашингтона в Сиэтле (США). Пытаясь понять, как у млекопитающих появились зубы, они исследовали черепа горгонопсов — саблезубых звероящеров, обитавших 255 миллионов лет назад, в самом конце палеозойской эры.Чтобы узнать, каким образом зубы горгонопсов крепились к черепу, исследователи разрезали одну из челюстей на мелкие части и увидели на корнях саблезубых клыков древнего хищника необычные костяные пузырьки неправильной формы. Это были одонтомы — доброкачественные опухоли зубной ткани.
Подобные образования нередко возникают в деснах и на зубах человека, обычно безболезненные, они не мешают челюсти нормально работать.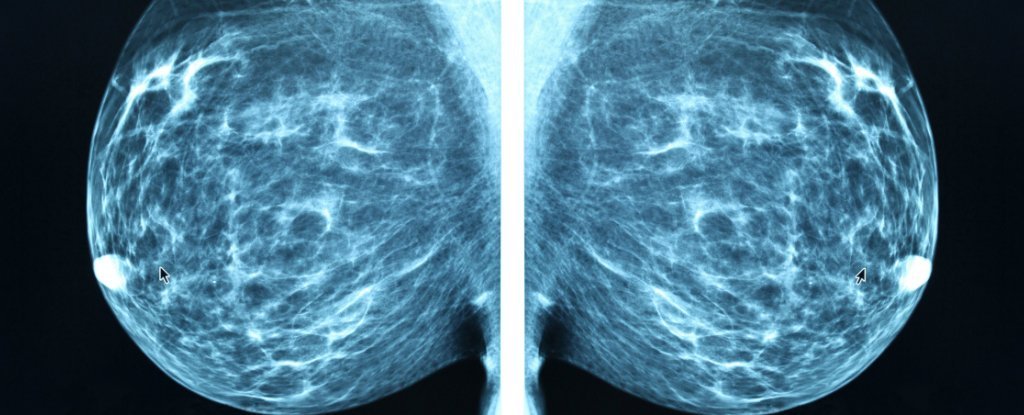 Однако их наличие указывает на возможность злокачественных проявлений в дальнейшем. Не исключено, что разного рода опухоли сопровождали многоклеточную жизнь фактически с момента ее возникновения на планете, заключают авторы статьи.
Однако их наличие указывает на возможность злокачественных проявлений в дальнейшем. Не исключено, что разного рода опухоли сопровождали многоклеточную жизнь фактически с момента ее возникновения на планете, заключают авторы статьи.
История и открытие рака
Вы когда-нибудь задумывались, когда впервые был обнаружен рак? Когда мы слышим о некоторых причинах рака, может показаться, что рак — недавняя болезнь. Тем не менее, мы узнали, что рак поражал людей на протяжении веков и еще с письменного слова. Давайте посмотрим на то, что мы знаем об истории рака, и на то, как идеи причинно-следственной связи и лечения менялись с течением времени.
Дэн Китвуд / Getty ImagesПроисхождение слова «рак»
Слово «рак» произошло от отца медицины: Гиппократа, греческого врача. Гиппократ использовал греческие слова carcinos и carcinoma для описания опухолей, таким образом назвав рак «karkinos». Греческие термины на самом деле были словами, которые использовались для описания краба, которого Гиппократ считал опухолью. Хотя Гиппократ, возможно, назвал болезнь «раком», он определенно не был первым, кто ее открыл. История рака на самом деле начинается намного раньше.
Гиппократ использовал греческие слова carcinos и carcinoma для описания опухолей, таким образом назвав рак «karkinos». Греческие термины на самом деле были словами, которые использовались для описания краба, которого Гиппократ считал опухолью. Хотя Гиппократ, возможно, назвал болезнь «раком», он определенно не был первым, кто ее открыл. История рака на самом деле начинается намного раньше.
Первый задокументированный случай рака
Самый старый задокументированный случай рака произошел в Древнем Египте в 1500 году до нашей эры.Подробности были записаны на папирусе, документально зафиксировав восемь случаев опухолей груди. Его лечили прижиганием, которое разрушало ткани горячим инструментом, называемым «пожарная дрель». Также было зафиксировано отсутствие лечения болезни, только паллиативное лечение.
Есть свидетельства того, что древние египтяне могли различать злокачественные и доброкачественные опухоли. Согласно надписям, поверхностные опухоли удаляли хирургическим путем так же, как и сегодня.
То, что, по мнению ранних врачей, было причиной рака
Конечно, в Древней Греции о человеческом теле было известно гораздо меньше, чем то, что известно сегодня. Например, Гиппократ считал, что тело состоит из четырех жидкостей: крови, мокроты, желтой желчи и черной желчи. Он считал, что избыток черной желчи в каком-либо участке тела вызывает рак. Это было общей мыслью о причине рака в течение следующих 1400 лет. В Древнем Египте считалось, что рак вызван Богами.
Рождение патологического вскрытия
Вскрытие, проведенное Уильямом Харви в 1628 году, открыло путь к большему изучению анатомии и физиологии человека. Было обнаружено кровообращение, что открыло двери для новых исследований болезней. Только в 1761 году было проведено вскрытие, чтобы выяснить причину смерти больных. Джованни Морганьи из Падуи был первым, кто провел такие вскрытия.
Другие теории о причинах рака
Теория лимфы разработана в 17 веке, заменив теорию черной желчи Гиппократа о причине рака.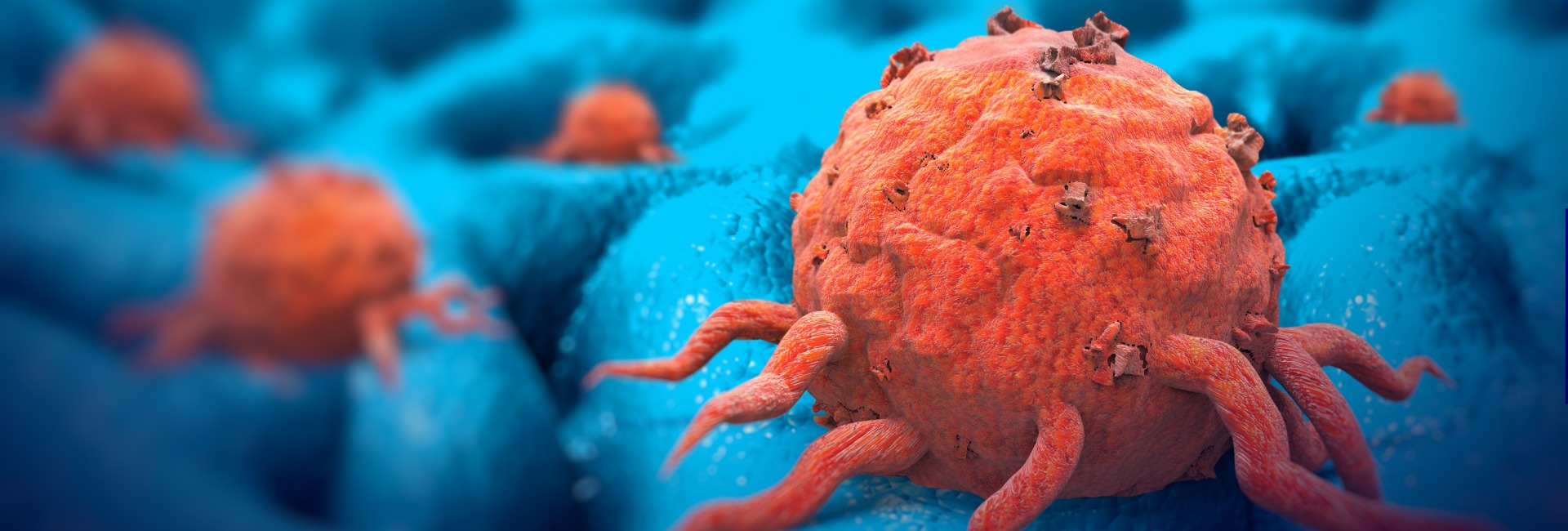 Открытие лимфатической системы дало новое понимание того, что может вызывать рак. Считалось, что причиной этого были аномалии лимфатической системы.
Открытие лимфатической системы дало новое понимание того, что может вызывать рак. Считалось, что причиной этого были аномалии лимфатической системы.
Только в конце 19 века Рудольф Вирхов осознал, что клетки, даже раковые клетки, происходят из других клеток. Появились и другие теории, например, рак, вызванный травмой, паразитами, и считалось, что рак может распространяться ». как жидкость «. Позже немецкий хирург Карл Тирш пришел к выводу, что рак распространяется через злокачественные клетки.В 1926 году за открытие причины рака желудка — червя — была незаконно присуждена Нобелевская премия. В 20 веке были отмечены наибольшие успехи в исследованиях рака. Были обнаружены исследования по выявлению канцерогенов, химиотерапии, лучевой терапии и более эффективных средств диагностики.
Сегодня мы можем лечить некоторые виды рака, и исследования продолжаются. Клинические испытания и научные исследования — ключ к поиску лекарства или окончательного метода профилактики.
История рака
Изучение рака называется онкологией. Раки известны человечеству с давних времен. Рак начинается, когда клетки в какой-либо части тела начинают бесконтрольно расти. Несколько различных частей тела могут быть поражены раком.
Раки известны человечеству с давних времен. Рак начинается, когда клетки в какой-либо части тела начинают бесконтрольно расти. Несколько различных частей тела могут быть поражены раком.
Самые ранние упоминания о раке
Некоторые из самых ранних свидетельств рака обнаружены среди окаменелых опухолей костей у человеческих мумий в Древнем Египте, и упоминания о них были найдены в древних рукописях. Также было обнаружено разрушение костного черепа, наблюдаемое при раке головы и шеи.
Хотя слово «рак» не использовалось, самое старое описание болезни относится к Египту и датируется примерно 3000 годом до нашей эры. Он называется Папирус Эдвина Смита и является копией части древнеегипетского учебника по хирургии травм. В нем описывается 8 случаев опухолей или язв груди, которые лечили путем прижигания с помощью инструмента, называемого пожарной дрелью. В описании добавлено, что это состояние не лечится.
Происхождение слова рак
Болезнь была впервые названа раком греческим врачом Гиппократом (460–370 до н. э.).Его считают «отцом медицины». Гиппократ использовал термины карциноз и карцинома для описания не язвенных и язвенных опухолей. По-гречески это означает краб. Это описание было названо в честь краба, потому что похожие на пальцы выступы рака напоминали форму краба.
э.).Его считают «отцом медицины». Гиппократ использовал термины карциноз и карцинома для описания не язвенных и язвенных опухолей. По-гречески это означает краб. Это описание было названо в честь краба, потому что похожие на пальцы выступы рака напоминали форму краба.
Поздний римский врач Цельс (28-50 до н.э.) перевел греческий термин на рак, латинское слово, обозначающее краб. Еще один римский врач Гален (130-200 г. н.э.) использовал термин oncos (греч. Отек) для описания опухолей.Онкос — это корневое слово для обозначения онкологии или изучения рака.
Между 15 и 18 веками
В начале 15 века ученые стали лучше понимать работу человеческого тела и его патологические процессы.
Вскрытие, проведенное Харви (1628 г.), привело к пониманию циркуляции крови в сердце и теле.
Джованни Морганьи из Падуи в 1761 году систематизировал вскрытие трупов, чтобы найти причину болезней. Это также положило начало изучению рака.
Шотландский хирург Джон Хантер (1728–1793) предположил, что некоторые виды рака можно вылечить хирургическим путем. Почти столетие спустя развитие анестезии побудило к регулярным операциям по поводу «подвижного» рака, который не распространился на другие органы.
Почти столетие спустя развитие анестезии побудило к регулярным операциям по поводу «подвижного» рака, который не распространился на другие органы.
XIX век
Рудольф Вирхов, которого часто называют основоположником клеточной патологии, заложил основу для патологического изучения рака под микроскопом. Вирхов соотносил микроскопическую патологию с болезнью.
Он также разработал исследование тканей, которые были удалены после операции. Патологоанатом также мог сказать хирургу, полностью ли удалось удалить рак.
История причин рака
На протяжении веков существовало множество теорий причин рака. Например, древние египтяне обвиняли богов в возникновении рака.
- Гиппократ считал, что в теле есть 4 жидкости (биологические жидкости): кровь, мокрота, желтая желчь и черная желчь.Он предположил, что дисбаланс этих жидкостей с избытком черной желчи в различных частях тела может вызвать рак. Это была гуморальная теория.
- После гуморальной теории появилась лимфатическая теория.
 Шталь и Хоффман предположили, что рак состоит из ферментирующей и дегенерирующей лимфы, различающейся по плотности, кислотности и щелочности. Джон Хантер, шотландский хирург 1700-х годов, согласился с тем, что опухоли растут из лимфы, постоянно выделяемой из крови.
Шталь и Хоффман предположили, что рак состоит из ферментирующей и дегенерирующей лимфы, различающейся по плотности, кислотности и щелочности. Джон Хантер, шотландский хирург 1700-х годов, согласился с тем, что опухоли растут из лимфы, постоянно выделяемой из крови. - Закут Лузитани (1575–1642) и Николас Тулп (1593–1674), врачи из Голландии, пришли к выводу, что рак заразен.На протяжении 17-18 веков некоторые считали, что рак заразен.
- В 1838 году немецкий патолог Йоханнес Мюллер показал, что рак состоит из клеток, а не лимфы. Мюллер предположил, что раковые клетки развиваются из почкующихся элементов (бластемы) между нормальными тканями.
- Рудольф Вирхов (1821–1902) предположил, что все клетки, включая раковые, происходят из других клеток. Он предложил теорию хронического раздражения. Он считал, что рак распространяется жидкостью.В 1860-х годах немецкий хирург Карл Тирш показал, что рак метастазирует через распространение злокачественных клеток, а не через жидкость.

- До 1920-х годов считалось, что причиной рака является травма.
История скрининга и выявления рака
Скрининг на рак помогает в раннем выявлении. Первым скрининговым тестом, который стал широко использоваться для выявления рака, был Пап-тест. Он был разработан Джорджем Папаниколау как метод исследования менструального цикла.Затем он отметил, что этот тест может помочь в раннем обнаружении рака шейки матки, и представил свои результаты в 1923 году.
Именно тогда Американское онкологическое общество (ACS) продвигало этот тест в начале 1960-х годов, и он стал широко использоваться в качестве инструмента скрининга.
Современные методы маммографии были разработаны в конце 1960-х годов и впервые официально рекомендованы ACS для выявления рака груди в 1976 году.
Развитие онкологической хирургии
Это было довольно рано в истории изучения рака, когда хирургия считалась методом лечения рака.Римский врач Цельс заметил, что, несмотря на операцию, рак, похоже, возвращается. Гален писал о методах хирургии рака. Хирургия тогда была очень примитивной, со многими осложнениями, включая потерю крови. Хирургия рака процветала в 19 и начале 20 веков после развития анестезии.
Гален писал о методах хирургии рака. Хирургия тогда была очень примитивной, со многими осложнениями, включая потерю крови. Хирургия рака процветала в 19 и начале 20 веков после развития анестезии.
Bilroth в Германии, Handley в Лондоне и Halsted в Балтиморе — пионеры хирургии рака. Уильям Стюарт Халстед, профессор хирургии Университета Джона Хопкинса, разработал радикальную мастэктомию в последнее десятилетие 19 века для лечения рака груди.Его работа была основана на В. Сэмпсоне Хэндли.
Стивен Пэджет, английский хирург того времени, обнаружил, что рак действительно распространяется через кровообращение. Это понимание метастазов стало ключевым элементом в распознавании пациентов, которым может помочь хирургия рака, а кому нет.
Разработка лучевой терапии
В 1896 году немецкий профессор физики Вильгельм Конрад Рентген открыл и представил свойства рентгеновских лучей. В течение следующих нескольких месяцев рентгеновские лучи стали использоваться для диагностики, а в следующие 3 года они стали применяться при лечении рака. Лучевая терапия началась с применения радия и относительно низковольтных диагностических аппаратов.
Лучевая терапия началась с применения радия и относительно низковольтных диагностических аппаратов.
Разработка химиотерапии
Было замечено, что во время Второй мировой войны солдаты, подвергшиеся действию горчичного газа во время военных действий, развили токсическое подавление костного мозга. Вскоре было обнаружено, что похожий химический азотный иприт действует против рака лимфатических узлов, называемого лимфомой. Это заложило основу для нескольких новых лекарств, которые можно было бы использовать против рака.
Разработка гормональной терапии
В 19 веке Томас Битсон обнаружил, что грудь кроликов перестала давать молоко после того, как он удалил яичники.Он пробовал удаление яичников (так называемая овариэктомия) при запущенном раке груди. Это было обнаружено до открытия самого гормона. Его работа заложила основу для современного использования гормональной терапии, такой как тамоксифен и ингибиторы ароматазы, для лечения или предотвращения рака груди.
Развитие иммунотерапии
С пониманием биологии раковых клеток было разработано несколько биологических агентов для лечения рака. Это называется терапией с использованием модификатора биологического ответа (BRM).Среди них следует отметить моноклональные антитела.
Первые терапевтические моноклональные антитела, ритуксимаб (Ритуксан) и трастузумаб (Герцептин), были одобрены в конце 1990-х годов для лечения лимфомы и рака груди соответственно. Ученые также изучают вакцины, которые усиливают иммунный ответ организма на раковые клетки.
Во второй половине 20-го века также были разработаны таргетные методы лечения, такие как ингибиторы факторов роста, такие как трастузумаб (Герцептин), гефитиниб (Иресса), иматиниб (Гливек) и цетуксимаб (Эрбитукс).Другой целевой подход — это препараты против нгиогенеза или образования кровеносных сосудов, такие как бевацизумаб (Авастин).
Дополнительная литература
Как давно мы страдаем от рака?
Как давно мы страдаем от рака?
13 августа 2012 г.
Написано приглашенным блоггером и канарским стажером Эбби Либерман, которая исследовала и написала эту краткую историю.
Хотя в последние десятилетия наблюдается резкий рост заболеваемости раком, на самом деле рак поражает людей на протяжении веков.Первый задокументированный случай рака произошел в Древнем Египте. По данным Американского онкологического общества, восемь задокументированных случаев рака груди обнаружены на папирусе, датируемом 3000 годом до нашей эры. Даже термин «рак» существует на протяжении веков — Гиппократ, греческий врач, которого многие считают отцом медицины, использовал слова carcinos и карцинома для описания опухолей. Эти греческие термины также использовались для описания краба, потому что Гиппократ думал, что опухоли напоминают крабов.
Два изображения Клары Якоби, голландки, у которой в 1689 году удалили опухоль из шеи
. Включает текст, описывающий опухоль и ее удаление.
Несмотря на свою долгую историю, рак часто считается современным заболеванием, потому что его влияние на современное общество гораздо более существенно, чем на прежние люди. В статье Стива Шапина Cancer World он выражает свое мнение о том, что «рост смертности от рака — это в своем роде очень хорошая новость.«Хотя это заявление может показаться тревожным, в нем есть сильная сторона. Одна из причин, по которой рак стал основной причиной смерти в Соединенных Штатах, заключается в том, что мы живем намного дольше, чем раньше. Как общество, мы более защищены от обширных инфекционных заболеваний; мы живем достаточно долго, чтобы рак проявил себя. Шапин прослеживает нашу современную борьбу с раком с 1971 года, когда президент Никсон объявил войну раку. Несмотря на то, что Соединенным Штатам (или любой другой стране) еще предстоит выиграть «войну», эти политические усилия действительно укрепили национальные усилия по борьбе с раком.
Насколько нам известно, люди борются с раком. Древние египтяне заключили еще в 1600 году до нашей эры. что болезнь «не лечится». Хотя нам еще предстоит найти лекарство от рака, общество добилось больших успехов в лечении. В то время как в прошлом общества могли пытаться лечить только раковые образования, видимые на поверхности тела, сегодня Canary Foundation работает над технологией, которая позволит врачам обнаруживать, устранять или лечить опухоли размером с чернику! Хотя есть еще путь к борьбе с раком, прогресс, достигнутый даже за последние 50 лет, впечатляет.Благодаря достижениям в области исследований и технологий ранней диагностики, Canary Foundation стремится вывести лечение рака на совершенно новый уровень. Благодаря борьбе с заболеванием на самых ранних стадиях, инвазивное лечение на более поздних стадиях больше не потребуется. Это просто вопрос времени, когда исследователи найдут способ предотвратить рак так же, как ученые нашли способы ограничить основные причины смерти на протяжении всей истории.
Древние египтяне заключили еще в 1600 году до нашей эры. что болезнь «не лечится». Хотя нам еще предстоит найти лекарство от рака, общество добилось больших успехов в лечении. В то время как в прошлом общества могли пытаться лечить только раковые образования, видимые на поверхности тела, сегодня Canary Foundation работает над технологией, которая позволит врачам обнаруживать, устранять или лечить опухоли размером с чернику! Хотя есть еще путь к борьбе с раком, прогресс, достигнутый даже за последние 50 лет, впечатляет.Благодаря достижениям в области исследований и технологий ранней диагностики, Canary Foundation стремится вывести лечение рака на совершенно новый уровень. Благодаря борьбе с заболеванием на самых ранних стадиях, инвазивное лечение на более поздних стадиях больше не потребуется. Это просто вопрос времени, когда исследователи найдут способ предотвратить рак так же, как ученые нашли способы ограничить основные причины смерти на протяжении всей истории.
Автор этого блога Abbie Lieberman , Development Intern.
вех в области исследований и открытий рака
За последние 250 лет мы стали свидетелями многих знаменательных открытий в наших усилиях по борьбе с раком, заболеванием, известным человечеству на протяжении тысячелетий. На этой временной шкале показаны несколько ключевых вех в истории исследований рака.
1775: Сажистый и плоскоклеточный рак дымоходов
Персивалл Потт определяет взаимосвязь между воздействием дымовой сажи и заболеваемостью плоскоклеточным раком мошонки среди трубочистов.Его доклад является первым, в котором четко говорится о связи воздействия окружающей среды с развитием рака.
1863: Воспаление и рак
Рудольф Вирхов определяет белые кровяные тельца (лейкоциты) в раковой ткани, устанавливая первую связь между воспалением и раком. Вирхов также ввел термин «лейкемия» и стал первым человеком, описавшим избыточное количество лейкоцитов в крови пациентов с этим заболеванием.
1882: Первая радикальная мастэктомия для лечения рака груди
Уильям Халстед выполняет первую радикальную мастэктомию для лечения рака груди.Эта хирургическая процедура остается стандартной операцией при раке груди до второй половины 20 века.
1886: Наследование риска рака
Бразильский офтальмолог Хилариу де Гувеа представляет первое документальное свидетельство того, что предрасположенность к раку может передаваться по наследству от родителя к ребенку. Он сообщает, что двое из семи детей, рожденных от отца, который успешно лечился от детской ретинобластомы, злокачественной опухоли глаза, также заболели этой болезнью.
1895: Первый рентгеновский снимок
Вильгельм Рентген открывает рентгеновские лучи. Первый рентгеновский снимок — это изображение руки его жены.
1898: Радий и полоний
Мари и Пьер Кюри открывают радиоактивные элементы радий и полоний. Через несколько лет начинается использование радия для лечения рака.
Через несколько лет начинается использование радия для лечения рака.
1902: Раковые опухоли и одиночные клетки с хромосомным повреждением
Теодор Бовери предполагает, что раковые опухоли возникают из отдельных клеток, которые испытали повреждение хромосом, и предполагает, что изменения хромосом вызывают неконтролируемое деление клеток.
1903: Первое применение лучевой терапии для лечения рака
S.W. Голдберг и Ефим Лондон описывают использование радия для лечения двух пациентов с базальноклеточным раком кожи. У обоих пациентов болезнь была ликвидирована.
1909: иммунный надзор
Пауль Эрлих предполагает, что иммунная система обычно подавляет образование опухолей, и эта концепция стала известна как гипотеза «иммунного надзора». Это предложение побуждает к исследованиям, которые продолжаются и сегодня, чтобы использовать силу иммунной системы для борьбы с раком.
1911: рак у кур
Пейтон Раус обнаружил вирус, вызывающий рак у кур (вирус саркомы Рауса), установив, что некоторые виды рака вызываются инфекционными агентами.
1915: рак у кроликов
Кацусабуро Ямагива и Коичи Итикава вызывают рак у кроликов, нанося каменноугольную смолу на их кожу, обеспечивая экспериментальное доказательство того, что химические вещества могут вызывать рак.
1928: Мазок Папаниколау
Джордж Папаниколау обнаруживает, что рак шейки матки можно обнаружить, исследуя клетки влагалища под микроскопом.Этот прорыв приводит к разработке Пап-теста, который позволяет обнаруживать и удалять аномальные клетки шейки матки до того, как они станут злокачественными.
1932: Модифицированная радикальная мастэктомия при раке груди
Дэвид Х. Пейти разрабатывает модифицированную радикальную мастэктомию при раке груди. Эта хирургическая процедура менее уродлива, чем радикальная мастэктомия, и в конечном итоге заменяет ее в качестве стандартного хирургического лечения рака груди.
1937: Национальный институт рака (NCI)
Закон подписан президентом Франклином Д. Рузвельт основывает Национальный институт рака (NCI).
Рузвельт основывает Национальный институт рака (NCI).
1937: Операция по сохранению груди с последующим облучением
Сэр Джеффри Кейнс описывает лечение рака груди с помощью операции по сохранению груди с последующей лучевой терапией. После операции по удалению опухоли длинные иглы, содержащие радий, вводятся по всей пораженной груди и возле прилегающих подмышечных лимфатических узлов.
1941: Гормональная терапия
Чарльз Хаггинс обнаруживает, что удаление яичек для снижения выработки тестостерона или введение эстрогенов вызывает регрессию опухолей простаты.Такие гормональные манипуляции, более известные как гормональная терапия, продолжают оставаться основой лечения рака простаты.
1947: антиметаболиты
Сидни Фарбер показывает, что лечение антиметаболитным препаратом аминоптерин, производным фолиевой кислоты, вызывает временные ремиссии у детей с острым лейкозом. Антиметаболитные препараты структурно похожи на химические вещества, необходимые для важных клеточных процессов, таких как синтез ДНК, и вызывают гибель клеток, блокируя эти процессы.
1949: Азотная иприта
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) одобряет азотный иприт (мехлорэтамин) для лечения рака. Азотный горчица относится к классу препаратов, называемых алкилирующими агентами, которые убивают клетки, химически модифицируя их ДНК.
1950: Курение сигарет и рак легких
Эрнст Виндер, Эвартс Грэм и Ричард Долл считают курение сигарет важным фактором развития рака легких.
1953: Первое полное излечение твердой опухоли человека
Рой Герц и Мин Чиу Ли достигают первого полного излечения от солидной опухоли человека с помощью химиотерапии, когда они используют метотрексат для лечения пациента с хориокарциномой, редким раком репродуктивной ткани, который в основном поражает женщин.
1958: Комбинированная химиотерапия
Исследователи из NCI Эмиль Фрей, Эмиль Фрейрих, Джеймс Холланд и их коллеги продемонстрировали, что комбинированная химиотерапия с использованием препаратов 6-меркаптопурина и метотрексата может вызывать частичную и полную ремиссию и продлевать выживаемость у детей и взрослых с острым лейкозом.
1960: Филадельфийская хромосома
Питер Новелл и Дэвид Хангерфорд описывают необычно маленькую хромосому в раковых клетках пациентов с хроническим миелогенным лейкозом (ХМЛ). Эта хромосома, известная как филадельфийская хромосома, обнаруживается в лейкозных клетках 95% пациентов с ХМЛ.
1964: Курение сигарет в центре внимания
Главный хирург США выпускает отчет, в котором говорится, что курение сигарет представляет собой серьезную опасность для здоровья в Соединенных Штатах и что необходимо принять меры для уменьшения его вредных последствий.
1964: вирус Эпштейна-Барра
Впервые вирус — вирус Эпштейна-Барра (EBV) — связан с раком человека (лимфома Беркитта). Позднее было показано, что ВЭБ вызывает несколько других видов рака, включая рак носоглотки, лимфому Ходжкина и некоторые виды рака желудка (желудка).
1971: Национальный закон о раке
23 декабря президент Ричард М. Никсон подписывает Национальный закон о борьбе с раком, который уполномочивает директора NCI координировать всю деятельность Национальной программы по борьбе с раком, создавать национальные центры исследований рака и создавать национальные программы борьбы с раком.
Никсон подписывает Национальный закон о борьбе с раком, который уполномочивает директора NCI координировать всю деятельность Национальной программы по борьбе с раком, создавать национальные центры исследований рака и создавать национальные программы борьбы с раком.
1976: ДНК нормальных куриных клеток
Доминик Штехелин, Гарольд Вармус, Дж. Майкл Бишоп и Питер Фогт обнаружили, что ДНК нормальных куриных клеток содержит ген, связанный с онкогеном (вызывающим рак геном) вируса саркомы птиц, который вызывает рак у кур. Это открытие в конечном итоге приводит к открытию онкогенов человека.
1978: Тамоксифен
FDA одобряет тамоксифен, антиэстрогеновый препарат, первоначально разработанный в качестве противозачаточного средства для лечения рака груди.Тамоксифен представляет собой первый из класса препаратов, известных как селективные модуляторы рецепторов эстрогена, или SERM, которые были одобрены для лечения рака.
1979: Ген TP53
Обнаружен ген TP53 (также называемый p53), наиболее часто мутирующий ген при раке человека. Это ген-супрессор опухоли, то есть его белковый продукт (белок p53) помогает контролировать пролиферацию клеток и подавлять рост опухоли.
Это ген-супрессор опухоли, то есть его белковый продукт (белок p53) помогает контролировать пролиферацию клеток и подавлять рост опухоли.
1984: Обнаружен ген HER2
Исследователи обнаружили в клетках крыс новый онкоген, который они назвали «neu.«Человеческая версия этого гена, называемая HER2 (и ErbB2), сверхэкспрессируется примерно в 20-25% случаев рака груди (известных как HER2-положительный рак груди) и связана с более агрессивным заболеванием и плохим прогнозом.
1984: ВПЧ 16 и 18
ДНКвируса папилломы человека (ВПЧ) типов 16 и 18 выявляется в большом проценте случаев рака шейки матки, что позволяет установить связь между инфицированием этими типами ВПЧ и канцерогенезом шейки матки.
1985: Грудосохраняющая хирургия
Результаты клинического исследования, поддерживаемого NCI, показывают, что у женщин с раком груди на ранней стадии, которым была проведена операция по сохранению груди (лампэктомия) с последующей лучевой терапией всей груди, показатели общей выживаемости и выживаемости без признаков заболевания были такими же, как у женщин, которые лечились только мастэктомией.
1986: Клонирование онкогена HER2
Клонирован человеческий онкоген HER2 (также называемый neu и erbB2). Сверхэкспрессия белкового продукта этого гена, которая встречается примерно в 20-25% случаев рака молочной железы (известных как HER2-положительный рак молочной железы), связана с более агрессивным заболеванием и плохим прогнозом.
1993: Анализ гваяковой фекальной скрытой крови (FOBT)
Результаты клинического исследования, поддерживаемого NCI, показывают, что ежегодный скрининг с использованием анализа скрытой крови гваякового кала (FOBT) может снизить смертность от колоректального рака примерно на 33%.
1994: Клонирование гена супрессора опухоли BRCA1
Клонирован ген-супрессор опухоли BRCA1. Специфические наследственные мутации в этом гене значительно увеличивают риск рака груди и яичников у женщин, а также риски некоторых других видов рака как у мужчин, так и у женщин.
1995: Клонирование гена супрессора опухоли BRCA2
Клонирован ген-супрессор опухоли BRCA2. Подобно BRCA1, наследование специфических мутаций гена BRCA2 значительно увеличивает риск рака груди и яичников у женщин, а также риск некоторых других видов рака как у мужчин, так и у женщин.
1996: Анастрозол
FDA одобрило применение анастрозола для лечения прогрессирующего рака молочной железы, положительного по рецепторам эстрогена, у женщин в постменопаузе. Анастрозол — первый ингибитор ароматазы (препарат, блокирующий выработку эстрогена в организме), одобренный для лечения рака.
1997: Ритуксимаб
FDA одобряет ритуксимаб, моноклональные антитела, для использования у пациентов с резистентной к лечению, низкосортной или фолликулярной B-клеточной неходжкинской лимфомой (НХЛ).Позднее ритуксимаб был одобрен в качестве начального лечения этих типов НХЛ, другого типа НХЛ, называемого диффузной крупноклеточной B-клеточной лимфомой, и хронического лимфолейкоза.
1998: Испытание по профилактике рака молочной железы, спонсируемое NCI
Результаты исследования по профилактике рака молочной железы, спонсируемого NCI, показывают, что антиэстрогеновый препарат тамоксифен может снизить заболеваемость раком груди среди женщин с повышенным риском заболевания примерно на 50%. FDA одобряет тамоксифен для снижения заболеваемости раком груди у женщин с повышенным риском.
1998: трастузумаб
FDA одобряет трастузумаб, моноклональное антитело, которое нацелено на раковые клетки, которые продуцируют белок HER2 в избыточном количестве, для лечения женщин с HER2-положительным метастатическим раком груди. Позднее трастузумаб был одобрен для адъювантного (послеоперационного) лечения женщин с HER2-положительным раком молочной железы на ранней стадии.
2001: мезилат иматиниба
Результаты клинических испытаний показывают, что препарат иматиниба мезилат, нацеленный на уникальный белок, продуцируемый филадельфийской хромосомой, эффективен против хронического миелогенного лейкоза (ХМЛ). Позже было показано, что он также эффективен при лечении опухолей стромы желудочно-кишечного тракта (GIST).
Позже было показано, что он также эффективен при лечении опухолей стромы желудочно-кишечного тракта (GIST).
2003: Исследование по профилактике рака простаты, спонсируемое NCI (PCPT)
Результаты исследования по профилактике рака простаты (PCPT), спонсируемого NCI, показывают, что препарат финастерид, который снижает выработку мужских гормонов в организме, снижает риск рака простаты у мужчин примерно на 25%.
2006: Исследование тамоксифена и ралоксифена NCI (STAR)
Результаты исследования тамоксифена и ралоксифена (STAR) NCI показывают, что женщины в постменопаузе с повышенным риском рака груди могут снизить риск развития заболевания, если они принимают антиэстрогеновый препарат ралоксифен.Риск серьезных побочных эффектов ниже при приеме ралоксифена, чем при приеме тамоксифена.
2006: Гардасил
FDA одобряет вакцину против ВПЧ Гардасил, которая защищает от инфекции двумя типами ВПЧ, которые вызывают примерно 70% всех случаев рака шейки матки. Ученые NCI разработали базовую технологию, используемую для производства Гардасила.
Ученые NCI разработали базовую технологию, используемую для производства Гардасила.
2009: Cervarix
FDA одобряет Церварикс, вторую вакцину, которая защищает от заражения двумя типами ВПЧ, вызывающими примерно 70% всех случаев рака шейки матки во всем мире.Ученые NCI разработали базовую технологию, используемую для производства Cervarix.
2010: Первая вакцина для лечения рака человека
FDA одобряет сипулеуцел-Т, вакцину для лечения рака, которая производится с использованием клеток собственной иммунной системы пациента (дендритных клеток), для лечения метастатического рака простаты, который больше не поддается гормональной терапии. Это первая (и пока единственная) вакцина для лечения рака человека, получившая одобрение.
2010: Скрининговое исследование рака легких, спонсируемое NCI (NLST)
Первоначальные результаты исследования скрининга рака легких (NLST), спонсируемого NCI, показывают, что скрининг с помощью спиральной компьютерной томографии (КТ) с низкой дозой снизил смертность от рака легких примерно на 20% в большой группе нынешних и бывших заядлых курильщиков.
2011: Ипилимумаб
FDA одобряет использование ипилимумаба, моноклональных антител, для лечения неоперабельной или метастатической меланомы. Ипилимумаб стимулирует иммунную систему атаковать раковые клетки, устраняя «тормоз», который обычно контролирует интенсивность иммунных ответов.
2012: Скрининговое исследование рака PLCO, спонсируемое NCI
Результаты исследования рака PLCO, спонсируемого NCI, подтверждают, что скрининг людей в возрасте 55 лет и старше на колоректальный рак с использованием гибкой сигмоидоскопии снижает заболеваемость и смертность от колоректального рака.В исследовании PLCO у прошедших скрининг лиц риск развития колоректального рака был на 21% ниже, а риск смерти от этого заболевания на 26% ниже, чем у контрольных субъектов.
2013: Адо-трастузумаб эмтанзин (T-DM1)
FDA одобряет адо-трастузумаб эмтанзин (T-DM1) для лечения пациентов с HER2-положительным раком молочной железы, которые ранее получали трастузумаб и / или препараты таксана. T-DM1 представляет собой иммунотоксин (конъюгат антитело-лекарственное средство), который получают путем химического связывания моноклонального антитела трастузумаб с цитотоксическим агентом мертансином, который ингибирует пролиферацию клеток, блокируя образование микротрубочек.
T-DM1 представляет собой иммунотоксин (конъюгат антитело-лекарственное средство), который получают путем химического связывания моноклонального антитела трастузумаб с цитотоксическим агентом мертансином, который ингибирует пролиферацию клеток, блокируя образование микротрубочек.
2014: Анализ ДНК при раке
Исследователи из проекта Атлас генома рака (TCGA), совместного усилия NCI и Национального исследовательского института генома человека по анализу ДНК и других молекулярных изменений в более чем 30 типах рака человека, обнаружили, что рак желудка (желудка) на самом деле является четыре различных заболевания, а не только одно, основанные на различных характеристиках опухоли. Это открытие TCGA и других связанных проектов может потенциально привести к новой системе классификации рака, в которой раковые образования классифицируются по их молекулярным аномалиям, а также по месту происхождения их органа или ткани.
2014: пембролизумаб
FDA одобряет пембролизумаб для лечения запущенной меланомы.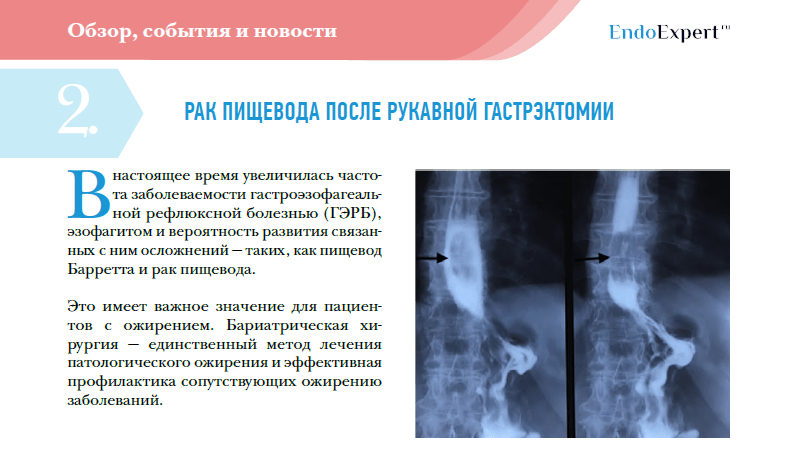 Это моноклональное антитело блокирует активность белка PD1 на иммунных клетках, что увеличивает силу иммунного ответа против рака.
Это моноклональное антитело блокирует активность белка PD1 на иммунных клетках, что увеличивает силу иммунного ответа против рака.
2014: Гардасил 9
FDA одобряет Гардасил 9, вакцину, которая защищает от заражения теми же четырьмя типами ВПЧ, что и Гардасил, плюс еще пять канцерогенных типов ВПЧ, которые вместе составляют почти 90% случаев рака шейки матки.В настоящее время это единственная вакцина против ВПЧ, доступная в США.
2015: Клиническое исследование NCI-MATCH
NCI и группа исследований рака ECOG-ACRIN запускают клиническое испытание NCI-MATCH (молекулярный анализ для выбора терапии) для тестирования более 20 лекарств и комбинаций лекарств, основанных на молекулярном анализе опухолей у людей с раком. Исследование призвано определить, будет ли таргетная терапия для людей, опухоли которых имеют определенные генные мутации, эффективными, независимо от типа рака.
2015: Talimogen Laherparepvec
FDA одобряет талимоген лахерпарепвек (T-VEC) для лечения некоторых пациентов с метастатической меланомой, которую нельзя удалить хирургическим путем. T-VEC, первый онколитический вирус, одобренный для клинического использования, работает, заражая и убивая опухолевые клетки и стимулируя иммунный ответ против раковых клеток по всему телу.
T-VEC, первый онколитический вирус, одобренный для клинического использования, работает, заражая и убивая опухолевые клетки и стимулируя иммунный ответ против раковых клеток по всему телу.
2016: Рак Moonshot℠
Конгресс принимает Закон о лечении рака 21 века, который обеспечивает финансирование Cancer Moonshot, широкой программы по ускорению исследований рака путем инвестирования в конкретные исследовательские инициативы, которые могут изменить лечение, обнаружение и профилактику рака.
2017: педиатрический MATCH
NCI и Группа детской онкологии запускают Pediatric MATCH, попытку расширить молекулярный анализ и целевое лечение детей и подростков, больных раком. Как и NCI-MATCH, Pediatric MATCH стремится определить, будет ли эффективным лечение опухолей лекарственными средствами молекулярной направленности на основе генетических характеристик опухоли, а не типа рака или локализации рака.
2017: CAR Т-клеточная терапия
FDA одобряет tisagenlecleucel для лечения формы острого лимфобластного лейкоза у некоторых детей и молодых людей. Впоследствии FDA одобряет использование аксикабтагена цилолейцела для пациентов с крупными В-клеточными лимфомами, у которых рак прогрессировал после получения по крайней мере двух предыдущих схем лечения. Оба метода лечения представляют собой Т-клеточную терапию с использованием химерных рецепторов антигена (CAR), индивидуальную для каждого пациента. Для создания этих методов лечения Т-клетки удаляются из пациента, генетически изменяются для распознавания раковых антигенов, выращиваются в больших количествах в лаборатории, а затем вводятся обратно пациенту, чтобы стимулировать его иммунную систему атаковать раковые клетки.
Впоследствии FDA одобряет использование аксикабтагена цилолейцела для пациентов с крупными В-клеточными лимфомами, у которых рак прогрессировал после получения по крайней мере двух предыдущих схем лечения. Оба метода лечения представляют собой Т-клеточную терапию с использованием химерных рецепторов антигена (CAR), индивидуальную для каждого пациента. Для создания этих методов лечения Т-клетки удаляются из пациента, генетически изменяются для распознавания раковых антигенов, выращиваются в больших количествах в лаборатории, а затем вводятся обратно пациенту, чтобы стимулировать его иммунную систему атаковать раковые клетки.
2017: Одобрение пембролизумаба в отношении онкологических заболеваний
FDA продлевает одобрение пембролизумаба для лечения метастатических и неоперабельных солидных опухолей, которые имеют определенные генетические изменения, где бы они ни происходили в организме, которые прогрессировали после предшествующего лечения и не имеют альтернативных вариантов лечения. Благодаря этому одобрению, не зависящему от тканей, пембролизумаб становится первым препаратом для лечения рака, основанным исключительно на наличии генетической особенности опухоли, а не на типе рака человека.
Благодаря этому одобрению, не зависящему от тканей, пембролизумаб становится первым препаратом для лечения рака, основанным исключительно на наличии генетической особенности опухоли, а не на типе рака человека.
2017: Тесты геномного профилирования
FDA разрешает два продукта для тестирования опухолей на предмет генетических изменений, которые могут сделать опухоли восприимчивыми к лечению одобренными FDA лекарствами молекулярной направленности. В ноябре FDA санкционирует тест MSK-IMPACT, разработанный и используемый онкологическим центром Memorial Sloan Kettering Cancer Center для анализа опухолей на предмет потенциально действенных изменений в 468 генах, связанных с раком. В декабре FDA одобряет тест FoundationOne CDx, который оценивает генетические изменения в 324 генах, которые, как известно, способствуют росту рака.Тест FoundationOne служит дополнительной диагностикой для нескольких одобренных FDA лекарств, направленных на борьбу с пятью распространенными типами рака.
2018: TCGA PanCancer Atlas
финансируемых Национальным институтом здравоохранения исследователей с TCGA завершили углубленный геномный анализ 33 типов рака. PanCancer Atlas предоставляет подробный геномный анализ молекулярных и клинических данных по более чем 10 000 опухолей, что дает исследователям рака беспрецедентное понимание того, как, где и почему возникают опухоли у людей.
2018: Клиническое исследование TAILORx, спонсируемое NCI,
Результаты клинического исследования, спонсируемого NCI по назначению индивидуальных вариантов лечения (Rx), или TAILORx, показывают, что большинству женщин с раком груди на ранней стадии не помогает химиотерапия после операции. В исследовании использовался молекулярный тест, который оценивает экспрессию 21 гена, связанного с рецидивом рака молочной железы, чтобы назначить женщин с ранней стадией, гормонально-положительным, HER2-отрицательным раком молочной железы, который не распространился на лимфатические узлы, в наиболее подходящие и эффективное послеоперационное лечение. Это одно из первых испытаний, посвященных изучению способа персонализации лечения рака
Это одно из первых испытаний, посвященных изучению способа персонализации лечения рака
2018: ларотректиниб
FDA одобряет ларотректиниб, первый препарат, нацеленный на опухоли со слиянием генов NTRK . Одобрение предназначено для педиатрических или взрослых пациентов с метастатическими или неоперабельными солидными опухолями, которые ухудшились после предыдущего лечения в любой части тела, вызванного слиянием гена NTRK без известной приобретенной мутации устойчивости. Ларотректиниб — второй препарат, одобренный для лечения рака с определенными молекулярными особенностями, независимо от того, где находится рак.
2020: Международный панкологический анализ полных геномов
Консорциум международных исследователей анализирует более 2600 полных геномов 38 типов рака и соответствующих нормальных тканей, чтобы определить общие закономерности молекулярных изменений. Исследование Pan-Cancer Analysis of Whole Genomes, в котором использовались данные, собранные International Cancer Genome Consortium и TCGA, раскрывает сложную роль, которую изменения всего генома играют в развитии, росте и распространении рака. Исследование также расширяет геномный анализ рака за пределы областей, кодирующих белок, на полный генетический состав клеток.
Исследование также расширяет геномный анализ рака за пределы областей, кодирующих белок, на полный генетический состав клеток.
Рак: историческая перспектива | SEER Обучение
С тех пор, как хранились самые ранние медицинские записи, рак как болезнь была описана в истории медицины. Самые ранние известные описания рака появляются в семи папирусах, обнаруженных и расшифрованных в конце 19 века.Они предоставили первое прямое знание египетской медицинской практики. Два из них, известные как папирусы «Эдвин Смит» и «Джордж Эберс», содержат описания рака, написанные около 1600 г. до н. Э., И, как полагают, датируются источниками еще 2500 г. до н. Э. Папирус Смита описывает хирургию, а папирус Эберса описывает фармакологические, механические и магические методы лечения.
На основании информации, записанной на папирусах и иероглифических надписях, древние египтяне смогли отличить доброкачественные опухоли от злокачественных. Они также могли использовать различные методы лечения, включая хирургическое вмешательство и другие методы лечения.
Они также могли использовать различные методы лечения, включая хирургическое вмешательство и другие методы лечения.
После упадка Египта следующие главы медицинской и научной истории были написаны в Греции и Риме. Великие врачи Гиппократ и Гален доминировали в медицинской мысли на протяжении 1500 лет. Они вывели медицину из области магии, суеверий и религии. Гиппократ и Гален определили болезнь как естественный процесс, лечение которого основано на наблюдениях и опыте.Были выявлены раковые заболевания с предупреждением о недопустимости лечения более тяжелых форм. Гиппократу приписывают название «рак» как «каркинома» (карцинома), потому что опухоль выглядела как «краб» («каркинома» в переводе с греческого означает «краб») в том смысле, что у опухоли есть центральное тело и появилось расширение опухоли. как ножки «краба».
После падения Рима Константинополь стал интеллектуальным хранилищем цивилизации. Оттуда в арабских переводах классические греческие и римские тексты вернулись через Европу. Древние учения Галена продолжали вдохновлять врачей в Константинополе, Каире, Александрии, Афинах и Антиохии в то время, когда на Западе доминировали магические заклинания и мифы. Рак продолжали объяснять как результат избытка черной желчи, излечимой только на самых ранних стадиях.
Древние учения Галена продолжали вдохновлять врачей в Константинополе, Каире, Александрии, Афинах и Антиохии в то время, когда на Западе доминировали магические заклинания и мифы. Рак продолжали объяснять как результат избытка черной желчи, излечимой только на самых ранних стадиях.
В современном мире наука и хирургия продвинулись вперед, когда врачи вернулись к непосредственному наблюдению за человеческим телом. Однако теория о том, что рак вызывается избытком черной желчи, продолжала преобладать в 16 веке.Рак считался неизлечимым, хотя для лечения его проявлений были разработаны самые разные пасты, содержащие мышьяк. В 17 веке старая теория болезней, основанная на телесных жидкостях, была отброшена, когда Гаспаре Аселли открыл сосуды лимфатической системы и предположил, что лимфатические аномалии являются основной причиной рака.
Отвергнув теорию 17 века о причине рака, французский врач Клод Жендрон. Он пришел к выводу, что рак возникает локально в виде твердой растущей массы, не поддающейся лечению с помощью лекарств, и ее необходимо удалить со всеми ее «нитями».![]() «
«
Два французских ученых 18-го века, врач Жан Астрюк и химик Бернар Пейриль, провели эксперименты, чтобы подтвердить или опровергнуть гипотезы, связанные с раком. Их усилия, какими бы абсурдными они ни казались в ретроспективе, установили экспериментальную онкологию, науку поиска лучших диагнозов, лечения и понимания причин рака. В течение этого периода были зарегистрированы случаи рака в окружающей среде, и были открыты больницы, специализирующиеся на лечении рака.
В конце 19-го века разработка более совершенных микроскопов не только помогла документировать и определить болезнетворные организмы, но также сделала возможным исследование клеток и клеточной активности.Изучение раковых тканей и опухолей показало, что раковые клетки заметно отличались по внешнему виду от нормальных клеток окружающей ткани или клеток, из которых они произошли. Исследователи начали сосредотачиваться на таких вопросах, как происхождение клеток и связь болезни с поведением клетки. Изобретением микроскопа была обнаружена сама раковая клетка.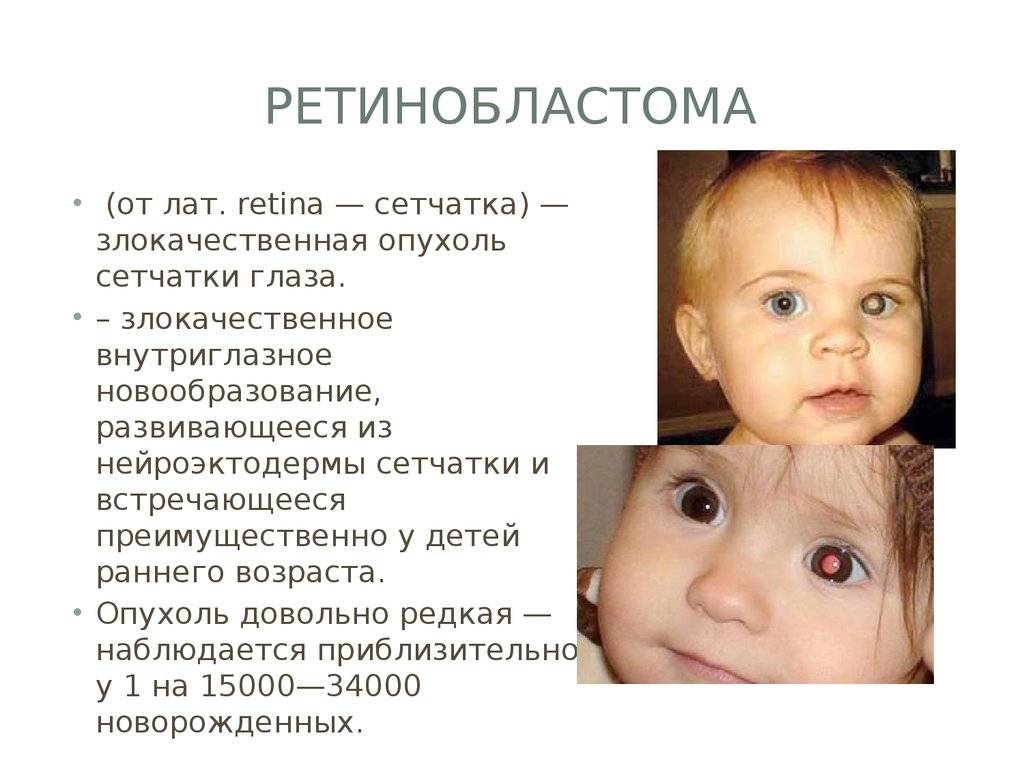
В начале 20 века были достигнуты большие успехи в понимании структур, функций и химии живых организмов.Исследования рака в клеточных культурах, химические канцерогены, методы диагностики и химиотерапия прочно утвердили онкологию как науку. Исследователи преследовали различные теории происхождения рака, подвергая свои гипотезы систематическим экспериментам. Вирусная причина рака у кур была задокументирована в 1911 году, и были окончательно идентифицированы как химические, так и физические канцерогены. Хромосомные аномалии также исследовались как возможные причины рака.
В 1913 году необходимость борьбы с растущим общественным страхом и невежеством в отношении рака привела к двум значительным событиям: публикации первой известной статьи о тревожных признаках рака в популярном женском журнале и формированию общенациональной организации, посвященной просвещению населения по вопросам рака. .Рак, как болезнь, вышел на свет.
В 1937 году Конгресс США объявил борьбу с раком национальной целью, единогласно приняв Закон о Национальном институте рака. В соответствии с этим законом был создан Национальный институт рака, который должен был открыть новые теоретические основы путем проведения собственных исследований, содействия исследованиям в других учреждениях и координации проектов и мероприятий, связанных с раком. В 1971 году президент Ричард М. Никсон подписал Национальный закон о раке, запустив Национальную программу по борьбе с раком, управляемую Национальным институтом рака.Ключевые события в истории законодательства США о национальной политике в области рака с 1937 по 1999 годы доступны здесь.
В соответствии с этим законом был создан Национальный институт рака, который должен был открыть новые теоретические основы путем проведения собственных исследований, содействия исследованиям в других учреждениях и координации проектов и мероприятий, связанных с раком. В 1971 году президент Ричард М. Никсон подписал Национальный закон о раке, запустив Национальную программу по борьбе с раком, управляемую Национальным институтом рака.Ключевые события в истории законодательства США о национальной политике в области рака с 1937 по 1999 годы доступны здесь.
С момента своего основания фундаментальные биомедицинские исследования, проводимые при поддержке Национального института рака, продвинули понимание рака. Используя инструменты молекулярной биологии и молекулярной генетики, ученые делают большие шаги в открытии и картировании связей между хромосомами, внутренними генами и раком. В дополнение к традиционным методам лечения рака, потенциальные решения по профилактике и лечению рака кажутся ограниченными только воображением.
Как давно появился рак?
Рак сейчас у всех на уме. Многие фармацевтические компании занимаются исключительно поиском новых методов лечения рака. В 2016 году президент Обама призвал ученых «положить конец известному нам раку». и подписал счет на 6,3 миллиарда долларов на лечение наркозависимости. Но рак — это далеко не новость. Королева Мария (также известная как «Кровавая Мэри») умерла от рака яичников в 1558 году.Но это мелочь для некоторых более старых, заметных случаев рака. Самый старый зарегистрированный случай, который мы зарегистрировали, был обнаружен в Египте с 3000 г. до н.э. Самое раннее свидетельство рака у гоминидов было обнаружено на пальце ноги 1,7-миллионного родственника человека, обнаруженного в Южной Африке.
Источник фото: pexels.com
Тем не менее, рак существует гораздо дольше, чем гоминиды бродили по земле. Ученые из Германии недавно обнаружили очень злокачественную опухоль в окаменелой кости ноги стволовой черепахи. Доктора Надя Фребиш, доктор философии, из Музея естественной истории Института Лейбница, и Брюс М. Ротшильд, доктор медицины, из Музея естественной истории Карнеги в Питтсбурге, сотрудничали в проекте, который выявил самых старых свидетельств рака. назначить свидание. Это была злокачественная опухоль, обнаруженная в кости черепахи возрастом 240 миллионов лет. Это говорит о том, что рак было около , по крайней мере, с триасового периода, около 250 миллионов лет назад. Результаты были недавно опубликованы в журнале JAMA Oncology .
Доктора Надя Фребиш, доктор философии, из Музея естественной истории Института Лейбница, и Брюс М. Ротшильд, доктор медицины, из Музея естественной истории Карнеги в Питтсбурге, сотрудничали в проекте, который выявил самых старых свидетельств рака. назначить свидание. Это была злокачественная опухоль, обнаруженная в кости черепахи возрастом 240 миллионов лет. Это говорит о том, что рак было около , по крайней мере, с триасового периода, около 250 миллионов лет назад. Результаты были недавно опубликованы в журнале JAMA Oncology .
Исследователи использовали палеопатологию, изучение древних болезней, чтобы изучить рак на филогенетическом древе. Это делается для того, чтобы понять потенциальные первопричины; какие виды более восприимчивы к раку, чем другие; и как распространенность рака изменилась в ходе эволюции. Этот последний пункт особенно информативен, поскольку число случаев рака у людей увеличилось по сравнению с случаями рака, обнаруженными в палеонтологической летописи. Увеличение числа случаев заболевания людей объясняется экологическими и генетическими изменениями.
Увеличение числа случаев заболевания людей объясняется экологическими и генетическими изменениями.
Источник фото: PixaBay.com
Интересная теория, которая помогает объяснить увеличение числа случаев рака, заключается в том, что люди просто живут дольше. Многие виды рака не проявляются до старости. Когда средняя продолжительность жизни человека составляла от 30 до 35 лет, было меньше случаев рака, потому что мы просто не жили так долго, чтобы болезнь проявилась. По сути, сначала вас убьет что-то другое. Тот факт, что уровень заболеваемости раком растет, свидетельствует о том, насколько мы увеличили среднюю продолжительность жизни с помощью современной медицины, нейтрализации хищничества и снижения (в среднем) уровня детской смертности.Многие говорят об использовании CBD и для лечения рака. К сожалению, в большинстве случаев полностью вылечить рак у человека невозможно. Люди также находят способы помочь своим семьям пережить финансовый стресс после их смерти, приобретая гарантированное страхование жизни или передавая сбережения / активы.
К сожалению, эти данные из летописи окаменелостей указывают на то, что мы имеем дело с очень старой болезнью. Возможно, поэтому лекарства от рака так долго ускользали от нас.Как мы развивались, так и происходит. Как хорошо известно многим онкологам, рак — это движущаяся мишень. Таким образом, наша древняя родословная наделила нас генами, способными вызывать рак. И наш современный образ жизни (еда, упражнения, факторы стресса) может использовать этот потенциал и включить эти древние гены.
Источники : USA Today, Biography.com, LiveScience.com, www.cancer.org, www.NaturalGeographic.com, JAMA Oncology, www.PsychologyToday.com
История рака молочной железы: хронология
Рак молочной железы это самый распространенный рак у женщин во всем мире.Он широко изучался на протяжении всей истории.
Фактически, исследования рака груди помогли проложить путь к прорывам в других типах исследований рака.
То, как мы лечим рак груди, во многом изменилось с момента первого открытия рака. Но другие результаты и методы лечения оставались неизменными в течение многих лет.
Но другие результаты и методы лечения оставались неизменными в течение многих лет.
Прочтите, чтобы узнать, как методы лечения рака груди превратились в то, что мы знаем сегодня.
Люди давно знают о раке груди.Например, Хирургический папирус Эдвина Смита описывает случаи рака груди. Этот медицинский текст датируется 3000-2500 гг. До н. Э.
В Древней Греции люди приносили по обету подношения в форме груди богу медицины. А Гиппократ описал стадии рака груди в начале 400-х годов до н. Э.
В первом веке врачи экспериментировали с хирургическими разрезами для уничтожения опухолей. Они также думали, что рак груди связан с окончанием менструации. Эта теория, возможно, подтолкнула к ассоциации рака с пожилым возрастом.
В начале средневековья медицинский прогресс переплетался с новыми религиозными философиями. Христиане считали хирургическое вмешательство варварским и поддерживали исцеление верой. Тем временем исламские врачи изучили греческие медицинские тексты, чтобы узнать больше о раке груди.
В эпоху Возрождения хирургия возродилась, врачи изучали человеческое тело. Джон Хантер, известный как шотландский отец исследовательской хирургии, определил лимфу как причину рака груди. Лимфа — это жидкость, переносящая лейкоциты по всему телу.
Лампэктомии также проводились хирургами, но анестезии еще не было. Чтобы добиться успеха, хирурги должны действовать быстро и аккуратно.
Наш современный подход к лечению и исследованиям рака груди начал формироваться в 19 веке. Рассмотрим эти вехи:
- 1882: Уильям Холстед выполнил первую радикальную мастэктомию. Эта операция останется стандартной операцией для лечения рака груди вплоть до 20 века.
- 1895: Сделан первый рентгеновский снимок.В конце концов, для выявления рака груди будут использоваться рентгеновские лучи с низкой дозой, называемые маммограммами.
- 1898: Мари и Пьер Кюри открывают радиоактивные элементы радий и полоний.
 Вскоре после этого радий используется для лечения рака.
Вскоре после этого радий используется для лечения рака. - 1932: Разработан новый подход к мастэктомии. Хирургическая процедура не так уродлива и становится новым стандартом.
- 1937: Лучевая терапия используется в дополнение к хирургическому вмешательству для сохранения груди.После удаления опухоли иглы с радием вводятся в грудь и возле лимфатических узлов.
- 1978: Тамоксифен (Нолвадекс, Солтамокс) одобрен Управлением по контролю за продуктами и лекарствами (FDA) для использования при лечении рака груди. Этот антиэстрогеновый препарат является первым в новом классе препаратов, называемых селективными модуляторами рецепторов эстрогена (SERM).
- 1984: Исследователи обнаружили новый ген у крыс. Человеческая версия, HER2, связана с более агрессивным раком груди при сверхэкспрессии.Он называется HER2-положительным раком молочной железы и не поддается лечению.
- 1985: Исследователи обнаружили, что женщины с ранней стадией рака груди, которым была проведена лампэктомия и лучевая терапия, имеют такие же показатели выживаемости, как и женщины, получившие только мастэктомию.

- 1986: Ученые выяснили, как клонировать ген HER2.
- 1995: Ученые могут клонировать гены-супрессоры опухолей BRCA1 и BRCA2. Унаследованные мутации в этих генах могут предсказывать повышенный риск рака груди.
- 1996: FDA одобряет анастрозол (аримидекс) в качестве средства лечения рака груди. Этот препарат блокирует выработку эстрогена.
- 1998: Тамоксифен снижает риск развития рака груди у женщин из групп риска на 50 процентов. Теперь он одобрен FDA для использования в качестве профилактической терапии.
- 1998: Трастузумаб (Герцептин), препарат, нацеленный на раковые клетки, которые продуцируют избыточно HER2, также одобрен FDA.
- 2006: Ралоксифен (Evista), действующий на основе SERM, снижает риск рака груди у женщин в постменопаузе, которые имеют более высокий риск.Он имеет меньшую вероятность серьезных побочных эффектов, чем тамоксифен.

- 2011: Большой метаанализ показывает, что лучевая терапия значительно снижает риск рецидива рака груди и смертность.
- 2013: Четыре основных подтипа рака груди определены как HR + / HER2 («просвет A»), HR- / HER2 («тройной отрицательный»), HR + / HER2 + («просвет B») и HR-. / HER2 + («обогащенный HER2»).
- 2017: Первый биоподобный препарат Огиври (трастузумаб-dkst) одобрен FDA для лечения рака груди.В отличие от дженериков, биосимиляры являются копиями биологических препаратов и стоят меньше, чем брендовые препараты.
- 2018: Клинические испытания показывают, что химиотерапия после операции не приносит пользы 70 процентам женщин с раком груди на ранней стадии.
- 2019: Enhertu одобрен FDA, и этот препарат оказался очень эффективным при лечении HER2-положительного рака молочной железы, который имеет метастазы или не может быть удален хирургическим путем.

- 2020: Лекарство Trodelvy одобрено FDA для лечения метастатического тройного отрицательного рака груди у людей, которые не ответили как минимум на два других лечения.
Лечение рака груди становится все более индивидуальным, поскольку врачи узнают больше об этом заболевании.
Сейчас это заболевание рассматривается как заболевание с подтипами, которые имеют разные паттерны и способы воздействия на организм. Возможность выделять определенные гены и классифицировать рак груди — это начало более индивидуальных вариантов лечения.
Специальные тесты также могут рассказать врачам больше о раке груди.
Например, тест профиля гена Oncotype DX может исследовать часть опухоли, чтобы выяснить, какие гены в ней активны.
Врачи могут определить, какие пациенты с раком груди на ранней стадии можно лечить только антиэстрогенами, а кому может потребоваться дополнительная химиотерапия.
Менее инвазивные и менее токсичные методы
Метод дозорных лимфатических узлов выявил первые лимфатические узлы, по которым может распространяться рак. Это позволяет удалить меньше лимфатических узлов.
Это позволяет удалить меньше лимфатических узлов.
Исследования также показали, что более короткие курсы облучения и более целенаправленные формы лучевой терапии могут быть столь же эффективными, как и более длительные курсы облучения.Это включает доставку лучевой терапии во время операции для некоторых пациентов.
Кроме того, таргетная и биологическая терапия может позволить врачам избегать химиотерапии в определенных ситуациях. Большое исследование 2018 года показало, что адъювантная эндокринная терапия и химиоэндокринная терапия были одинаково эффективны при определенных типах рака груди.
Мы прошли долгий путь со времен Древней Греции, но нам еще многое предстоит узнать о том, как формируется рак груди и как его лечить.
По данным Американского онкологического общества, в 2019 году в США у 268 600 женщин и 2670 мужчин был диагностирован рак груди.
Раннее выявление и лечение по-прежнему считаются лучшей линией защиты от рака груди. Современные технологии позволяют исследователям учиться быстрее, чем десятилетия назад.

 Шталь и Хоффман предположили, что рак состоит из ферментирующей и дегенерирующей лимфы, различающейся по плотности, кислотности и щелочности. Джон Хантер, шотландский хирург 1700-х годов, согласился с тем, что опухоли растут из лимфы, постоянно выделяемой из крови.
Шталь и Хоффман предположили, что рак состоит из ферментирующей и дегенерирующей лимфы, различающейся по плотности, кислотности и щелочности. Джон Хантер, шотландский хирург 1700-х годов, согласился с тем, что опухоли растут из лимфы, постоянно выделяемой из крови.
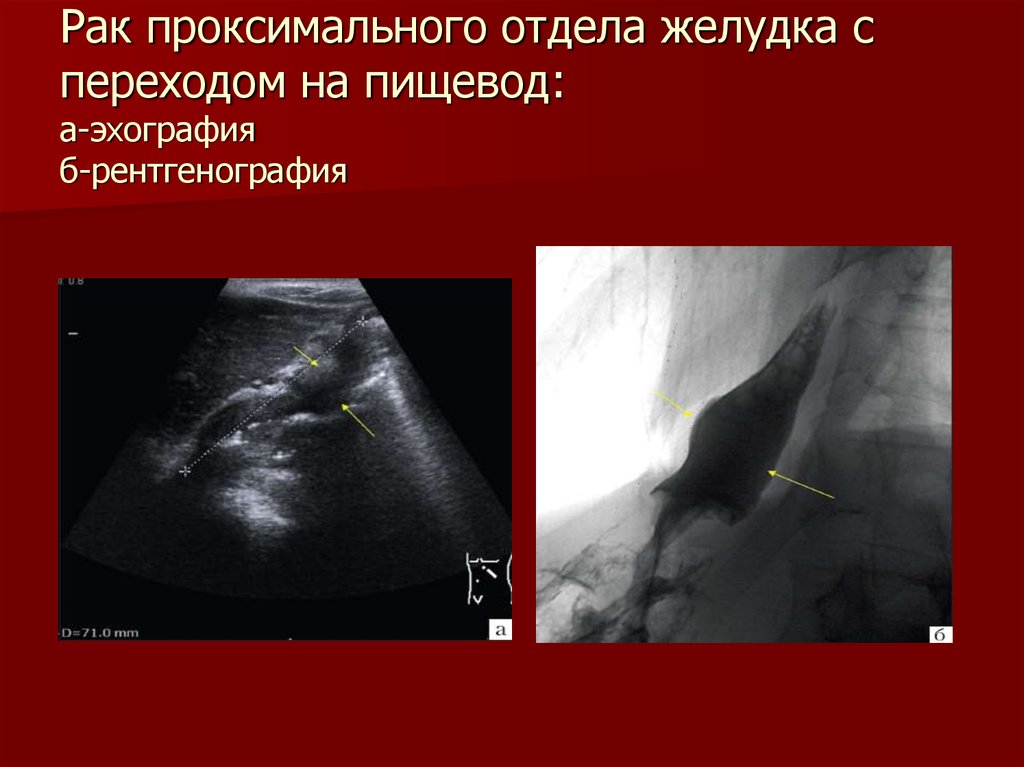 Вскоре после этого радий используется для лечения рака.
Вскоре после этого радий используется для лечения рака.